| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学知识点总结《化学平衡常数》高频考点巩固(2017年模拟版)(一)
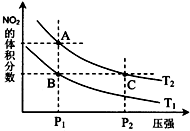 2、填空题 温室气体二氧化碳减排的一种方法是:从燃煤电厂或天然气电厂排放气中回收CO2,再与CH4热解炉产生的H2反应生成CH3OH. (1)500℃时,在体积为1L的容积固定的密闭容器中,充入1molCO2和3molH2,测得CO2和CH3OH(g)的浓度随时间变化如图1所示. 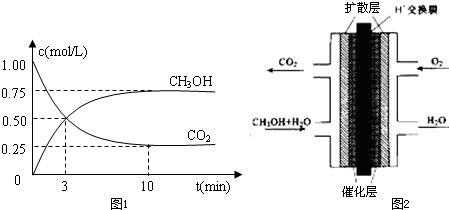 ①从反应开始到平衡,氢气的平均反应速率v(H2)=______mol?L-1?min-1. ②该反应的平衡常数K=______(保留一位小数),平衡时H2的转化率为______. ③已知温度升高,K值减小.下列措施中能使
A.升高温度B.充入He(g),使体系压强增大 C.将H2O(g)从体系中分离D.再充入1molCO2和3molH2 (2)CH3OH作为内燃机燃料或通过燃料电池驱动车辆.可减少CO2排放多达45%. ①已知: CH3OH(g)+H2O(g)═CO2(g)+3H2(g)△H1=+49.0kJ?mol-1 2H2(g)+O2(g)═2H2O(g)△H=-483.6kJ?mol-1 则反应CH3OH(g)+
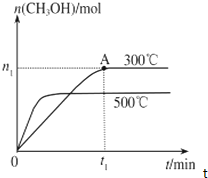
②甲醇质子交换膜燃料电池的结构示意图如图2,已知H+移向通入O2的电极,甲醇进入______极(填“正”或“负”),正极发生的电极反应为______. 3、填空题 PCl5的热分解反应如下:PCl5(g)?PCl3(g)+Cl2(g) 4、选择题 在容积为2L的密闭容器中进行反应:CO(g)+2H2(g)?CH3OH(g),其他条件不变,在300℃和500℃时,物质的量n(CH3OH)-反应时间t的变化曲线如图,下列说法正确的是( ) |
5、填空题 80℃时,将0.40mol的N2O4气体充入2 L已经抽空的固定容积的密闭容器中,发生如下反应:
N2O4 2NO2,△H>0隔一段时间对该容器内的物质进行分析,得到如下数据
2NO2,△H>0隔一段时间对该容器内的物质进行分析,得到如下数据
(1)计算20s-40s内用N2O4表示的平均反应速率为______________mol·L-1·s-1
(2)计算在80℃时该反应的平衡常数K=_______________;
(3)要增大该反应的K值,可采取的措施有(填序号)__________________;
A.增大N2O4的起始浓度
B.向混合气体中通入NO2
C.使用高效催化剂
D.升高温度
(4)如图是80℃时容器中N2O4物质的量的变化曲线,请在该图中补画出该反应在60℃时N2O4物质的量的变化曲线。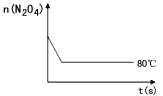
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学知识点总结《热化学方程.. | |