微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 不久前,美国一个海军航空站安装了一 台250 kW的MCFC型燃料电池,该电池可同时供应电和水蒸气,其工作温度为600 ℃~700 ℃,所用燃料为H2,电解质为熔融的K2CO3,已知该电池的总反应为2H2+O2=2H2O, 负极反应为H2+ CO32--2e-=H2O+CO2,则下列推断正确的是? (?)
A.正极反应为:4OH- =O2+2H2O+4e-
B.放电时 CO32-向负极移动
C.电池供应1 mol水蒸气,转移的电子数为4 mol
D.放电时CO32-向正极移动
参考答案:B
本题解析:A、根据总反应和负极反应方程式,二者相减得正极反应式为O2+2 CO2+4e-= 2CO32-,错误;B、原电池装置中阴离子向负极移动,正确;C、根据负极反应式判断电池供应1 mol水蒸气,转移的电子数为2 mol,错误;D、与B相反,错误,答案选B。
本题难度:一般
2、填空题 (16分)如右图所示,A、B、C三个装置中的三个烧杯分别盛有足量的CuCl2溶液。?

A(左Zn右Cu)? B(左C右Pt)? C(左Zn右Cu)
(1)、A、B、C三个装置中属于原电池的是_____ (填标号,下同),属于电解池的是___?_________。
(2)、A池中Zn是_______极,发生_______反应(填“氧化”或“还原”,下同),电极反应式为_________; Cu是_____极, 发生_____反应, 电极反应式为?,A中总反应的化学方程式为?。
(3)、B池中C是_____极,发生_____反应,电极反应为?;Pt是_____极,发生______反应,电极反应为?。B池中总反应的化学方程式为? ________________。
(4) C池中Zn是_____极,发生______反应,电极反应为_______________;Cu是?极, 发生?反应, 电极反应为??反应过程中,溶液浓度________(填“变大”“变小”或“不变”)。
参考答案:(1)A; B、C;
(2)负,氧化,Zn-2e-=Zn2+;正,还原,Cu2++2e-=Cu; Zn+CuCl2=Cu+ Zn Cl2;
(3)阴,还原,Cu2++2e-=Cu;阳,氧化,2Cl--2e-=Cl2↑; CuCl2?Cu+Cl2↑;
(4)阴,还原,Cu2++2e-=Cu;阳,氧化,Cu-2e-=Cu2+;不变;
本题解析:略
本题难度:简单
3、计算题 (6分)(1) 将铁片和铜片用导线连接并插入足量的CuSO4溶液中,当导线上有0.2mol电子通过时,从理论上分析铁片和铜片的质量变化(写出计算过程);
(2) 将(1)的反应中的铜片和导线去掉,也能发生反应,同样发生0.2mol电子转移时,铁片上的质量又如何变化?(简要地写出计算过程)
参考答案:(1)铁片质量减少5.6g,铜片质量增加6.4g
(2)铁片增重0.8g
本题解析:考查原电池的有关计算。在原电池中较活泼的金属作负极,失去电子,发生氧化反应。电子经导线传递到正极上,所以溶液中的阳离子向正极移动,阴离子向负极移动。正极得到电子,发生还原反应。所以铁是负极,铜是正极,溶液中的铜离子得到电子而形成铜。如果不用导线相连,则铁直接和硫酸铜发生置换反应。
(1)铁比铜活泼,铁是负极,铜是正极,电极反应式分别是
Fe?-? 2e-?=? Fe2+?、?Cu2+?+? 2e-?=? Cu
56g? 2mol? 2mol? 64g
5.6g? 0.2mol?0.2mol? 6.4g
即铁片质量减少5.6g,铜片质量增加6.4g
(2)去掉导线,则发生反应
Fe+CuSO4=FeSO4+Cu?~e-?~△m↑
56g? 64? 2mol? 8g
0.2mol? 0.8g
即铁片增重0.8g。
本题难度:一般
4、选择题 下面能够构成原电池及电极反应式正确的是
A.Fe、Cu、浓硝酸溶液,负极反应式为:Fe-2e-==Fe2+
B.Al、Cu、稀硫酸,负极反应式为:Cu-2e-==Cu2+
C.Al、Mg、NaOH溶液,负极反应式为:Al+4OH--3e-==AlO2-+2H2O
D.Zn、Cu、乙醇,负极反应式为:Zn-2e-==Zn2+
参考答案:C
本题解析:A错,负极为Cu,因为Fe在浓硝酸溶液中会发生钝化,所以负极反应式为:Cu-2e-==Cu2+;B错,负极Al,反应式为AL-3e-==AL3+;C正确,Al与NaOH溶液能反应,Mg与NaOH溶液不反应,所以负极反应式为:Al+4OH--3e-==AlO2-+2H2O;D错,乙醇为非电解质,不能构成原电池;
本题难度:一般
5、选择题 观察下列几个装置示意图,有关叙述正确的是( )
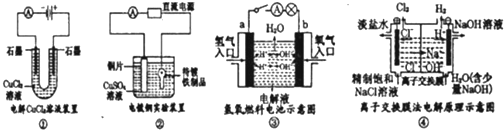
A.装置①中阳极上析出红色固体
B.装置②中铜片应与电源负极相连
C.装置③中外电路电流方向:b极→a极
D.装置④中阴极反应:2?Cl--2e-=Cl2
参考答案:A、电解氯化铜溶液时,阴极上铜离子得电子析出金属铜单质,故A错误;
B、电镀时,镀层应与电源正极相连,镀件与电源负极相连,所以铜做阳极,待镀铁制品应与电源负极相连,故B错误;
C、氢氧燃料电池中,负极上氢气失电子,正极上氧气得电子,所以装置③中闭合电键后外电路电子由a极流向b极,电路电流方向:b极→a极,故C正确;
D、所以装置④是电解池,阴极上氢离子得到电子生成氢气,故D错误;
故选C.
本题解析:
本题难度:简单