微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (14分) 研究NO2、SO2、CO等大气污染气体的处理具有重要意义。
(1)利用反应6NO2+8NH3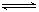 7N2+12H2O可处理NO2。当转移3.6mol电子时,生成的N2在标准状况下是?L。
7N2+12H2O可处理NO2。当转移3.6mol电子时,生成的N2在标准状况下是?L。
(2)已知:反应1:2SO2(g)+O2(g)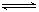 2SO3(g)? ΔH =" ―196.6" kJ・mol-1
2SO3(g)? ΔH =" ―196.6" kJ・mol-1
反应2:NO2(g)+SO2(g)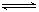 SO3(g)+NO(g)? ΔH = ―41.8kJ・mol-1
SO3(g)+NO(g)? ΔH = ―41.8kJ・mol-1
则反3:2NO(g)+O2(g)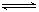 2NO2(g)的? ΔH =" _________" kJ・mol-1
2NO2(g)的? ΔH =" _________" kJ・mol-1
(3) 一定条件下,将2molNO与2molO2置于恒容密闭容器中发生上述反应3,下列各项能说明反应达到平衡状态的是?。
a.体系压强保持不变? b.混合气体颜色保持不变
c.NO和O2的物质的量之比保持不变? d.每消耗1 molO2同时生成2 molNO2
(4)CO可用于合成甲醇,一定温度下,向体积为2L的密闭容器中加入CO和H2,发生反应CO(g)+2H2(g) CH3OH(g),达平衡后测得各组分浓度如下:
CH3OH(g),达平衡后测得各组分浓度如下:
物质
| CO
| H2
| CH3OH
|
浓度(mol?L―1)
| 0.9
| 1.0
| 0.6
|
①混合气体的平均相对分子质量__________________________。
②列式并计算平衡常数K=__________________________。
③若将容器体积压缩为1L,不经计算,预测新平衡中c(H2)的取值范围是__________。
④若保持体积不变,再充入0.6molCO和0.4molCH3OH,此时v正___v逆(填“>”、“<”或“=”)。
参考答案:(14分)(1) 23.52(2分)? (2)-113(2分)? (3)abc(2分)
(4)①18.56(2分)?②0.6/(0.9×1.02)="2/3" L2? moL―2 (或0.67 L2? moL―2)?(2分)?
③1 mol?L―1<c(H2)<2 mol?L―1(2分)?④=(2分)
本题解析:(1)根据反应式可知,NO2是氧化剂,氮元素的化合价从+4价降低到0价,得到4个电子,则生成7mol氮气,转移24mol电子。因此当转移3.6mol电子时,生成的N2是7×3.6mol÷24=1.05mol,则在标准状况下的体积是1.05mol×22.4L/mol=23.52L。
(2)考查盖斯定律的应用。根据盖斯定律可知,①-②×2即得到反应2NO(g)+O2(g)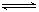 2NO2(g),所以该反应热△H=―196.6 kJ・mol-1+41.8kJ・mol-1×2=-113kJ/mol。
2NO2(g),所以该反应热△H=―196.6 kJ・mol-1+41.8kJ・mol-1×2=-113kJ/mol。
(3)在一定条件下,当可逆反应的正反应速率和逆反应速率相等时(但不为0),反应体系中各种物质的浓度或含量不再发生变化的状态,称为化学平衡状态。颜色深浅和浓度有关系,所以b正确。反应是体积减小的,所以压强也是减小的,则a可以说明;NO和O2的物质的量之比保持不变,即说明物质的含量不再发生变化,c正确;d中反应速率的方向是相同的,速率之比是相应的化学计量数之比,因此d中的关系始终是成立,不正确,答案选abc。
(4)①平衡时CO、氢气和甲醇的物质的量分别是1.8mol、2.0mol和1.2mol,所以混合气体的平均相对分子质量是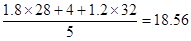 。
。
②平衡常数K=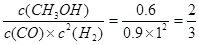
③正反应是体积减小的,所以增大压强,平衡向正反应方向进行,则根据勒夏特列原理可知,平衡时氢气的浓度一定是1 mol?L―1<c(H2)<2 mol?L―1。
④若保持体积不变,再充入0.6molCO和0.4molCH3OH,,则此时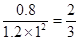 ,所以是平衡状态,则正反应速率等于逆反应速率。
,所以是平衡状态,则正反应速率等于逆反应速率。
本题难度:一般
2、简答题 由碳棒、铁片和200mL稀H2SO4组成的原电池中,当在碳棒上共放出3.36L(标准状况)气体时,消耗铁的物质的量为______,有______个电子通过了电线.
参考答案:该电池的电池反应式为:Fe+H2SO4=FeSO4+H2↑?转移电子
? 1mol? 22.4L? 2×6.02×10 23个
? 0.15mol? 3.36L? 1.806×1023?个
?所以消耗铁的物质的量为0.15mol;有1.806×1023?个电子通过导线.
故答案为:0.15mol;1.806×1023.
本题解析:
本题难度:一般
3、选择题 用Pt作电极电解一定浓度的下列水溶液,电解结束后,向剩余溶液中加少量水,能使溶液浓度和电解前相同的是( )
A.AgNO3
B.H2SO4
C.NaOH
D.NaCl
参考答案:A、电极硝酸银溶液电解的是硝酸银和水,电解结束后加水不能回复原溶液的浓度,故A错误;
B、电极硫酸溶液实质是电极水,电解结束后,向剩余溶液中加少量水,能使溶液浓度和电解前相同,故B正确;
C、电极氢氧化钠溶液实质是电极水,电解结束后,向剩余溶液中加少量水,能使溶液浓度和电解前相同,故C正确;
D、电解氯化钠实质是电极水和氯化钠,电解结束后,向剩余溶液中加少量水,不能使溶液浓度和电解前相同,故D错误;
故选BC.
本题解析:
本题难度:一般
4、填空题 (共8分)
(1)2.00g C2H2完全燃烧生成液态水和CO2,放出99.6kJ热量,请写出表示C2H2燃烧热的热化学方程式: ;
(2)C2H2可用于制作燃料电池,请写以KOH溶液为电解质溶液的乙炔燃料电池的负极反应式: ;
(3)用乙炔燃料电池电解AgNO3溶液,用石墨做电解池两极,请写出与电源负极相连的石墨电极的电极反应式: ;
(4)高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压。高铁电池的总反应为:3Zn + 2K2FeO4 + 8H2O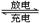 3Zn(OH)2 + 2Fe(OH)3 + 4KOH。请写出该电池在充电时阴极的电极反应式: ;
3Zn(OH)2 + 2Fe(OH)3 + 4KOH。请写出该电池在充电时阴极的电极反应式: ;
参考答案:(1)C2H2(g)+5/2 O2(g)=2CO2(g)+H2O(l) △H=-1294.8kJ/mol
(2) C2H2 +14OH―-10e-=2CO32-+8H2O (3)Ag++e-=Ag (4)Zn(OH)2+2e-=Zn+2OH-
本题解析:(1)燃烧热是在一定条件下,1mol可燃物完全燃烧生成稳定的氧化物时所放出的热量,2.00g C2H2完全燃烧生成液态水和CO2,放出99.6kJ热量,则1mol乙炔完全燃烧生成液态水和CO2,放出99.6kJ×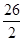 =1294.8kJ热量,因此热化学方程式为C2H2(g)+5/2 O2(g)=2CO2(g)+H2O(l) △H=-1294.8kJ/mol。
=1294.8kJ热量,因此热化学方程式为C2H2(g)+5/2 O2(g)=2CO2(g)+H2O(l) △H=-1294.8kJ/mol。
(2)原电池中负极失去电子,发生氧化反应,所以乙炔在负极通入,由于是氢氧化钾溶液则负极电极反应式为C2H2 +14OH―-10e-=2CO32-+8H2O。
(3)电解池中与电源负极相连的是阴极,溶液中的银离子放电,电极反应式为Ag++e-=Ag。
(4)充电相当于是电解池,阴极得到电子发生还原反应,根据总反应式可知充电时氢氧化锌在阴极失去电子,电极反应式为Zn(OH)2+2e-=Zn+2OH-。
考点:考查热化学方程式的书写以及电化学原理的应用
本题难度:困难
5、选择题 下列各组材料中,不能组成原电池的是
?
| A
| B
| C
| D
|
电极材料
| Zn片、石墨
| Cu片、Ag片
| Cu片、Zn片
| Fe片、Cu片
|
插入的溶液
| H2SO4溶液
| AgNO3溶液
| 蔗糖溶液
| 稀盐酸
参考答案:C
本题解析:构成原电池的条件是活泼性不同的金属或金属和非金属,导线相连并插入电解质溶液中。C中蔗糖不是电解质,不能构成原电池,所以答案选C。
本题难度:简单
|