微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 某研究小组将V1mL 1.0mol/L HCl溶液和V2mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如下图所示(实验中始终保持V1+V2=50mL)。回答下列问题
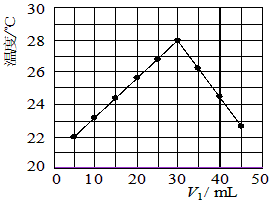
(1)研究小组做该实验时环境温度__________(填“高于”、“低于”或“等于”)22 ℃,判断的依据是____________________。
(2)由题干及图形可知,V1/V2=__________时,酸碱恰好完全中和,此反应所用NaOH溶液的浓度应为
__________mol/L。
(3)实验时将酸碱在简易量热计中混合,并用____________搅拌,使溶液混合均匀。经有关计算知此反应共放出Q kJ的热量,请写出此反应的热化学方程式:__________________ 。
2、简答题 (1)中和热测定的实验中,用到的玻璃仪器有烧杯、温度计、量筒、______.
(2)量取反应物时,取50mL?0.50mol?L-1的盐酸,还需加入的试剂是______(填序号).
A.50mL?0.50mol?L-1?NaOH溶液
B.50mL?0.55mol?L-1?NaOH溶液
C.1.0g?NaOH固体
(3)已知稀盐酸与稀氢氧化钠溶液反应的中和热△H=-57.3kJ?mol-1,请用离子方程式表示该中和反应的热化学方程式______.
3、简答题 用右图所示装置进行中和热测定实验,请回答问题:
(1)大小烧杯之间填满碎泡沫塑料的作用是______,从实验装置上看,图中缺少的一种玻璃仪器是______.
(2)使用补全仪器后的装置进行实验,取50mL0.25mol/LH2SO4溶液与50mL0.55mol/LNaOH溶液在小烧杯中进行中和反应,三次实验温度平均升高3.4℃.已知中和后生成的溶液的比热容为4.18J/(g-℃),溶液的密度均为1g/cm3.通过计算可得中和热△H=______,H2SO4与NaOH反应的热化学方程式为______.
(3)实验中若用60mL0.25mol-L-1H2SO4溶液跟50mL0.55mol-L-1NaOH溶液进行反应,与上述实验相比,所放出的热量______?(填“相等”、“不相等”),所求中和热______?(填“相等”、“不相等”);,若用50mL0.50mol-L-1醋酸代替H2SO4溶液进行上述实验,测得反应前后温度的变化值会______?(填“偏大”、“偏小”、“不受影响”).
4、实验题 50 mL1.0 mol・L-1盐酸跟50mL1.1 mol・L-1氢氧化钠溶液在下图装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。试回答下列问题。
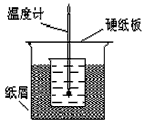
⑴大小烧杯间填满碎纸条的作用是什么?___________________________
⑵大烧杯上如不盖硬纸板,对求得中和热的数值有何影响? __________________________
⑶改用60 mL1.0mol・L-1盐酸跟50mL1.1mol・L-1氢氧化钠溶液进行反应,与上述实验相比,所测中和热的数值理论上是否相等(不考虑空气的影响)?简述理由。__________________________
⑷用相同浓度和体积的氨水代替NaOH溶液进行实验,为什么测得中和热的数值偏低?
_____________________________________________
5、选择题 关于中和热测定实验的下列说法不正确的是?
[? ]
A.烧杯间填满碎泡沫塑料是减少实验过程中的热量损失
B.使用环形玻璃棒既可以搅拌又避免损坏温度计
C.向盛装酸的烧杯中加碱时要小心缓慢
D.测了酸后的温度计要用水清洗后再测碱的温度