微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、简答题 A、B、C三种强电解质,它们溶于水在水中电离出的阳离子有K+、Ag+,阴离子有NO3-、OH-(电解质电离的离子有重复).
图1装置中,甲、乙、丙三个烧杯中依次盛放足量的A溶液、足量的B溶液、足量的C溶液,电极均为铂电极.接通电源,经过一段时间后,测得甲中b电极质量增加了43.2g.常温下各烧杯中溶液pH与电解时间t关系如图2.请回答下列问题:

(1)写出三种强电解质的化学式:A______;B______;C______.
(2)写出乙烧杯c电极发生的电极反应为______,甲烧杯中的总反应的化学方程式为______.
(3)计算丙烧杯e电极上生成的气体在标准状况下的体积为______,甲烧杯中溶液体积为400ml,pH=______.
(4)要使甲烧杯中的A溶液恢复到电解前的状态,需要加入的物质是______,其质量为______.
(5)若直流电源使用的是铅蓄电池,铅蓄电池的正极材料是PbO2,负极材料是Pb,电解质溶液时H2SO4,则放电时N级上发生的电极反应为______,M级附近溶液的pH______(选填“升高”或“降低”或“不变”).铅蓄电池充电时,若阳极和阴极之间用阳离子交换膜(只允许H+通过)隔开,则当外电路通过0.2mol电子时,由阳极室通过阳离子交换膜进入阴极室的阳离子有______mol.
2、选择题 锌溴液流电池是一种新型电化学储能装置(如右图所示),电解液为溴化锌水溶液,电解液在电解质储罐和电池间不断循环。下列说法不正确的是
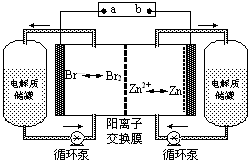
A.充电时电极a连接电源的负极
B.放电时负极的电极反应式为Zn―2e-=Zn2+
C.放电时左侧电解质储罐中的离子总浓度增大
D.阳离子交换膜可阻止Br2与Zn直接发生反应
3、填空题 (8分)某同学在用锌与稀硫酸反应制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气生成的速率。请回答下列问题:
(1)上述实验中,发生的化学反应方程式有______________________________
(2)硫酸铜溶液加快氢气生成的速率的原因______________________________
(3)实验室现有Na2SO4、MgSO4、HgSO4、K2SO4等四种溶液,可与上述实验中CuSO4溶液起相似作用的是____________________
(4)要加快上述实验中气体生成的速率,还可以采取的措施有____________
4、判断题 (6分)铅蓄电池是典型的可充型电池,它的正负极格板是惰性材料,电池总反应式为:
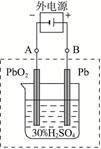
铅蓄电池示意图
Pb+PbO2+4H++2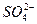
 2PbSO4+2H2O
2PbSO4+2H2O
请完成下列问题(不考虑氢、氧的氧化还原):
(1)放电时:正极的电极反应式是
____________________________________________________;电解液中H2SO4的浓度将变_________________;当外电路通过1 mol电子时,理论上负极板的质量增加
_________________g。
(2)在完全放电耗尽PbO2和Pb时,若按右图连接,电解一段时间后,则在A电极上生成
_____________________、B电极上生成_____________________,此时铅蓄电池的正负极的极性将__________________________________。
5、填空题 (10分)能源短缺是人类社会面临的重大问题。甲醇是一种可再生能源,具有广泛的开发和应用前景。
(1)工业上一般采用下列两种反应合成甲醇:
反应I:?CO(g)+2H2(g)? ?CH3OH(g)?ΔH1
?CH3OH(g)?ΔH1
反应II:CO2(g)+3H2(g) ? CH3OH(g)?+?H2O(g)?ΔH2
? CH3OH(g)?+?H2O(g)?ΔH2
①上述反应符合“原子经济”原则的是?(填“I”或“Ⅱ”)。
②下表所列数据是反应I在不同温度下的化学平衡常数(K)。
温度
| 250℃
| 300℃
| 350℃
|
K
| 2.041
| 0.270
| 0.012
|
由表中数据判断ΔH1?0(填“>”、“=”或“<”)。?
③某温度下,将2molCO和6molH2充入2L的密闭容器中,充分反应,达到平衡后,测得c(CO)=0.2mol/L,则CO的转化率为?。
(2)某实验小组依据甲醇燃烧的反应原理,设计如图所示的电池装置。
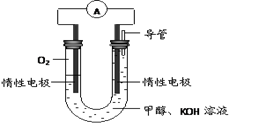
①?该电池正极的电极反应为?。
②工作一段时间后,测得溶液的pH减小,该电池总反应的离子方程式为?。