| �߿�ʡ������ | |
|
|
| �߿�ʡ������ | |
|
|
|
�߿���ѧ֪ʶ����������ѧ��Ӧ������������ǿ����ϰ��2017�����°棩(��)
�ο��𰸣�D ������������峣�����ȷ�Ӧ���ٿ�ȼ���ȼ�գ�������кͷ�Ӧ���۴�������Ϸ�Ӧ���ܽ���������û���Ӧ�������ȷ�Ӧ�ȣ��������ȷ�Ӧ���ٴ�����ֽⷴӦ�����ε�ˮ�⣻��Ba(OH)2��8H2O��NH4Cl��Ӧ����̼��ˮ������C��CO2�ķ�Ӧ��ѡD �����Ѷȣ�һ�� 2��ѡ���� �����Ȼ�ѧ����ʽ��д��˵����ȷ���� |
�ο��𰸣�D
���������A���Ȼ�ѧ����ʽ�У��ʱ�ĵ�λ��kJ��mol-1������B��ȼ������ָ1moL������ȫȼ�������ȶ��Ļ�����ʱ�ų���������̼���ȶ��������Ƕ�����̼������C���������������ᷴӦ����ˮ�⣬�������ᱵ���������ԣ��κ�ǿ���ǿ����кͷ�Ӧ����1mol H2O(l)�ķ�Ӧ�Ȳ�������-a kJ��mol-1������D����ȷ��ѡD��
���㣺�����Ȼ�ѧ����ʽ�����жϡ�
�����Ѷȣ�һ��
3��ѡ���� ��������ֻ�����Ӽ�����
A��H2O
B��Na2O
C��NaOH
D��HCl
�ο��𰸣�B
���������һ����õĽ���Ԫ������õķǽ���Ԫ���γ����Ӽ����ǽ���Ԫ��֮���γɹ��ۼ����Դ������A��H2O��ֻ��H��O֮���γɵĹ��ۼ�����A��ѡ��B���������к������ӡ��������γɵ����Ӽ�����Bѡ��C��NaOH�к������ӡ������������γɵ����Ӽ���H��O֮���γɵĹ��ۼ�����C��ѡ��D���Ȼ�����ֻ��H��Cl֮���γɵĹ��ۼ�����D��ѡ����ѡB��
�����Ѷȣ�һ��
4��ѡ���� �Ӻ�ˮ����ȡ�������·�Ӧ��5NaBr+NaBrO3+3H2SO4�T3Br2+3Na2SO4+3H2O����÷�Ӧ��������ԭ��Ӧԭ���������Ƶ���
A.2NaBr+Cl2�T2NaCl+Br2
B.C+CO22CO
C.2H2S+SO2�T2H2O+3S��
D.AlCl3+3NaAlO2+6H2O�T4Al��OH��3��+3NaCl
�ο��𰸣�BC
���������������NaBr�е���Ԫ�ػ��ϼ�Ϊ-1�ۣ�NaBrO3����Ԫ�صĻ��ϼ�Ϊ+5�ۣ����������0�۵��嵥�ʣ�����������ԭ��Ӧ�еĹ��з�Ӧ���ͣ�
���A�����ϼ۱仯�ķֱ�����Ԫ�غ���Ԫ�أ����ǹ��з�Ӧ���ͣ���A����
B�����ϼ۱仯����̼Ԫ�أ�һ������0�����ߵ�+2�ۣ�һ������ +4�۽���+2�ۣ��ǹ��з�Ӧ���ͣ���B��ȷ��
C����Ԫ�صĻ��ϼ۴�-2������0�ۣ����еĴ�+4�۽���0�ۣ�����������ԭ��Ӧ�еĹ��з�Ӧ���ͣ���C��ȷ��
D����Ӧ��û��Ԫ�ػ��ϼ۵ı仯������������ԭ��Ӧ����D����
��ѡBC��
���������⿼��ѧ�������ͽ�����������������ѧ��������ԭ��Ӧ֪ʶ����ȷԪ�ػ��ϼ��ǽⱾ��ؼ����ѶȲ���
�����Ѷȣ���
5������� ��10�֣�ú��������úΪԭ�ϣ�������ѧ�ӹ�ʹúת��Ϊ���塢Һ�塢����ȼ���Լ����ֻ�����Ʒ�Ĺ�ҵ���̡�
��1����ˮ����ͨ�����ȵ�̼���ɲ���ˮú������ӦΪ��
C(s)��H2O(g) 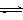 CO(g)��H2(g) ��H=��131.3 kJ?mol-1����S=��133.7J?(K?mol) -1
CO(g)��H2(g) ��H=��131.3 kJ?mol-1����S=��133.7J?(K?mol) -1
�ٸ÷�Ӧ�ܷ��Է�������__________�йأ�
��һ���¶��£���һ���ݻ��ɱ���ܱ������У�����������Ӧ���������жϸ÷�Ӧ�ﵽ��ѧƽ��״̬����__________������ĸ����ͬ����
a�������е�ѹǿ���� b��1 mol H��H�����ѵ�ͬʱ����2 molH��O��
c��v��(CO) = v��(H2O) d��c(CO)=c(H2)
��2������ͬ����CO(g)��H2O(g)�ֱ�ͨ�뵽���Ϊ2L�ĺ����ܱ������У����з�Ӧ 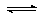 CO(g)��H2O(g) CO2(g)��H2(g)���õ������������ݣ�
CO(g)��H2O(g) CO2(g)��H2(g)���õ������������ݣ�
| ʵ���� | �¶�/�� | ��ʼ��/mol | ƽ����/mol | �ﵽƽ���� ��ʱ��/min | ||
| H2O | CO | H2 | CO | |||
| 1 | 650 | 2 | 4 | 1.6 | 2.4 | 5 |
| 2 | 900 | 1 | 2 | 0.4 | 1.6 | 3 |
| 3 | 900 | a | b | c | d | t |
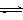 CH3OH(g)��H2O(g) ������ͼ��ʾ�÷�Ӧ���й���������(��λΪkJ?mol-1)�ı仯�������Ϊ1 L�ĺ����ܱ������У�����1mol CO2��3mol H2�����д�ʩ����ʹc (CH3OH)�������___________��
CH3OH(g)��H2O(g) ������ͼ��ʾ�÷�Ӧ���й���������(��λΪkJ?mol-1)�ı仯�������Ϊ1 L�ĺ����ܱ������У�����1mol CO2��3mol H2�����д�ʩ����ʹc (CH3OH)�������___________��
�ο��𰸣�(1)���¶ȣ�2�֣� ��bc��2�֣�
(2)�� 0.16mol��L-1��min-1 ��2�֣� ������2�֣�
(3)cd��2�֣�
�����������
�����Ѷȣ�����
| ���� �� С������ӡ�� �������� ���ر��� �����ض����� | |
| ��һƪ���߿���ѧ���⡶Ӱ�컯ѧ��Ӧ����.. | |
| �����Ŀ |