微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 15分)某兴趣小组同学设计了如下装置(其中夹持仪器、加热仪器及冷却水管没有画出),用加热苯甲酸、浓H2SO4和乙醇混合物的方法来制备苯甲酸乙酯,并检验反应的部分副产物。且苯甲酸乙酯的沸点为213℃,乙醚的沸点为34.6℃。

⑴关闭活塞a、接通竖直冷凝管的冷凝水,给A加热30分钟,制备。仪器E的作用是?。
⑵上述反应的副产物可能有:乙醚(CH3CH2-O-CH2CH3)、乙烯、SO2、水等。
①打开活塞a,在竖直冷凝管上方塞上塞子,通过B、C、D装置检验SO2和乙烯。已知C中盛放的试剂是NaOH溶液,B、D中应盛放的试剂依次分别是?。
②有同学拟通过红外光谱仪鉴定所得产物中是否含有“-CH2CH3”,来确定副产物中存在乙醚。请你对该同学的观点进行评价:?。
⑶通过下列实验方案,可以提纯苯甲酸乙酯。
①为除去产品中杂质,先将三口烧瓶中残液倒入盛有冷水的烧杯中,并加入?。
②用分液法可分离上述有机层和水层,分液完成后,取出有机层的操作是?。
③向锥形瓶中加入适量豆粒大小的无水氯化钙干燥剂,至醚层澄清透明;过滤得醚层,然后将醚层加入到干燥的蒸馏烧瓶中蒸馏,蒸馏过程中控制的温度为?。
2、实验题 (14分)某化学兴趣探究小组将一批废弃的线路板简单处理后,得到含Cu(70%)、Al(25%)、Fe(4%)及少量Au、Pt等金属的混合物,并设计出如下制备硫酸铜和硫酸铝晶体的路线:
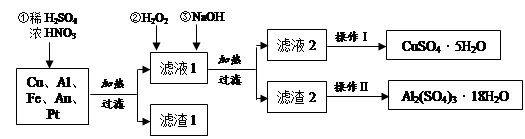
(1)在金属混合物与酸的反应中,表现氧化性的离子为?;得到滤渣1的主要成分为?。
(2)第②步加H2O2后发生反应的离子方程式为?;
通过加入NaOH调节溶液的pH,其目的是?;
(3)操作Ⅰ中包括的实验步骤有?、过滤;
(4)通过操作Ⅱ可以由滤渣2制取Al2(SO4)3・18H2O 。下列是操作Ⅱ的一种实验方案。

实验中:试剂1是?,试剂2是?。(填化学式)
3、实验题 (12分)某化学兴趣小组用如下图1所示装置进行探究实验,以验证产物中有乙烯生成且乙烯具有不饱和性。当温度迅速上升后,可观察到试管中溴水褪色,烧瓶中浓H2SO4与乙醇的混合液体变为棕黑色。
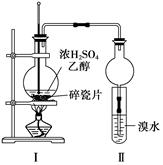

图1?图2
(1)写出该实验中生成乙烯的化学方程式?。
(2)甲同学认为:考虑到该混合液体反应的复杂性,溴水褪色的现象不能证明反应中有乙烯生成且乙烯具有不饱和性,其理由正确的是?。
a.乙烯与溴水易发生取代反应
b.使溴水褪色的反应,未必是加成反应
c.使溴水褪色的物质,未必是乙烯
(3)乙同学经过细致观察后试管中另一现象后并借用pH试纸测定,证明反应中有乙烯生成,请简述
?。
(4)丙同学对上述实验装置进行了改进,在Ⅰ和Ⅱ之间增加上图2装置以除去乙醇蒸气和SO2,则A中的试剂是?,B中的试剂为?。
(5)处理上述实验后烧瓶中废液的正确方法是?。
a.冷却后倒入下水道中 ?b.冷却后倒入空废液缸中 c.冷却后加水稀释,倒入废液缸中,加废碱中和
4、填空题 (14分)某学生实验小组拟用孔雀石(主要成分是Cu(OH)2・CuC03,其杂质主要为FeC03等)制胆矾,实验设计流程如下:

回答下列问题:
(1)步骤(a)中,实验研磨孔雀石的仪器名称?;用硫酸浸取的化学方程式:?
(2)步骤(b)中,pH控制在3.O~3.5,其目的是?;加过氧化氢发生反应的离子方程式为?。
(3)怎样判断蒸发浓缩已完成:?。
(4)将制得的样品用热重仪进行热重分析,热重仪原理及热重记录如下表:
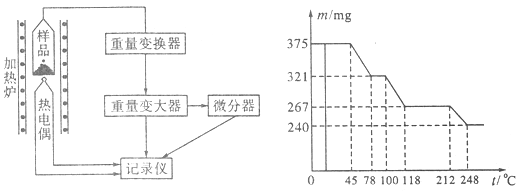
写出212~248℃温度范围内发生反应的化学方程式?。
(5) FeC03为白色沉淀,此沉淀的Ksp(FeC03)=2×10-11,将FeCl2的稀溶液与Na2CO3溶液等体积混合,若FeCl2的浓度为2×lO一5mol・L-1.则生成沉淀所需Na2CO3溶液的最小浓度为?mol・L-1。
5、填空题 水处理技术在生产、生活中应用广泛。
(1)含有较多?离子的水称为硬水。硬水加热后产生碳酸盐沉淀的离子方程式
为?(写出一个即可)。
(2)将RH型阳离子交换树脂和ROH型阴离子交换树脂串接来软化天然硬水,应先使硬水通过
?(填“RH”或“ROH”)型离子交换树脂,原因是?。
(3)通过施加一定压力使水分子通过半透膜而将大分子或离子截留,从而获得纯净水的方法称为?。电渗析法净化水时,使离子通过半透膜的推动力是?。
(4)检验蒸馏水的纯度时,最简单易行的方法是测定水的?。