微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (20分)聚合氯化铝是一种新型、高效絮凝剂和净水剂,其单体是液态的碱式氯化铝[Al2(OH)nCl6-n]。本实验采用铝盐溶液水解絮凝法制备碱式氯化铝。其制备原料为分布广、价格廉的高岭土,化学组成为:Al2O3(25%~34%)、SiO2(40%~50%)、Fe2O3(0.5%~3.0%)以及少量杂质和水分。已知氧化铝有多种不同的结构,化学性质也有差异,且一定条件下可相互转化;高岭土中的氧化铝难溶于酸。制备碱式氯化铝的实验流程如下:

已知:Fe3+、Al3+以氢氧化物形式完全沉淀时,溶液的pH分别为3.2、5.2。
根据流程图回答下列问题:
(1)“煅烧”的目的是_______________________________________________。
(2)“浸出”过程中发生反应的离子方程式为_______________________________。
(3)“浸出”选用的酸为_______。配制质量分数15%的A酸需要200mL30%的A酸(密度约为1.15g/cm3)和_______g蒸馏水,配制用到的仪器有烧杯、玻璃棒、______________。
(4)为提高铝的浸出率,可采取的措施有?_______________(要求写出三条)。
(5)“调节溶液pH在4.2~4.5”的过程中,除添加必要的试剂,还需借助的实验用品是_________________;“蒸发浓缩”需保持温度在90~100℃,控制温度的实验方法是___________?______。
(6)实验中制备碱式氯化铝反应的化学方程式为_________________
参考答案:(1)改变高岭土中氧化铝的结构,使其能溶于酸。
(2)Al2O3+6H+ ="=" 2Al3++3H2O? Fe2O3+6H+ ="=" 2Fe3++3H2O
(3)盐酸? 230?量筒
(4)加热或提高反应温度,将煅烧后的块状固体粉碎,适当增大盐酸浓度,充分搅拌,延长反应时间(任答3条)
(5)pH计(或精密pH试纸)?水浴加热?
(6)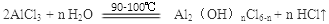
本题解析:“煅烧”的目的是改变高岭土中氧化铝的结构,使其能溶于酸。“浸出”过程中发生反应与酸反应。该酸要溶液挥发,不会形成杂质。为提高铝的浸出率,可采取的措施有加热或提高反应温度,将煅烧后的块状固体粉碎,适当增大盐酸浓度,充分搅拌,延长反应时间。控制温度的实验方法是水浴加热?。
本题难度:一般
2、选择题 某化学式趣小组设计了下列四个实验装置,试图在短时间内通过观察实验现象说明CO2与NaOH溶液发生了反应。其中无法达到实验目的的是
参考答案:D
本题解析:略
本题难度:一般
3、实验题 实验室常利用甲醛法测定(NH4)2SO4样品中氮的质量分数,其反应原理为:4NH4++6HCHO===3H++6H2O+(CH2)6N4H+[滴定时,1mol(CH2)6N4H+与1molH+相当],然后用NaOH标准溶液滴定反应生成的酸。某兴趣小组用甲醛法进行了如下实验:
步骤Ⅰ 称取样品1.500g。
步骤Ⅱ 将样品溶解后,完全转移到250mL容量瓶中,定容,充分摇匀。
步骤Ⅲ 移取25.00mL样品溶液于250mL锥形瓶中,加入10mL20%的中性甲醛溶液,摇匀、静置5min后,加入1~2滴酚酞试液,用NaOH标准溶液滴定至终点。按上述操作方法再重复2次。
(1)根据步骤Ⅲ填空:
①碱式滴定管用蒸馏水洗涤后,直接加入NaOH标准溶液进行滴定,则测得样品中氮的质量分数??(填“偏高”、“偏低”或“无影响”)。
②锥形瓶用蒸馏水洗涤后,水未倒尽,则滴定时用去NaOH标准溶液的体积??(填“偏大”、“偏小”或“无影响”)。
③滴定时边滴边摇动锥形瓶,眼睛应观察?。
A.滴定管内液面的变化
B.锥形瓶内溶液颜色的变化
④滴定达到终点的判断是?。
(2)滴定结果如下表所示:
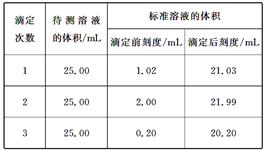
若NaOH标准溶液的浓度为0.1010mol/L,则该样品中氮的质量分数为?。
参考答案:(1)①偏高 ②无影响 ③B ④当加入最后一滴,溶液有无色变成粉红(或浅红)色,且30s不变色 (2)18.85%
本题解析:(1)碱式滴定管如果没有用标准液润洗,则氢氧化钠溶液的浓度将变小。则消耗氢氧化钠溶液的体积偏大,测定结果偏高;锥形瓶只能用蒸馏水润洗,所以不影响;滴定时边滴边摇动锥形瓶,眼睛应观察锥形瓶内溶液颜色的变化,答案选B;滴定达到终点的判断是当加入最后一滴,溶液有无色变成粉红(或浅红)色,且30s不变色。
(2)三次实验中消耗的氢氧化钠溶液的体积分别是20.01ml、19.99ml、20.00ml,所以三次的平均值为20.00ml,所以25.00mL溶液中氢离子的物质的量为0.02L×0.1010mol/L=0.00202mol。则原溶液中氢离子的物质的量为0.00202mol×10=0.0202mol,所以NH的物质的量也是0.0202mol。因此该样品中氮的质量分数为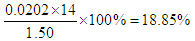 。
。
本题难度:一般
4、实验题 某化学小组拟采用如下装置(夹持和加热仪器已略去)来电解饱和食盐水,并用电解产生的H2还原CuO粉末来测定Cu的相对原子质量,同时检验氯气的氧化性。
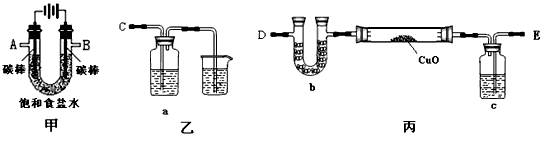
(1)为完成上述实验,正确的连接顺序为A连_______;B连_______(填写连接的字母)。
(2)对硬质玻璃管里的氧化铜粉末加热前,需要的操作为__________________。
(3)若检验氯气的氧化性,则乙装置的a瓶中溶液可以是________________,对应的现象为_______________________。
(4)丙装置的c瓶中盛放的试剂为_______________,作用是_______________________。
(5)为测定Cu的相对原子质量,设计了如下甲、乙两个实验方案精确测量硬质玻璃管的质量为ag, 放入CuO后,精确测量硬质玻璃管和CuO的总质量为bg, 实验完毕后
甲方案:通过精确测量硬质玻璃管和Cu粉的总质量为cg, 进而确定Cu的相对原子质量。
乙方案:通过精确测定生成水的质量dg,进而确定Cu的相对原子质量。
①请你分析并回答:________方案测得结果更准确。你认为不合理的方案的不足之处在__________________________________。
②若按甲方案测定的数据计算,Cu的相对原子质量______________________。
参考答案:(1)E;C
(2)检验氢气的纯度,防止发生爆炸
(3)淀粉KI溶液;溶液变为蓝色
(4)浓硫酸;吸收H2中的H2O,防止硬质玻璃管炸裂
(5)①甲;空气中的CO2和H2O通过D口进入U形管造成实验误差较大;②16(c-a)/(b-c)
本题解析:
本题难度:困难
5、选择题 下列相关实验不能达到预期目的的是
?
| 相关实验
| 预期目的
|
A.
相同温度下,等质量的大理石块、大理石粉分别与等体积、等浓度的盐酸反应
探究接触面积对化学反应速率的影响
B.
把装有颜色相同的NO2和N2O4混合气的两支试管(密封)分别浸入冷水和热水中
探究温度对化学平衡的影响
C.
在蔗糖中加入稀硫酸,水浴加热,再加入新制的氢氧化铜并加热
探究蔗糖水解产物具有还原性
D.
两支试管中装有等体积、等浓度H2O2溶液,向其中一支试管中加入FeCl3溶液
探究FeCl3溶液对H2O2分解速率的影响
|
题型:单选题难度:中档来源:不详 答案 蔗糖在稀H2SO4溶液水解后应加入NaOH溶液中和掉H2SO4使溶液呈碱性,否则加入新制Cu(OH)2并加热时,得不到Cu2O沉淀,也无法探究蔗糖水解产物具有还原性。
马上分享给同学