微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 可逆反应:2HI(g)?H2(g)+I2(g);△H>0.在密闭容器中进行,当达到平衡时欲使混合气体的颜色加深,应采取的措施( )
A.减小容器体积
B.降低温度
C.加入催化剂
D.充入H2气体
2、选择题 在某温度下反应ClF(气)+F2(气)?
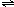
ClF3(气)+268千焦在密闭容器中达到平衡.下列说法正确的是( )
A.温度不变,缩小体积,ClF的转化率增大
B.温度不变,增大体积,ClF3的产率提高
C.升高温度,增大体积,有利于平衡向正反应方向移动
D.降低温度,体积不变,F2的转化率降低
3、选择题 可逆反应N2(g)+3H2(g)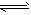 2NH3(g) △H=-QKJ/mol(Q>0)。有甲、乙两个容积相同且不变的密闭容器,向甲容器中加入1molN2和3molH2,在一定条件下达到平衡时放出热量为Q1KJ;在相同条件下,向乙容器中加入2molNH3达到平衡后吸收热量为Q2KJ,已知Q1=4Q2。下列叙述不正确的是
2NH3(g) △H=-QKJ/mol(Q>0)。有甲、乙两个容积相同且不变的密闭容器,向甲容器中加入1molN2和3molH2,在一定条件下达到平衡时放出热量为Q1KJ;在相同条件下,向乙容器中加入2molNH3达到平衡后吸收热量为Q2KJ,已知Q1=4Q2。下列叙述不正确的是
[? ]
A.达A到平衡时,甲容器中反应物的转化率与乙容器相等
B.达到平衡时,甲中NH3的体积分数与乙相等
C.达到平衡后,再向乙中加入0.2moLN2、0.6molH2、1.6molNH3,平衡向生成NH3的方向移动
D.乙中的热化学反应方程式为2NH3(g) N2(g)+3H2(g);△H=+QKJ/mol(Q>Q2>0)
N2(g)+3H2(g);△H=+QKJ/mol(Q>Q2>0)
4、填空题 80℃时,将0.40mol的N2O4气体充入2L已经抽空的固定容积的密闭容器中,发生如下反应:
N2O4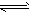 2NO2,隔一段时间对该容器内的物质进行分析,得到如下数据
2NO2,隔一段时间对该容器内的物质进行分析,得到如下数据
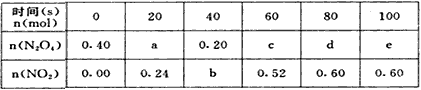
(1)计算20s-40s内用N2O4表示的平均反应速率为_______mol/L.
(2)计算在80℃时该反应的平衡常数K=_______;
(3)反应进行至100s后将反应混合物的温度降低,混合气体的颜色_______(填“变浅”、“变深”或“不变”) ;
(4)要增大该反应的K值,可采取的措施有(填序号)______________
A.增大N2O4的起始浓度
B.向混合气体中通入NO2
C.使用高效催化剂
D.升高温度
(5)如图是80℃时容器中N2O4物质的量的变化曲线,请在该图中补画出该反应在60℃时N2O4物质的量的变化曲线。
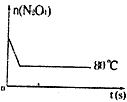
5、选择题 在如图所示的三个容积相同的容器①②③中进行如下反应:3A(g)+B(g) 2C(g),ΔH<0若起始温度相同,分别向三个容器中通入3molA和1molB,则达到平衡时各容器中C物质的体积分数由大到小的顺序为
2C(g),ΔH<0若起始温度相同,分别向三个容器中通入3molA和1molB,则达到平衡时各容器中C物质的体积分数由大到小的顺序为

[? ]
A.③②①
B.③①②
C.①②③
D.②①③