��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��Ӧ��
PCl5(g)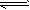 PCl3(g)��Cl2(g)��
PCl3(g)��Cl2(g)��
2HI(g)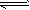 H2(g)��I2(g)��
H2(g)��I2(g)��
2NO2(g) N2O4(g)��
N2O4(g)��
��һ�������£��ﵽ��ѧƽ��ʱ����Ӧ���ת���ʾ���a%�������ָ���Ӧ���¶Ⱥ���������������ı䣬�ֱ��ټ���һ�����ĸ��Եķ�Ӧ���ת����
[? ]
A��������
B�������ڲ��䣬�ۼ���
C��������
D���ټ��٣��ڲ��䣬������
�ο��𰸣�D
���������
�����Ѷȣ�һ��
2��ѡ���� ������������ƽ���ƶ�ԭ�����͵��ǣ�������
A���ϳɰ������в��ýϸߵ�ѹǿ
B�����Ṥҵ�����У�O2��SO2���ʵ����ı�ֵ����1�s2
C����ʢ��NO2��N2O4�������IJ����������ˮ�У�������ɫ����
D��������ʳƷ�ױ���
�ο��𰸣�A���ϳɰ���ҵ��N2+3H2?2NH3 ��H��0������Ӧ�����������С��Ӧ������ѹǿƽ��������Ӧ�����ƶ����ʲ��ýϸߵ�ѹǿ�����ڰ��ĺϳɣ�����ƽ���ƶ�ԭ�����ͣ���A��ѡ��
B�����Ṥҵ��O2+2SO2?2SO2������������Ũ�ȣ�ƽ��������Ӧ�����ƶ�����������߶�������������ʣ�����ƽ���ƶ�ԭ�����ͣ���B��ѡ��
C������ƽ��2NO2?N2O4��������Ӧ�Ƿ��ȷ�Ӧ�������¶ȣ�ƽ�����淴Ӧ�����ƶ�������������ɫ���������ƽ���ƶ�ԭ�������ͣ���C��ѡ��
D�������·�Ӧ���ʼӿ죬ʳƷ�ױ��ʣ���ƽ���ƶ��أ�������ƽ���ƶ�ԭ�����ͣ���Dѡ��
��ѡD��
���������
�����Ѷȣ�һ��
3������� ��1�����Ҷ�������ʯ���γɹ����а������з�Ӧ��
CaCO3��s��+H2O��l��+CO2��g��?Ca2+��aq��+2HCO3-��aq����H=-321.7kJ/mol
��д���÷�Ӧ��ƽ�ⳣ������ʽ��K=______
��Ca��HCO3��2?��Һ�е�?c��OH-��?��c��H+����c��H2CO3����c��CO32-��֮��Ĺ�ϵΪ��c��OH-��=______
��2��������ɺ�����������Ҫ�ɷֶ���̼��ƣ������˵ġ�ɺ����������ʯ�ࣨCaSO4?2H2O���Ƴɵģ������һ����ʵ�鷽���������ɺ������______��
��3����¯ˮ���к��е�CaSO4��������̼������Һ������ʹ֮ת��Ϊ���ɡ�������������ʣ���ת�������ӷ���ʽ��______��
�ο��𰸣���1����CaCO3��s��+H2O��l��+CO2��g��?Ca2+��aq��+2HCO3-��aq��ƽ�ⳣ��k=c(Ca2+)��c2(HCO3-)c(H2O)��c(CO2)��
�ʴ�Ϊ��c(Ca2+)��c2(HCO3-)c(H2O)��c(CO2)��
����Һ�д���H2O?H++OH-��HCO3-?H++CO32-��HCO3-+H2O?OH-+HCO3-����Һ��������Դ��ˮ�ĵ��룬��̼�������ˮ�⣬ˮ�����������Ũ��Ϊc��H+��-c��CO32-����̼�����ˮ��õ�������Ũ�ȵ���̼���Ũ�ȣ�����Һ��c��OH-��=c��H+��+c��H2CO3��-c��CO32-����
�ʴ�Ϊ��c��OH-��=c��H+��+c��H2CO3��-c��CO32-����
��2��ͨ�������Ƿ���̼��������м��𣬾��������ȡ��������ɺ�������Թ��У���������ϡ���ᣬ���ų�������ʹ����ʯ��ˮ����ǵ���ɫ���壬ɺ����Ϊ�棬����Ϊ�٣�
�ʴ�Ϊ��ȡ��������ɺ�������Թ��У���������ϡ���ᣬ���ų�������ʹ����ʯ��ˮ����ǵ���ɫ���壬ɺ����Ϊ�棬����Ϊ�٣�
��3��ˮ���к��е�CaSO4������̼������Һ������ת��Ϊ?CaCO3��ת�������ӷ���ʽ��CaSO4��s��+CO32-?��aq��?CaCO3��s?��+SO42-?��aq����
�ʴ�Ϊ��CaSO4��s��+CO32-?��aq��?CaCO3��s?��+SO42-?��aq����
���������
�����Ѷȣ�һ��
4������� t��ʱ����3mol A��1molB����ͨ�����Ϊ2L���ܱ������У��ݻ����䣩���������·�Ӧ��
3A��g�� + B(g)  xC(g)2minʱ��Ӧ�ﵽƽ��״̬���¶Ȳ��䣩��ʣ����0.8molB,�����C��Ũ��Ϊ0.4mol/L,����д���пհ�:
xC(g)2minʱ��Ӧ�ﵽƽ��״̬���¶Ȳ��䣩��ʣ����0.8molB,�����C��Ũ��Ϊ0.4mol/L,����д���пհ�:
(1)�ӿ�ʼ��Ӧ���ﵽƽ���״̬,����Cƽ����Ӧ����Ϊ .
(2)x= ;ƽ�ⳣ��K= .
(3)��������ԭ������������ͨ����������(�躤����A��B��C������Ӧ)��ѧƽ�⣨����ĸ�� ��A��������Ӧ�����ƶ� B�����淴Ӧ�����ƶ� C��ƽ�ⲻ�ƶ�
��4������ԭƽ��������������ٳ���amolC����t��ʱ�ﵽ��ƽ�⣬��ʱB�����ʵ���Ϊ
n��B��= mol��
��5�����������Ӧ����ͬ�¶Ⱥ������н��У���ʹ��Ӧ�ﵽC�����ʵ���������ԭƽ����ȣ���ʼ������������ʵ����ʵ���n��A����n��B����n��C��֮��Ӧ������Ĺ�ϵʽΪ�� ��
�ο��𰸣�(1)0.2mol/(L��min) (2) 4 1/27(��0.037) (3)C (4)0.8 + 0.2a (5)n(A)/n(B) ��3/1,n(C)��0
�����������1��C��Ũ��Ϊ0.4mol/L��������C�ķ�Ӧ������0.4mol/L��2min��0.2mol/(L��min)��
��2������B�����ʵ�����0.2mol����Ũ����0.1mol/L�������Ũ�ȵı仯��֮������Ӧ�Ļ�ѧ������֮�ȿ�֪��x��4��ƽ��ʱʣ��A�����ʵ�����3mol��0.6mol��2.4mol����Ũ����1.2mol/L������ƽ�ⳣ��K��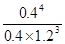 ��
��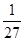 ��
��
��3�����������뷴Ӧ������ƽ�ⲻ�ƶ�����ѡC��
��4�����ڷ�Ӧǰ��������䣬����ԭƽ��������������ٳ���amolC����ƽ���ǵ�Ч�ģ�������t��ʱ�ﵽ��ƽ�⣬��ʱB�����ʵ���Ϊ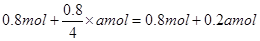 ��
��
��5�����ڷ�Ӧǰ��������䣬���Чƽ��������ǵ�Чת����ֻҪ��Ӧ�������������ʵ����ı�����ԭƽ����ʼ̬��ͬ����ƽ���Ч�������������ʵ����ʵ���n��A����n��B����n��C��֮��Ӧ������Ĺ�ϵʽΪn(A)/n(B) ��3/1��n(C)��0��
���㣺���鷴Ӧ���ʡ�ƽ�ⳣ�����㣬���������ƽ��״̬��Ӱ���Լ���Чƽ����й��ж�
�������������е��Ѷȵ����⣬�����ۺ���ǿ����ѧ����˼ά��������˸��ߵ�Ҫ�������ڲ��ض�ѧ������֪ʶ���̺�ѵ����ͬʱ�����ض�ѧ�������������ͽ��ⷽ����ָ����ѵ��������Ĺؼ�����ȷƽ�ⳣ���͵�Чƽ��ĺ����Լ�Ӱ�����أ�Ȼ�����ݷ���ʽ������ü��ɡ�����������ѧ�������������������ѧ�����������ɡ��ܽ������������
�����Ѷȣ�����
5������� ����2a mol��P��Q��R��S��һ�ܱ������л�ϣ��������·�Ӧ��xP��yQ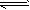 zR��wS���ﵽƽ����n(P)��a mol��n(Q)��
zR��wS���ﵽƽ����n(P)��a mol��n(Q)��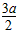 mol��n(R)��
mol��n(R)�� mol��n(S)��3a mol����֪����������ֻ��R�ǹ��塣
mol��n(S)��3a mol����֪����������ֻ��R�ǹ��塣
(1)���÷�Ӧ�����ʵĻ�ѧ������x��2����z��________��w��________��
(2)�ﵽƽ��ʱ��P��ת������____________��
(3)���ֻ�ı�ѹǿ����ѧ��Ӧ���ʷ����仯������ѧƽ�ⲻ�ƶ�����÷�Ӧ�и����ʵľۼ�״̬�ֱ��ǣ�Q____________��S____________��
(4)���ֻ�����¶ȣ���Ӧһ��ʱ������ʵ����ʵ�������Ϊ2a mol����÷�Ӧ������ӦΪ________�ȷ�Ӧ��
�ο��𰸣�(1)3��2��
(2)50% ��
(3)Һ̬����̬��
(4)��
���������
�����Ѷȣ�һ��