微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (共8分)在恒温恒容的密闭容器中通入1mol N2和Xmol H2发生如下反应:N2+3H2 2NH3。达到平衡后,测得反应放出的热量为18.4kJ,混合气体的物质的量为3.6mol,容器内的压强变为原来的90%。
2NH3。达到平衡后,测得反应放出的热量为18.4kJ,混合气体的物质的量为3.6mol,容器内的压强变为原来的90%。
(1)起始时充入H2的物质的量为 mol,氢气的转化率为 ;
(2)该反应的热化学方程式为 ;
(3)若起始时加入N2、H2、NH3的物质的量分别为a、b、c,达到平衡时各组分物质的量与上述平衡相同。若维持反应向正方向进行,则起始时c的取值范围是 。
2、选择题 对于可逆反应mA(g)+nB(g) pC(g)+gD(g),若其它条件都不变,只是在反应前是否加入催化剂,可得到两种υ~t图象如下图:
pC(g)+gD(g),若其它条件都不变,只是在反应前是否加入催化剂,可得到两种υ~t图象如下图:
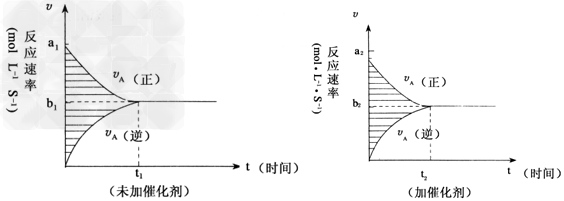
如下关系正确的为
[? ]
①a1=a2 ②a1<a2 ③b1=b2 ④b1<b2 ⑤t1>t2 ⑥t1=t2 ⑦两图中阴影部分面积相等 ⑧下图阴影部分面积更大
A.②④⑤⑦?
B.②④⑥⑧
C.②③⑤⑦?
D.②③⑥⑤
3、选择题 反应X(g)+3Y(g)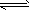 2Z(g);ΔH<0,在不同温度、不同压强(P1>P2)下,达到平衡时,混合气体中Z的体积分数φ(Z)随温度变化的曲线应为
2Z(g);ΔH<0,在不同温度、不同压强(P1>P2)下,达到平衡时,混合气体中Z的体积分数φ(Z)随温度变化的曲线应为
[? ]
A.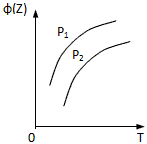
B.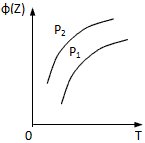
C.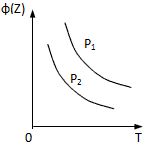
D.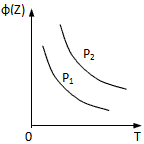
4、填空题 四川有丰富的天然气资源。以天然气为原料合成尿素的主要步骤如下图所示(图中某些转化步骤及生成物未列出):
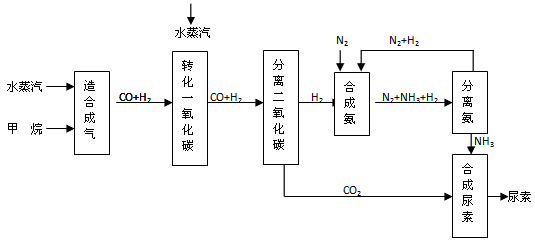
请填写下列空白:
(1)已知0.5 mol甲烷与0.5 mol水蒸汽在t℃、pkPa时,完全反应生成一氧化碳和氢气(合成气),吸收了a kJ热量,该反应的热化学方程式是:_________________ 。
(2)在合成氨的实际生产过程中,常采取的措施之一是:将生成的氨从混合气体中及时分离出来,并将分离出氨后的氮气和氢气循环利用,同时补充氮气和氢气。请运用化学反应速率和化学平衡的观点说明采取该措施的理由:___________________。
(3)当甲烷合成氨气的转化率为75%时,5.60×107L甲烷为原料能够合成 ____________L氨气。(假设体积在标准状况下测定)
(4)已知尿素的结构简式为H2N-C-NH2,请写出两种含有碳氧双键的尿素的同分异构体的结构简式: ①___________ ;②__________________ 。
5、填空题 (4分)一定条件下的可逆反应2NO2 (g)  N2O4 (g) △H=" -92.4kJ/mol " 达到化学平衡状态且其它条件不变时,
N2O4 (g) △H=" -92.4kJ/mol " 达到化学平衡状态且其它条件不变时,
(1)如果升高温度,平衡混合物的颜色 ;(变深、变浅)
(2)如果在体积固定的容器中加入一定量的二氧化氮,化学平衡向 方向移动。