��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� �ס������ձ��зֱ�װ����ͬ�������ͬpH�İ�ˮ��NaOH��Һ��������10 mL 0.1 mol��L-1 AlCl3��Һ�����ձ��ж��г������ɡ������ж���ȷ����
[? ]
A�����г���һ�������еĶ�
B�����г���һ�������е���
C�����г������ܱ����е���
D�����к����еij�������һ����
�ο��𰸣�D
���������
�����Ѷȣ�һ��
2��ѡ���� ���й��ڵ������Һ��������ȷ����(? )
A�������£���0.1 mol��L-1һԪ��BOH��Һ��pH=10������֪BOH��Һ���ڣ�BOH B++OH-
B++OH-
B�������£�pH��7��NH4Cl�백ˮ�Ļ����Һ�У�c(Cl-)��c(NH4+)��c(H+)��c(OH-)
C���к�pH���������ͬ������ʹ�����Һ������NaOH�����ʵ�����ͬ
D����pH��4������ϡ�ͺ���Һ���������ӵ�Ũ�Ⱦ�����
�ο��𰸣�A
���������A������£�0.1 mol/L��һԪ���pH=10������һԪ�����������Һ�в�����ȫ���룻���ݵ���غ㣬B����ȷ�ı���ʽӦΪ��c(Cl-)��c(NH4+)��c(H+)��c(OH-)��C����������ᣬ���ĵ�NaOH�϶ࣻ����ˮ�����ӻ�������֪������ϡ�ͺ�OH-Ũ��������
�����Ѷȣ�һ��
3��ѡ���� �������Ϊ1 L��pH������2������ʹ����У��ֱ�Ͷ��0.12 gþ�۳�ַ�Ӧ����ͼ�бȽϷ��Ϸ�Ӧ��ʵ��������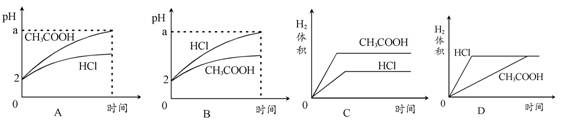
�ο��𰸣�B
�����������
�����Ѷȣ���
4������� ����ͬ�����½���Mg���ᷴӦ�Ķ�Ӧʵ�飬����������£�
?
| þ������
| ����
| ��ʼ�ķ�Ӧ����
| ����H2����
|
��
| 0.24g
| HCl��? 0.2 mol/L 100mL
| ��1
| n1
|
��
| 0.24g
| CH3COOH��0.2 mol/L 100mL
| ��2
| n2
|
��1���ԱȽ��й����Ĵ�С����1 ??��2��n1 ??n2 ���������������������
��2�������ı�������ʹʵ����Ц�1���ͣ������ı�n1��ֵ����д�����ֿ��еķ�����
��??��?
�ο��𰸣���1����1?��?��2��n1��?n2��2����?��ˮϡ��?
��?�������������ƹ�����¡�
�����������1�������Dz��ֵ��룬ͬŨ�ȵ�����£������ƶ���H+Ũ��С����ʼ�ķ�Ӧ���ʱ�ȻС�������ߵķ�Ӧ������þ��������������㣬���е�H+��Ȼ�����û�����������n1��?n2��
��2��ʹʵ����Ц�1���ͣ�ֻҪ����H+��Ũ�ȼ��ɣ����������ܸı䡣���Կ��Լ�������ƹ������Խ����¶�ʹ����ĵ���ƽ�����ơ�
�����Ѷȣ�һ��
5��ѡ���� ������ʵ�У���˵��MOH���������
��0��1mol/LMOH����ʹ��̪��Һ���
��0��1mol/LMCl��Һ�ij�����
��0��1mol/LMOH��Һ�ĵ����Ա�0��1mol/LNaOH��Һ��
�ܵ������0��1mol/LMOH��Һ��0��1mol/LHCl��Һǡ����ȫ��Ӧ
A���٢ڢ�
B���ڢ�
C���ڢ�
D���ۢ�
�ο��𰸣�B
�����������0.1mol/L MOH����ʹ��̪��Һ��죬˵�� MOH��Һ�ʼ��ԣ�������˵�� MOH�ĵ���̶ȣ�����֤�� MOH��������ʣ�����0.1mol/L��MCl��Һ�ij����ԣ�˵��MClΪǿ�������Σ�M+����ˮ���������Һ�����ԣ���MOHΪ������ʣ���ȷ����0.1mol/L MOH��Һ�ĵ����Ա�0.1mol/L NaOH��Һ����˵�� MOH��Һ������Ũ�Ƚ�С�� MOH���ֵ��룬��ȷ���ܵ������0.1mol/L MOH��Һ��0.1mol/L HCl��Һǡ����ȫ��Ӧ��������ǿ��������ǡ����ȫ��Ӧ������ѡB��
�����Ѷȣ�һ��