微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列各组微粒中,互为同位素的是
A.金刚石和石墨
B.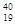 X和
X和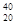 X
X
C.D2O和H2O
D.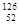 Y和
Y和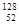 Y
Y
参考答案:D
本题解析:同位素是指,质子相同而中子数不同的同一元素的不同原子互为同位素;
A错,金刚石和石墨是由C元素组成的不同单质,属于同素异形体:
B错,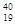 X和
X和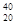 X的质子数不同;
X的质子数不同;
C错,.D2O和H2O都为水,是水分子;
D正确,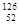 Y和
Y和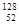 Y互为同位素,它们的质子数,中子数不同。
Y互为同位素,它们的质子数,中子数不同。
本题难度:一般
2、选择题 碳化硅(又名金刚砂)的一种晶体,具有类似于金刚石的结构,其中碳原子与硅原子位置是交替的。下列的各晶体:①晶体硅?②硝酸钾?③金刚石?④碳化硅?⑤干冰,它们的熔点由高到低的顺序是(?)
A.①②③④⑤
B.①④③②⑤
C.③④①②⑤
D.③④①⑤②
参考答案:C
本题解析:这些晶体有的属原子晶体(①③④),②属离子晶体,⑤属于分子晶体。一般来说,熔点:原子晶体>离子晶体>分子晶体;对于晶体类型相同的①③④,由于都是原子晶体,在晶体中键长Si―Si>C―Si>C―C,相应键能Si―Si<C―Si<C―C,故它们的熔点由高到低的顺序是金刚石>碳化硅>晶体硅>硝酸钾>干冰。
本题难度:简单
3、选择题 实验室制取少量干燥的氨气涉及下列装置,其中正确的是
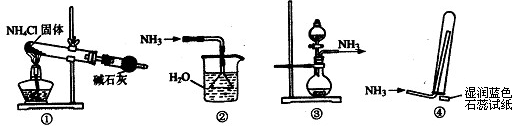
A.①是氨气发生装置
B.②是氨气吸收装置
C.③是氨气发生装置
D.④是氨气收集、检验装置
参考答案:C
本题解析:试题分析:选项A、氨气的制备不能用加热氯化铵固体的方法,因为氯化铵受热分解后生成的两种气体在试管口易反应,重新生成氯化铵固体。
选项B、氨气易溶于水,吸收氨气时应注意防止倒吸,而防止倒吸时,倒置的漏斗应接触液面即可,不可伸入液面下。
选项C、正确。其反应物为生石灰和浓氨水。生石灰具有吸水性,且能与水反应放出大量热,促进了氨气的逸出。
选项D、氨气的检验应用湿润的红色石蕊试纸,遇到氨气,变成蓝色。
考点:实验室制氨气
点评:本题综合考查了氨气的制备、收集、性质检验等方面的内容,属于较为综合的题目。但是所考查的知识点又都是较为基础的内容,考生只需熟练掌握即可解答。
本题难度:简单
4、填空题 (11分)常用于除去高速公路冰雪的是“氯盐类”融雪剂,如NaCl、MgCl2等,请回答:
(1)“氯盐类”融雪剂主要成分的晶体类型为?;
(2)冰比硫化氢熔点高的原因是?,冰分子中氧原子的杂化轨道类型为?;
(3)已知X、Y和Z为第三周期元素,其原子的第一至第四电离能如下表所示:
电离能/kJ・mol-1
| I1
| I2
| I3
| I4
|
X
| 578
| 1817
| 2745
| 11578
|
Y
| 738
| 1451
| 7733
| 10540
|
Z
| 496
| 4562
| 6912
| 9543
|
元素Y第一电离能大于X的原因是?;
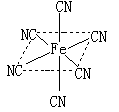
(4)融雪剂对环境危害很大,如和路基上的铁等金属形成原电池,加快路面破损。铁元素应用广泛,Fe2+与KCN溶液反应得Fe(CN)2沉淀,KCN过量时沉淀溶解,生成黄血盐,结构如图。
①写出铁元素基态原子价电子的轨道表示式?;
②已知CN- 与 N2 结构相似,1 mol CN- 中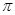 键数目为?;
键数目为?;
参考答案:(1)离子晶体?(2)水分子间存在氢键? sp3?
(3)? Mg为3s2构型,此时3p0全空,特别稳定
(4)①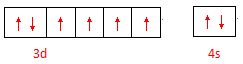 ?②2NA
?②2NA
本题解析:(1)NaCl、MgCl2等均是由离子键形成的离子化合物,因此形成的晶体是离子晶体。
(2)水和硫化氢虽然都是分子晶体,但水分子中存在氢键,所以其熔点高于硫化氢的。水分子中的中心原子有4对电子对,其中2对是孤电子对,所以杂化轨道类型是sp3。
(3)气态电中性基态原子失去1个电子转化为气态基态正离子所需要的最低能量叫第一电离能。根据表中数据可判断X、Y、Z分别是Al、Mg、Na。由于Al是3p1,而Mg为3s2构型,此时3p0全空,特别稳定。
(4)①元素原子的最外层电子是价电子,对于副族和第Ⅷ元素其次外层或倒数第三层电子也可以成为价电子。铁属于第Ⅷ元素,其价电子轨道表达式是
②氮气中氮原子和氮原子形成的化学键是氮氮三键,而三键是由2个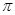 键和1个
键和1个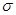 键组成的。CN- 与 N2 结构相似,所以1 mol CN-中
键组成的。CN- 与 N2 结构相似,所以1 mol CN-中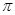 键数目为2NA。
键数目为2NA。
本题难度:一般
5、选择题 短周期元素X和Y能形成XY4化合物,若X的原子序数为m,Y的原子序数为n,则m和n不可能的关系是:(? )
A.m-13=n
B.m -5=n
C.m- n=8
D.n-11=m
参考答案:C
本题解析:由化学式XY4知道,X、Y两元素的化合价为+4、―1,则两元素可能分别属于第IVA族和第VIIA族,即C、Si、F、Cl;另还有CH4、SiH4,综合可知答案为C
本题难度:简单