微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 工业上用固体硫酸亚铁制取颜料铁红(Fe2O3),反应原理是:

2FeSO4?Fe2O3 + SO2↑+SO3↑,某学生欲检验该反应所产生的气态物质,他依次将气体通过盛有(I)BaCl2溶液、(II)x溶液、(III)NaOH溶液的三个装置。则下列对该方案的评价中正确的是(?)
A.(I)中会生成BaSO3、BaSO4两种沉淀
B.可将(I)中的BaCl2溶液改为Ba(NO3)2溶液
C.(III)的作用是检验生成的SO2气体
D.(II)所盛x应为品红溶液
2、实验题 (10分)
(1)浓硫酸和木炭(C)加热时反应的化学方程式为:
?;
为了验证反应的全部生成物,用下图装置进行实验。

(2)上图A处是完成实验的必要装置,它是下列图中的(填编号)?;

(3) C装置中盛放的试剂为?,
其作用是?;
(4)能够证明存在CO2气体的实验现象是:
?。
3、选择题 向下列溶液中通入足量SO2的过程中,一定不会产生沉淀的是?(?)
A.Ba(OH)2
B.Ba( NO3)2
C.Na2S
D.BaCl2
4、填空题 如图每一方框中的字母代表一种反应物或生成物。产物J是含金属元素A的白色胶状沉淀,I为NaCl溶液,D是淡黄色固体单质。试填写下列空白。
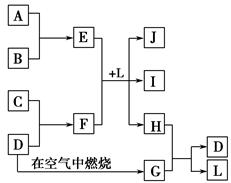
(1)框图中所列物质中属于非电解质的物质的化学式是?。
(2)用电子式表示出H的形成过程?。
(3)将E的水溶液蒸干并灼烧得到的固体物质的化学式为?。
(4)F的水溶液中各离子浓度由大到小的顺序为?。
(5)F的水溶液显碱性的原因:?(用离子方程式表示)。
(6)E与F在L中反应的离子方程式为?。
(7)H和G之间反应的化学方程式为?。
5、选择题 某同学利用下列装置进行浓硫酸和铜反应并验证二氧化硫的性质。按如图实验装置连接仪器和放置药品。加热浓硫酸约1分钟后撤去酒精灯,将铜丝插入液面,反应一段时间后拔出。实验结束后会看到两个试管的液体底部均有少量的白色固体。下列对该实验的现象分析或推断正确的是

A.湿润的蓝色石蕊试纸先变红后褪色
B.左边试管出现的白色固体是由于浓硫酸的脱水性所致
C.从该实验的描述中可以体会出铜与浓硫酸的反应是一个放热反应
D.本实验体现了二氧化硫的酸性、漂白性和弱氧化性