微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 实验室用图示装置制取乙酸乙酯。
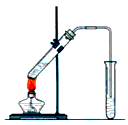
(1)浓H2SO4的作用是:①_____________,②_____________。
(2)右边收集试管内装有_____________,该溶液的作用是_____________________________________。 导气管不能插入液面以下,原因是_____________。加热前,大试管中加入几粒碎瓷片的作用是___________________________。
(3)制取乙酸乙酯的反应方程式是________________________。
(4)实验室可用乙醇来制取乙烯,将生成的乙烯通入溴的四氯化碳溶液,反应后生成物的结构简式是
_________________。
2、实验题 垃圾是放错地方的资源,工业废料也可以再利用。某化学兴趣小组在实验室中用废弃含有铝、铁、铜的合金制取硫酸铝溶液、硝酸铜晶体和铁红(Fe2O3)。其实验方案如下
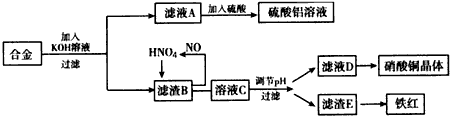
(1)请写出在合金中加入KOH溶液后所发生的离子反应方程式:____________________
(2)在滤液A中直接加入硫酸所获得的硫酸铝溶液中会含有杂质(K2SO4),请设计一个更合理的实验方案由滤液A制备纯净的硫酸铝溶液。依照上图形式画出制备流程图:(提示:在箭头上下方标出所用试剂或实验操作)

(3)已知Fe(OH)3沉淀的pH是2-3.2溶液C通过调节pH可以使Fe3+沉淀完全。下列物质中,可用作调整溶液C的pH的试剂是____(填序号)。
A.铜粉 B.氨水 C.氧化铜 D.氢氧化铜
(4)利用滤液D制取硝酸铜晶体,必须进行的实验操作步骤:加热蒸发、冷却结晶、__________(填操作名称)、自然干燥。
(5)在0.1L的混合酸溶液中c(HNO3) =2 mol/L,c(H2SO4)=3 mol/L。将0.3 mol的铜放入并充分反应后,产生的铜盐的化学式是_____________,被还原的n(HNO3)=_____________。
3、实验题 实验室制备苯甲醇和苯甲酸的化学原理是
 ,
,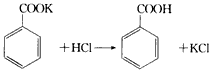
已知苯甲醛易被空气氧化:
苯甲醇沸点为205.3℃;苯甲酸熔点121.7℃,沸点为249℃,溶解度为0.34 g;乙醚(C2H5OC2H5)沸点为
34.8℃,难溶于水,制备苯甲醇和苯甲酸的主要过程如下所示
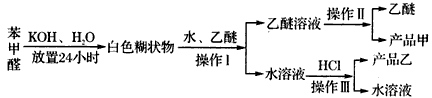
试根据上述信息回答:
(1)操作I的名称是_________,乙醚溶液中所溶解的主要成分是__________。
(2)操作Ⅱ的名称是_____________。
(3)操作Ⅲ的名称是_____________,产品乙是_____________。
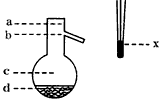
(4)操作Ⅱ中温度计水银球上沿x放置的位置应为_______(图a、b、c或d),该操作中,除需带支管烧瓶、温度计外,还需的玻璃仪器是_________,收集产品甲的适宜温度为___________。
4、实验题 在苹果、香蕉等水果的果香中存在着乙酸正丁酯,它常用于硝化纤维及漆类的溶剂。某化学课外兴趣小组欲以乙酸和正丁醇为原料合成乙酸正丁酯

(Ⅰ)乙酸正丁酯的制备
在干燥的50mL圆底烧瓶中,加入11.5mL(9.25g,0.125mol)正丁醇和7.2mL(7.5g,0.125mol)冰醋酸,再加入3~4滴浓硫酸,摇匀,投入1~2粒沸石。按图(上图)安装带分水器的回流反应装置,并在分水器中预先加入水,使水面略低于分水器的支管口。打开冷凝水,反应瓶在石棉网上用小火加热回流。在反应过程中,通过分水器下部的旋塞分出生成的水,注意保持分水器中水层液面原来的高度,使油层尽量回到反应瓶中。反应达到终点后,停止加热,记录分出的水量。
(Ⅱ)产品的精制
将分水器分出的酯层和反应液一起到入分液漏斗中,用10 mL水洗涤,有机层继续用10 mL10%Na2CO3 洗涤至中性;再用10 mL 的水洗涤,最后将有机层到入小锥形瓶中,用无水可硫酸镁干燥。将干燥后的乙酸正丁酯滤入50 mL 烧瓶中,常压蒸馏,收集124-126 ℃的馏分。称量,得到产品的质量11.34g。
(1)冰醋酸在低温时凝结成冰状固体(熔点16.6℃)。取用方法是____________________。冷水应该从冷凝管_________(填a或b)管口通入;
(2)判断反应终点的依据是:__________________;分水器的使用条件是:__________________。
(3)本实验采用什么方法来提高反应速率和提高产品产率的?___________________________
(4)产品的精制过程中,第一次水洗的目的是__________________,第二层水洗的目的是__________________。洗涤完成后将有机层从分液漏斗的_________放入小锥形瓶中。
(5)该实验过程中,生成乙酸正丁酯的产率是:__________________。
(产率%=实际产量/理论产量×100%)
5、选择题 某化学课外小组利用废铜制取硫酸铜,设计了如下制取方案,其中从理论、操作、经济和环保等方面考虑,你认为最合理的是
[? ]
A.Cu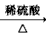 CuSO4
CuSO4
B.Cu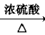 CuSO4
CuSO4
C.Cu CuO
CuO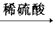 CuSO4
CuSO4
D.Cu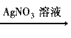 Cu(NO3)2
Cu(NO3)2 Cu(OH)2
Cu(OH)2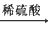 CuSO4
CuSO4