��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��12�֣���ȸʯ��Ҫ��Cu2��OH��2CO3�������������Ļ������Ļ�����Կ�ȸʯΪԭ�Ͽ��Ʊ�CuCl2��3H2O�������������ͼ��
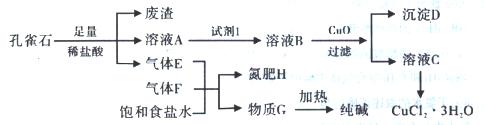
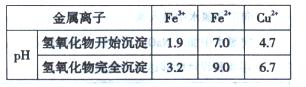
��֪����ҺAֻ��Cu2+��Fe2+��Fe3+���ֽ������ӣ����������ӳ�����pH�����ʾ���ش��������⣺
��1��ͼ�С��Լ�1��Ϊ? ?��
?��
��2������CuO�����ǵ�����ҺpH����pH�ķ�ΧΪ?��
��3������E��F�뱥��ʳ��ˮ��������H��Gʱ��E��FӦ��һ���Ⱥ�˳��ͨ�˱���ʳ��ˮ�С����У�Ӧ��ͨ��������?������ż���Ӧ���ʵĻ�ѧʽ��
��4������ҺC���CuCl2��3H2O����Ҫ����?��?�����˵Ȳ�����
��5����֪��������Cu��OH��2��Ksp=2��10-20������Cu2++2H2O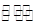 Cu(OH)2+2H+��Ӧƽ�ⳣ��?��
Cu(OH)2+2H+��Ӧƽ�ⳣ��?��
�ο��𰸣�

�����������
�����Ѷȣ�һ��
2��ѡ���� ij��Ԫ�ᣨ��дΪH2A����Һ������ʽ���룺 H2A=H++HA-���� HA-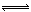 H++A2-����֪������Ũ��Ϊ0.1mol/L��H2A��Һ��c(H+)��0.11mol/L�������0.1mol/L��NaHA��Һ��������������ȷ���ǣ���?��
H++A2-����֪������Ũ��Ϊ0.1mol/L��H2A��Һ��c(H+)��0.11mol/L�������0.1mol/L��NaHA��Һ��������������ȷ���ǣ���?��
A����Һ�϶��������ԣ��������Ի��Ǽ�����ȷ��
B��������0.1mol/L��NaHA��Һ��PH=2
C����Һ��c(Na+)=c(HA-)+ c(A2-)
D����Һ��c(Na+)��c(HA-)��c(A2-)��c(H+)
�ο��𰸣�C
����������ɵ��뷽��ʽ����֪��H2A��һ������Ϊǿ���룬��������Ϊ�����룬����HA-������ˮ�⣬ֻ�������룬��������������NaHA��Һ�����ԣ�A��������HA-�ĵ��������������������㳣����0.1mol/L��NaHA��Һ�е�������Ũ�ȣ���ȷ��PH�ľ���ֵ��B������NaHA��Һ�е�Ԫ���غ����֪����Ԫ����AԪ�ص�Ũ��֮��Ϊ1:1������c(Na+)=c(HA-)+ c(A2-)��C��ȷ��NaHA��Һ�У�HA-�������H+��A2-Ũ����ȣ����ǿ���ˮ�����H+����c(H+)��c(A2-)��D����ѡC��
�����Ѷȣ���
3������� ��12�֣��ڳ����£�����������Һ����0.1mol/L NH4Cl ?��0.1mol/L CH3COONH4��0.1mol/L NH4HSO4?��0.1mol/L NH3��H2O�� 0.1mol/L NH4Cl���Һ?��0.1mol/L NH3��H2O�����Ҫ����д���пհף�
?��0.1mol/L CH3COONH4��0.1mol/L NH4HSO4?��0.1mol/L NH3��H2O�� 0.1mol/L NH4Cl���Һ?��0.1mol/L NH3��H2O�����Ҫ����д���пհף�
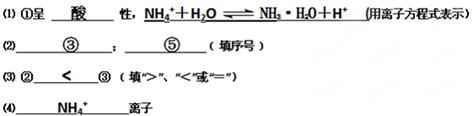
��1����Һ�ٳ�??�ԣ���ᡱ��������С�������ԭ����??�������ӷ���ʽ��ʾ��
��2��������������Һ�У�pH��С����?��c(NH4+)��С����??�z����ũ{
��3���Ƚ���Һ�ڡ�����c(NH4+)�Ĵ�С��ϵ�Ǣ�?�۩z�������������������
��4������Һ����NH3��H2O��?���ӵ����ʵ���Ũ��֮��Ϊ0.2 mol/L��
�ο��𰸣�
�����������
�����Ѷȣ�һ��
4��ѡ���� �����й�ũҵ���⣬����ȡ�Ĵ�ʩ�����������ȷ����(?)
A���̬���ʺͲ�ľ��(��K2CO3)�ܻ��ʩ��
B�����ʺ�ũ�ҷ�(���̷�)���ɻ��ʩ��
C�����μ�ء�����Na2CO3ͨ����ʯ��ʹ֮����̼��ƣ���������ƽ���ƶ�ԭ��������c(CO32��)Ũ�ȵĽ��ͣ����μ�ء��ļ��Խ���
D�����Ϸ�(����������)����ʯ����һ��ʩ��
�ο��𰸣�C
����������̬�������ľ�һ�Ͽ�˫ˮ�⣬Ӫ����ʧ�����ʺ�ũ�ҷ���ȫ�ɻ��ʩ�ã����Ϸ�(����������)����ʯ����һ��ʩ�ã����߽���Ӧ������������ƣ���������ˮ�����ܱ�ֲ�����ա����μ�ء���Na2CO3ˮ��ʹ�����ɼ��ԣ�����CO32����H2O HCO3����OH����ͨ����ʯ�����ɳ���������c(CO32��)Ũ�ȣ�ƽ�����ƣ��������Լ������ʴ�ΪC
HCO3����OH����ͨ����ʯ�����ɳ���������c(CO32��)Ũ�ȣ�ƽ�����ƣ��������Լ������ʴ�ΪC
�����Ѷȣ�һ��
5��ѡ���� �����и���Һ�У��������ʵ���Ũ�ȹ�ϵ������ȷ����
A��0.1 mol/L��(NH4)2SO4��Һ�У�c(SO42-)��c(NH4+)��c(H��)��c(OH��)
B��0.1 mol/L��NaHCO3��Һ�У�c(Na��)��c(HCO3-)��c(H2CO3)��2c(CO32-)
C����0.2 mol/L NaA��Һ��0.1 mol/L��������������ü�����Һ�У�
c(Na��)��c(H��)��c(A��)��c(Cl��)
D����25��100 mL NH4Cl��Һ�У�c(Cl��)��c(NH4+)��c(NH3��H2O)
�ο��𰸣�D
��������� A��0.1 mol/L��(NH4)2SO4��Һ��NH4��ˮ�⣬��Һ�����ԣ�����Һ������Ũ�ȴ�С��ϵ��c(NH4+)��c(SO42-)��c(H��)��c(OH��)��A����ȷ��B��0.1 mol/L��NaHCO3��Һ�и��������غ��֪c(Na��)��c(HCO3-)��c(H2CO3)��c(CO32-)��B����ȷ��C����0.2 mol/L NaA��Һ��0.1 mol/L��������������ü�����Һ�к�����ͬŨ�ȵ�HA��NaA����Һ�Լ��ԣ�˵��A����ˮ��̶ȴ���HA�ĵ���̶ȣ���˸��ݵ���غ��֪��Һ������Ũ�ȴ�С��ϵ��c(Na��)��c(H��)��c(A��)��c(Cl��)��c(OH��)��C����ȷ��D����25��100 mL NH4Cl��Һ�и��������غ��֪c(Cl��)��c(NH4+)��c(NH3��H2O)��D��ȷ����ѡD��
�����Ѷȣ�һ��