微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 将0.39g锌粉加入到20.0 mL的0.200 mol・L-1 MO2+溶液中,恰好完全反应,则还原产物可能是
A.M+
B.M2+
C.M3+
D.MO42-
参考答案:B
本题解析:
试题解析:0.39g锌粉完全反应转移的电子是0.012mol?, MO2+中M的化合价是+5,设还原产物中的化合价是x,则有 0.004×(5-x)=0.012,解得x=2;B正确。
本题难度:简单
2、计算题 (10分)用黄铜矿炼铜按反应物和生成物可将总反应可以写成:
aCuFeS2 + bSiO2 + cO2 → dCu +e FeSiO3 + fSO2
(1)配平上述化学反应方程式:a =___?b=___?c=___?d=___?e=___?f=___?
(2)若2.5吨黄铜矿(含CuFeS280%)发生上述反应,计算生成的SO2在标准状况下的体积(m3)。
(3)若将标准状况下的SO2 280mL通入100mL碘水中充分吸收后,多余的碘用0.182mol/LNa2S2O3溶液滴定(I2 + 2Na2S2O3 =" 2NaI" + Na2S4O6),用去Na2S2O3溶液5.50mL。写出SO2通入碘水中反应的离子方程式。
(4)计算(3)中碘水的物质的量浓度。
参考答案:(1)? 225224(2分)
(2)? 2.5×106g×80%÷184g/mol×2×22.4×10-3m3/mol = 487m3(3分)(无过程不得分,)
(3)? SO2 + I2 +2H2O = 4H+ + SO42- +2I-(2分)
(4)? (0.182mol/L×5.50×10-3L×1/2+0.280L÷22.4L/mol)÷0.100L = 0.130mol/L
(3分,无过程不得分,答案为0.13mol/L扣1分)
本题解析:(1)根据方程式可知,铜元素的化合价从+2价降低到0价,得到2个电子,而氧气在反应中得到4个电子。S元素的化合价从-2价升高到+4价,失去6个电子,所以根据电子的得失守恒和原子守恒可知,配平后的化学计量数依次是2、2、5、2、2、4。
(2)2.5吨黄铜矿中含有CuFeS2的质量是2.5×106g×80%=2.0×106g,所以根据反应的方程式可知,生成的SO2在标准状况下的体积是2.0×106g÷184g/mol×2×22.4×10-3m3/mol = 487m3。
(3)单质碘具有氧化性,能把SO2氧化生成硫酸,反应的方程式是SO2 + I2 +2H2O = 4H+ + SO42- +2I-。
(4)根据反应式I2 + 2Na2S2O3 =" 2NaI" + Na2S4O6可知,剩余的单质碘是0.182mol/L×5.50×10-3L×1/2=5.005×10-4mol。而根据反应式SO2 + I2 +2H2O = 4H+ + SO42- +2I-可知,与SO2反应的单质碘是
0.280L÷22.4L/mol=0.0125mol,所以碘水的浓度是(5.005×10-4mol+0.0125mol)÷0.100L = 0.130mol/L。
本题难度:一般
3、计算题 将4.6g金属钠投入到95.6g水中,计算所得溶液中溶质的质量分数?
参考答案:略
本题解析:略
本题难度:简单
4、选择题 标准状况下,往100 mL 0.1 mol・L-1的FeBr2溶液中通入一定体积的Cl2,充分反应后,溶液中有50%的Br-被氧化。则通入的氯气的体积是( )
A.0.224 L
B.0.336 L
C.0.448 L
D.0.672 L
参考答案:A
本题解析:Fe2+的还原性强于Br-,所以Cl2先氧化Fe2+,再氧化Br-。溶液中有50%的Br-被氧化时则Fe2+完全被氧化。失电子数为0.01mol+0.02mol×50%=0.02mol,所以得电子数为0.02mol,氯气的物质的量为0.01mol,氯气的体积为0.224 L。
点评:本题根据得失电子数相等计算。
本题难度:一般
5、填空题 已知 2Na2O2+2CO2=2Na2CO3+O2,因此Na2O2可在呼吸面具和潜水艇里作供氧剂。
(1)请在答卷上用双线桥法标出上述方程式的电子转移方向和数目。
(2) ??是还原剂,??是还原产物。
(3)若转移3mol电子,则所产生的氧气在标准状况下的体积为??。
参考答案:(1)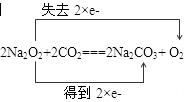 ?[得失未写或电子数写错均不得分]
?[得失未写或电子数写错均不得分]
(2)Na2O2? Na2CO3?(3)33.6L? [每空2分]
本题解析:(1)过氧化钠与二氧化碳的反应中,过氧化钠既是氧化剂又是还原剂,
(2)过氧化钠既是氧化剂又是还原剂,还原产物是氧化剂发生还原反应后的产物,为Na2CO3
(3)每生成1mol的氧气,则转移2mol电子,当转移3mol电子时会有1.5mol的氧气生成,标准状况下的体积为33.6L
本题难度:一般