��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��ұ�������ȼ���״������һ����ҵ������ͼ��ʾ��������������Դ�������ʣ����ٻ�����Ⱦ��
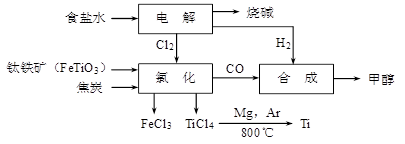
��ش��������⣺
��1��Fe��ԭ������Ϊ26��������������Ϊ2����д����ԭ�ӽṹʾ��ͼ_______��
��2��д���������ڸ������뽹̿���Ȼ��õ����Ȼ��ѵĻ�ѧ����ʽ ��
��3���ȼ���Cl2�����ӷ���ʽΪ
| TiCl4
| Mg
| MgCl2
| Ti
|
�۵�/��
| ��25��0
| 648��8
| 714
| 1667
|
�е�/��
| 136��4
| 1090
| 1412
| 3287
|
��4����TiCl4��Ti��Ӧ��õ�Mg��MgCl2��Ti�Ļ����ɲ����������ķ�������õ�Ti�������±���Ϣ������ȵ��¶��Ը��� �漴�ɡ�
��5��Ϊ�˼��ٲ�ҵ������ʱ�����Ĺ�ҵ���϶Ի�������в����NaCl��FeTiO3�����ʵ���֮��Ϊ ʱ��������Cl2�����������
�ο��𰸣���1��
��2��2FeTiO3��6C��7Cl2����2FeCl3��2TiCl4��6CO ��2�֣�
��3��2Cl- + 2H2O  H2�� + Cl2�� + 2OH-��2�֣�
H2�� + Cl2�� + 2OH-��2�֣�
��4��1412 ��2�֣�
��5��7��1
�����������1����λ��Ԫ�����ڱ��ĵ�4���ڵڢ��壬�ǹ��ɽ���Ԫ�صĴ�����ԭ������Ϊ26�����Ӳ�ṹΪ��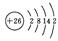
��2����ͼʾ��֪�Ȼ�ʱ�ķ�Ӧ��ΪFeTiO3��C��Cl2��������ΪFeCl3��TiCl4��CO���ٸ��ݵ�ʧ���Ӻ�ԭ���غ㼴�ɵó��÷�Ӧ�ķ���ʽΪFeTiO3��6C��7Cl2����2FeCl3��2TiCl4��6CO��
��3����ҵ���õ�ⱥ��NaCl��Һ�ķ�������ȡNaOH��Cl2��H2����������Ϊԭ������һϵ�л�����Ʒ����Ϊ�ȼҵ��������Ӧ��2Cl����2e��=Cl2����������Ӧ����������Ӧ��2H��+2e��=H2������ԭ��Ӧ������ˣ���ⱥ��ʳ��ˮ���ܷ�Ӧ���Ա�ʾΪ��2Cl�� + 2H2O  H2�� + Cl2�� + 2OH����
H2�� + Cl2�� + 2OH����
��4��Ar���н��з�ֹ�ѡ�þ�������������¶�ʹTiCl4��Mg��MgCl2ת��Ϊ������Ti���ۻ������¶��Ը���1412�棻
��5������2Cl�� + 2H2O  H2�� + Cl2�� + 2OH�����ٸ���ͼʾ��֪�Ȼ�ʱ�ķ�Ӧ��ΪFeTiO3��C��Cl2��������ΪFeCl3��TiCl4��CO���ٸ��ݵ�ʧ���Ӻ�ԭ���غ㼴�ɵó��÷�Ӧ�ķ���ʽΪ2FeTiO3+6C+
H2�� + Cl2�� + 2OH�����ٸ���ͼʾ��֪�Ȼ�ʱ�ķ�Ӧ��ΪFeTiO3��C��Cl2��������ΪFeCl3��TiCl4��CO���ٸ��ݵ�ʧ���Ӻ�ԭ���غ㼴�ɵó��÷�Ӧ�ķ���ʽΪ2FeTiO3+6C+ 2FeCl3+2TiCl4+6CO���ó���ϵʽ2FeTiO3 ~ 7Cl2 ~ 14NaCl������Ϊ�˼��ٲ�ҵ������ʱ�����Ĺ�ҵ���϶Ի�������в����NaCl��FeTiO3�����ʵ���֮��Ϊ7��1ʱ��������Cl2�����������
2FeCl3+2TiCl4+6CO���ó���ϵʽ2FeTiO3 ~ 7Cl2 ~ 14NaCl������Ϊ�˼��ٲ�ҵ������ʱ�����Ĺ�ҵ���϶Ի�������в����NaCl��FeTiO3�����ʵ���֮��Ϊ7��1ʱ��������Cl2�����������
���㣺���黯ѧ��ҵ��������֪ʶ��
�����Ѷȣ�����
2��ѡ���� ��һδ��ɵ����ӷ���ʽ____��XO3-��6H��=3X2��3H2O���ݴ��жϣ���������ͻ�ԭ��������ʵ���֮��Ϊ
A��1��1
B��3��1
C��5��1
D��7��1
�ο��𰸣�C
�������������ԭ���غ�͵���غ�ȷ����ȱ������Ϊ5X������Ӧ��5X�����ϼ����߱�����������������5/2X2��XO3-����ԭ�ɳɻ�ԭ����1/2X2���ʴ�ΪC��
�����Ѷȣ�һ��
3��ѡ���� ���ۺ�ͭ�۵ľ��Ȼ����ƽ���ֳ��ĵȷݣ��ֱ����ͬŨ�ȵ�ϡ���ᣬ��ַ�Ӧ���ڱ�״��������NO�������ʣ��������������±�(������Ļ�ԭ����ֻ��NO)��
���
| ��
| ��
| ��
| ��
|
ϡ�������/mL
| 100
| 200
| 300
| 400
|
ʣ�����/g
| 18��0
| 9��6
| 0
| 0
|
NO���/mL
| 2240
| 4480
| 6720
| V
|
?
���м�������ȷ���� ��? ��
A�������ܽ���5��6gFe? B�������Ũ��Ϊ0��4mol/L
C�������ܽ���9��6gCu?D������V=8960
�ο��𰸣�D
�������������������ݿ�֪��ʵ��١��ڶ��н���ʣ�࣬��Ӧ�����Һ�в����ܺ�������������Һ�н�������Ϊ�������Ӻ�ͭ���ӣ�ʵ�������ʵ��ٵĻ����ϼ���100mL���ᣬ�μӷ�Ӧ�Ľ���������Ϊ8.4g������NO�����Ϊ2240mL�����ʵ���Ϊ0.1mol�����ݵ���ת���غ��֪���μӷ�Ӧ���������ʵ���Ϊ0.1mol����5��2��/2=0.15mol���μӷ�Ӧ������Ħ������Ϊ56g/mol���ù���ֻ��Fe�μӷ�Ӧ����ʵ���ֻ��Fe���뷴Ӧ������NO�������Ϸ���ʽ����μӷ�ӦFe�����ʵ�������������ʵ���������m=nM����μӷ�ӦFe������������c=nV������������ʵ���Ũ�ȣ���ʵ��ڵĻ����ϼ���100mL���ᣬ�μӷ�Ӧ�Ľ���������Ϊ9.6g������NO�����Ϊ2240mL�����ʵ���Ϊ0.1mol�����ù���ֻ��Cu�μӷ�Ӧ�����ݵ���ת���غ㣬��Cu�����ʵ���0.15mol��Cu������9.6g�����ڲμӷ�Ӧ�������������ʸù���ֻ��Cu��Ӧ����Cuǡ����ȫ��Ӧ�������200mL����ʱ��Feǡ�÷�Ӧ����������������ʵ��۵Ļ������ټ���100mL���ᣬ��������Һ���������ӷ�Ӧ����NO�������������ӵ����ʵ��������õ���ת���غ����ý�����NO�����ʵ������ٸ���V=nVm����ý�����NO���������������V��ֵ��A����������������֪��ʵ��ٷ�����Ӧ3Fe+8HNO3�T3Fe��NO3��2+2NO��+4H2O������NO�����ʵ���Ϊ0.1mol�����ݷ���ʽ��֪���μӷ�Ӧ�������ʵ���Ϊ0.15mol������Ϊ8.4g������B����������������֪��ʵ��ٷ�����Ӧ3Fe+8HNO3�T3Fe��NO3��2+2NO��+4H2O������NO�����ʵ���Ϊ0.1mol�����ݷ���ʽ��֪���μӷ�Ӧ����������ʵ���Ϊ0.4mol������������ʵ���Ũ��4mol/L������C��������������֪��ʵ����вμӷ�Ӧ�Ľ���ΪFe��Cuû�вμӷ�Ӧ������D��������������֪��ʵ�����Fe������ǡ�÷�Ӧ������������������NO�����ʵ���0.2mol����3Fe+8HNO3�T3Fe��NO3��2+2NO��+4H2O��֪����Һ���������ӵ����ʵ���Ϊ0.3mol����ʵ��۵Ļ������ټ���100mL���ᣬΪ��������Һ���������ӷ�Ӧ����NO�����ݵ���ת���غ��֪������NO�����ʵ���0.1mol�����Ϊ2240mL��V=6720+2240=8960����ȷ��
�����Ѷȣ�һ��
4������� �Ѽ���Ͻ�����ܶ�С��ǿ�ȸߣ���ʴ���������ܣ����㷺���ں��졢���ա�������ʯ�ͻ�����ҽҩ�Ȳ��ţ���ˣ��ѱ���Ϊ����������ս�Խ����������ѿ���ȡ�����ѣ������ѣ�����Ҫ���չ������£�
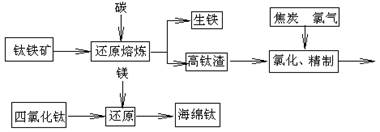
��1�����������Ҫ�ɷ���FeTiO3,��һ�������ķ�Ӧ��FeTiO3+C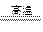 TiO2+Fe+CO��,��FeTiO3�������������У��ѵĻ��ϼ�Ϊ?��
TiO2+Fe+CO��,��FeTiO3�������������У��ѵĻ��ϼ�Ϊ?��
��2���ڶ��������������ڸ������뽹̿��������Ӧ�������Ȼ��Ѻ�һ����̼��д����ѧ����ʽ��?����ԭ������?��
��3����þ�ڸ����»�ԭ���Ȼ��ѣ��÷�Ӧ�Ļ���Ҫ����?��д����ѧ����ʽ?��
��4����þ����Ҫ�ɷ���̼��þ�����պ��뽹̿������Ȼ����и�����ͨ�����������Ȼ�þ����������Ȼ�þ�õ�þ��
��д����þ�����ռ��Ȼ���ȡ�Ȼ�þ�Ļ�ѧ����ʽ��?��
��д����������Ȼ�þ�ĵ�ⷽ��ʽ?��
�ο��𰸣�
��1��+4��?��2��TiO2+2C+2Cl2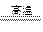 TiCl4+2CO?���Ȼ���? (3)�������屣��? 2Mg+TiCl4
TiCl4+2CO?���Ȼ���? (3)�������屣��? 2Mg+TiCl4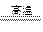 2MgCl2+Ti?
2MgCl2+Ti?
(4)��MgCO3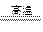 MgO+CO2��,MgO+Cl2+C
MgO+CO2��,MgO+Cl2+C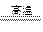 MgCl2+CO;��MgCl2
MgCl2+CO;��MgCl2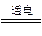 Mg+Cl2��
Mg+Cl2��
�����������1������������������֪������+2�ۣ��ӷ�Ӧʽ������ʧ����������ȣ�˵���ѻ��ϼ�û�б䣬���ѳ�+4�ۡ���2�����ݷ�Ӧ��Ͳ���д��ѧ����ʽ��ע����ƽ����3��������þ���Ѷ����������������Ӧ����Ҫ�ڱ������л�ԭ�ѣ������ö�����̼�͵���������������Ϊþ���������̼�͵�����Ӧ���ö�����������������������ȡ���4��̼��þ�ֽ�����̼��ƣ������������½�̿��ԭ����þ�����Ȼ�þ��һ����̼����������Ȼ�þ����þ�����������н̲��г����˵��ˮ�����н������õ�ⷨұ��þ�������ƵȻ��ý�����
�����Ѷȣ�һ��
5������� (16��) �Ե�ⷨ���������̲������������У����̺����ߴ�40%��50%����Ҫ�ɷ�ΪMnO2��ˮ����Һ�����������Pb2+��Sn2+���ؽ������ʡ������ղ��õ�ľм��������ά���ڽ�Ũ��������������͡�ˮ�����ɻ�ԭ�ǣ����������£�����������̷�Ӧ���ɿ����Ե������̡�

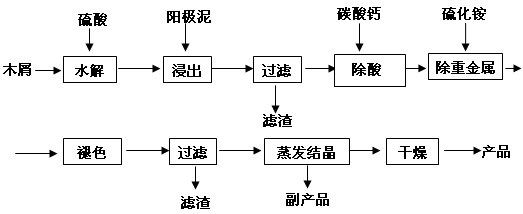
��1����ҵ�ϵ�������̵�ˮ��Һ���������̣������ĵ缫��ӦʽΪ ��
��2��д��ľмˮ�ⷴӦ�Ļ�ѧ����ʽ�� ����ƽ�������跴Ӧ����ʽC6H12O6 + MnO2 + H2SO4�� MnSO4 + CO2 + H2O
��3����ȡ������������裬������� ���壨�ѧʽ������Ⱦ������
��4�������յ�һ�ָ���Ʒ����Ҫ��ũҵ�������ϣ�д���仯ѧʽ ��
��5��ȡһ���������������ʵ��������õ�����ͼ����������������Ϊ mL������������������������ᵼ�� ���ѧʽ��������������
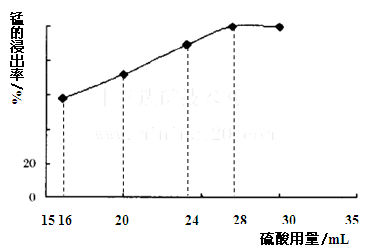
��6��ij��������MnO2����Է�������Ϊ87������������Ϊ50.0%����174g����������320g36.5%��Ũ�����ϼ��ȣ�������������ڱ�״����Ӧ���� L���������������е������ɷֲ����뷴Ӧ��
�ο��𰸣���1��4OH- -4e-��O2 + 2H2O ��2H2O
���������
�����Ѷȣ�����