��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� �����ƣ�Na2SX�����Ƹ﹤ҵ�г�����Ƥë����ë����ũҵ�Ͽ���ɱ�����Ҳ�Ƿ�����ѧ�еij����Լ����ڼ�����Һ�У�Na2SX��NaBrO3������Ӧ����Na2SO4��NaBr��
(1)��������Ӧ�з���������Ӧ��������?������ԭ��Ԫ����?����дԪ�ط��Ż�ѧʽ����
(2)����Na2SX��NaBrO3��Ӧ�����ʵ���֮��Ϊ3��10����x = ?��
(3)��NaBrO3Ҳ������������������NaBr��Ӧ����Br2��������6mol Br2����Ӧ��ת�Ƶ��ӵ����ʵ���Ϊ?��
(4)����������������Ӧ������֪Na2SX�� Br2��NaBr��ԭ����ǿ������˳����?����д��ѧʽ����
�ο��𰸣�Na2SX��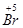 ?��1��1�𣬹�2�֣�
?��1��1�𣬹�2�֣�
3 ��2�֣�
10 mol ��2�֣�
Na2SX > NaBr > Br2��2�֣�
���������(1)��ӦNa2SX+NaBrO3��Na2SO4+NaBr�У���Ļ��ϼ���+5�۽�����1�ۣ�����ԭ������Ԫ�صĻ��ϼ��ɸ�������+6�ۣ�������
��2��Na2SX��x����ԭ�ӵĻ��ϼ۹���2�ۣ����վ���Ϊ+6�ۣ�������6x+2�ۣ���NaBrO3����Ļ��ϼ���+5�۽�����1�ۣ�������6�ۣ�Ϊ�����غ㣬���ߵ����ʵ�����Ϊ3��3x+1����Na2SX��NaBrO3��Ӧ�����ʵ���֮��Ϊ3��10���ɵ�x=3
(3)��Ԫ�ط����˹��з�Ӧ��BrO3����5Br����6H��=3Br2��3H2O����Ӧ����5�����ӵ�ת�ƣ�����6mol Br2����Ӧ��ת�Ƶ��ӵ����ʵ���Ϊ10mol
��4�����ݻ�ԭ���Ļ�ԭ��ǿ�ڻ�ԭ����Ļ�ԭ�Կɵ�Na2SX�� Br2��NaBr��ԭ����ǿ������˳����Na2SX > NaBr > Br2
�����Ѷȣ���
2��ѡ���� ���з�Ӧ�в�����������ԭ��Ӧ���ǣ�?��
A��Cl2+H2O====HCl+HClO
B��3CO+Fe2O3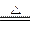 2Fe+3CO2
2Fe+3CO2
C��CaCO3+SiO2 CaSiO3+CO2��
CaSiO3+CO2��
D��3CuS+8HNO3====3Cu��NO3��2+2NO��+3S��+4H2O
�ο��𰸣�C
����������ж�ij��Ӧ�Ƿ�����������ԭ��Ӧ�ķ����Ǽ�鷴Ӧǰ��Ԫ�صĻ��ϼ����ޱ仯��A�е���Ԫ�أ�B�е�̼������Ԫ�أ�D������Ԫ�ػ��ϼ۾��б仯������������ԭ��Ӧ��Ψ��C�и�Ԫ�صĻ��ϼ��ޱ仯���ʲ�����������ԭ��Ӧ��
�����Ѷȣ���
3������� ���з�Ӧ������Ԫ�صĻ��ϼ������ˣ�����Ԫ�صõ���ƫ���˵��ӣ��������ʷ�����������Ӧ��
Fe2O3+3CO 2Fe+3CO2
2Fe+3CO2
�ο��𰸣�̼Ԫ�صĻ��ϼ������ˣ���Ԫ�صõ����ӣ�CO������������Ӧ��
���������
�����Ѷȣ�һ��
4������� ijһ��Ӧ��ϵ���з�Ӧ��������ﹲ5�����ʣ�S��H2S��HNO3��NO��H2O���÷�Ӧ�л�ԭ������
___________������Ӧ������ת����0.3���ӣ������������������__________��
�ο��𰸣�NO��4.8g
���������
�����Ѷȣ�һ��
5��ѡ���� ��֪��������(HCNO)�ṹʽΪH��N��C��O�����е�Ԫ��Ϊ��3�ۣ�HCNO�ܺ�NO2��Ӧ����N2��CO2��H2O.����˵����ȷ����(����)��
A���ڷ�Ӧ�У�HCNO�ȱ������ֱ���ԭ
B���ڷ�Ӧ�У�NO2����������HCNO�ǻ�ԭ��
C���ڷ�Ӧ�У�NO2��HCNO�����ʵ���֮��Ϊ1��1
D��ÿ����1 mol CO2��4 mol����ת��
�ο��𰸣�B
�����������������̼Ԫ�صĻ��ϼ��ǣ�4�ۣ������ڷ�Ӧ��̼Ԫ�صĻ��ϼ۲��䡣��NԪ�صĻ��ϼ���ӣ�3�����ߵ�0�ۡ���NO2�е�Ԫ�صĻ��ϼ۴ӣ�4�۽��͵�0�ۣ����NO2����������HCNO�ǻ�ԭ�������ݵ��ӵĵ�ʧ�غ���ƣ��������ͻ�ԭ�������ʵ���֮����3�U4�����Է�Ӧ�ķ���ʽΪ8HCNO��6NO2=7N2��8CO2��4H2O����˸��ݷ���ʽ��֪��ÿ����1 mol CO2��3 mol����ת�ƣ����Դ�ѡB��
�����Ѷȣ�һ��