微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列反应中,属于氧化还原反应的是
[? ]
①Na2O2+2HCl===2NaCl+H2O2 ②2Na2O2+2H2O===4NaOH+O2↑
③Cl2+H2O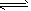 HCl+HClO ④ICl+H2O===HCl+HIO
HCl+HClO ④ICl+H2O===HCl+HIO
A.①④
B.①③
C.②③
D.只有②
2、填空题 氧化还原反应在生产、生活中具有广泛的用途,贯穿古今。
(1)下列生产、生活的事例中发生了氧化还原反应的是?。
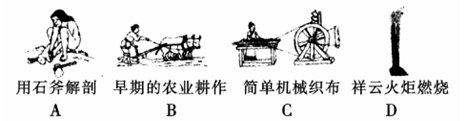
(2)水是人体的重要组成部分,是人体中含量最多的一种物质。而“四种基本反应类型与氧化还原反应的关系”也可用如图表达。
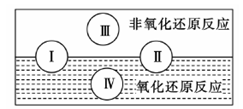
试写出有水参加、水为还原剂且为类型Ⅳ的一个化学方程式:?。
(3)NaNO2是一种食品添加剂,它能致癌。酸性KMnO4溶液与NaNO2反应的离子方程式是:

①请补充完整,配平方程式并标出电子转移的方向和数目。
②某同学称取了7.9 g KMnO4,固体,欲配制100 mL溶液。回答下列问题:
该实验中,使用容量瓶时要检查是否漏水,其操作是?。
③不规范的实验操作会导致实验结果的误差。下列操作会使实验结果偏小的是?(填序号)。
A.在溶解过程中有少量液体溅出烧杯外
B.定容时仰视容量瓶上的刻度线
C.定容后,将容量瓶振荡摇匀后,静置发现液面低于刻度线,于是又加入少量水至刻度线
④某同学用上述配好的KMnO4溶液滴定未知浓度的NaNO2溶液:取20 mL未知浓度的NaNO2溶液于锥形瓶;取上述配好的KMnO4溶液于________(填“酸式”或“碱式”)滴定管,滴定完成后消耗KMnO4溶液10 mL,则NaNO2溶液的浓度为________________。
3、计算题 FeCl3可用作印刷电路铜板腐蚀剂。为回收废腐蚀液中的铜,必须对废腐蚀液的组成进行分析。某同学取废腐蚀液200mL,分成甲、乙两等份。向甲溶液中滴加AgNO3溶液至不再有沉淀产生,得到沉淀129.15g;向乙溶液中加入10g足量铁粉,充分反应,剩余固体质量4.8g。计算中忽略溶液体积的变化。
(1)写出FeCl3溶液腐蚀印刷电路铜板的离子方程式,并标出电子转移的方向和数目。
__________________________
(2)废腐蚀液中含有的Cl-离子的物质的量浓度是_________________。
(3)计算废腐蚀液中铜离子的物质的量浓度(写出计算过程)。
4、选择题 关于反应

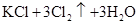 的有关叙述中,正确的是(?)
的有关叙述中,正确的是(?)
A.KCl中含有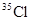
B.KCl中含有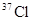
C.生成物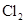 的相对分子质量大于71
的相对分子质量大于71
D.该反应转移电子数为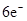
5、选择题 取相同体积的KI、Na2S、FeBr2溶液,分别通入足量的Cl2,当反应恰好完成时,消耗Cl2的体积相同(同温、同压下),则KI、Na2S、FeBr2溶液的物质的量浓度之比是(?)
A.2:1:3
B.6:3:2
C.1:1:2
D.3:2:1