微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、计算题 ?反应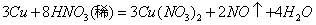 ,
,
(1)请用双线桥标出反应中电子转移的情况。(3分)
(2)若有19.2g Cu被氧化,则被还原的HNO3的质量为多少?(7分)
参考答案:(1)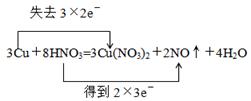 (2)12.6g
(2)12.6g
本题解析:(1)根据反应的化学方程式可知,在反应中铜的化合价从0价升高到+2价,失去个电子。硝酸中氮元素的化合价从+5价降低到+2价,得到3个电子,所以用双线桥标出反应中电子转移的情况是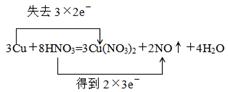 。
。
(2)19.2g铜到物质的量是19.2g÷64g/mol=0.3mol
则被还原的硝酸是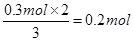
质量是0.2mol×63g/mol=12.6g
点评:该题是中等难度的试题,试题基础性强,侧重能力的培养和解题方法的指导与训练。试题难易适中,贴近高考,有助于培养学生的逻辑思维能力和发散思维能力,提高学生的规范答题能力和应试能力。
本题难度:一般
2、选择题 合金是一类用途广泛的金属材料。下列物质中属于合金的是
A.钢
B.氢氧化铝
C.金刚石
D.四氧化三铁
参考答案:A
本题解析:考查合金的概念:由两种或两种以上的金属或非金属熔合在一起的物质。
BCD均为纯净的单质或化合物,排除,而钢是铁与碳等其它元素熔合在一起的一种合金,符合题意。
本题难度:一般
3、选择题 已知氧化还原反应:
2Cu(IO3)2+24KI+12H2SO4=2CuI↓+13I2+12K2SO4+12H2O
其中1 mol氧化剂在反应中得到的电子为(?)
A.10mol
B.11mol
C.12mol
D.13mol
参考答案:B
本题解析:这是一个氧化还原反应,氧化剂所得到的电子数与还原剂所失去的电子数相等,每反应掉2mol的碘酸铜就反应掉24mol的碘化钾,其中作还原剂的碘化钾为22mol,共失去22mol的电子,那么有1mol的氧化剂参加反应时,所得到的电子就为11mol。选B
本题难度:一般
4、选择题 所谓合金,就是不同种金属(也包括一些非金属)在熔化状态下形成的一种熔合物,下表为四种金属的熔、沸点:
?
| Na
| Cu
| Al
| Fe
|
熔点(℃)
| 97.5
| 1 083
| 660
| 1 535
|
沸点(℃)
| 883
| 2 595
| 2 200
| 3 000
|
根据以上数据判断其中不能形成合金的是
A.Cu和Na ? B.Fe和Cu
C.Fe和Al? D.Al和Na
参考答案:A
本题解析:由合金的形成可知,两种金属若能够形成合金,则熔点较高的金属的熔点不能大于熔点较低的金属的沸点。铜的熔点高于钠的沸点,两种金属不能形成合金。选A。
本题难度:一般
5、选择题 已知2MOyx-+5S2-+16H+=2M2++5S↓+8H2O,则MOyx-中的x的值为(?)
A.1
B.2
C.3
D.4
参考答案:A
本题解析:根据电子的得失守恒可知5×2=2×n,解得n=5,即MOyx-在反应中得到5个电子,所以化合价是+7价。根据原子守恒可知,y=4,所以x=1,答案选A。
本题难度:一般