微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 用简便的方法鉴别硫酸铜、碳酸钠、氢氧化镁三种白色固体粉末,应选用的最佳试剂是
A.稀盐酸
B.紫色石蕊试液
C.水
D.氢氧化钠溶液
参考答案:C
本题解析:略
本题难度:一般
2、实验题 据统计,每年世界上银总消耗量的40%用于感光材料的生产,感光材料经曝光、显影、定影后,黑白片上的银80%左右进入定影液,彩色片上的银几乎全部进入废定影液,所以废定影液中银的含量是十分惊人的。
某研究性学习小组拟对某照相公司的废定影液进行实验处理,回收其中的银和溴。
(一) 资料支撑:
① 定影液(硫代硫酸钠,Na2S2O3)跟胶片或相纸上没有感光部分的溴化银反应,反应方程式为:AgBr(s)+? 2Na2S2O3(aq) = Na3[Ag(S2O3)2](aq) + NaBr(aq)。
② 在酸的作用下,Na3[Ag(S2O3)2]能转化为不溶性的Ag2S。反应原理为:
6HCl+2Na3[Ag(S2O3)2]=6NaCl+Ag2S↓+3S↓+3SO2↑+H2SO4+2H2O。
③溶液中有少量溴化银,可用锌将其还原出来。
(二) 实验程序设计

(三) 试回答下列问题
(1)本实验需用6mol/L的盐酸250mL,配制时除需量筒、烧杯、玻璃棒外,还需用的仪器有:?、?。
(2)指出流程图中操作所包含的装置是(填序号:A、B、C)Ⅰ?Ⅱ?Ⅲ?。

(3)步骤③是在空气中灼烧的。该反应的化学方程式:?。实验操作时,加入适量的硝酸钾加盖后再灼热,加硝酸钾的目的可能是:?。
(4)加入锌粉发生的离子反应为:?。
参考答案:(1)250mL容量瓶、胶头滴管 (2)C;B;A
(3)Ag2S + O2 2Ag + SO2;释放氧气,使硫化银完全被氧化;
2Ag + SO2;释放氧气,使硫化银完全被氧化;
(4)2AgBr + Zn =" Ag?" + Zn2+ + 2Br-.
本题解析:前两题主要考查了基本实验操作。一是物质的量浓度溶液的配制,需要用到容量瓶(注意要写规格)和胶头滴管。一是过滤、萃取分液、蒸馏三种基本的物质分离方法。
未知反应的方程式书写,由题示中分析出滤渣主要是Ag2S,而产物是Ag,由于在空气中发生,少不了氧气的参与。根据氧化还原规律,推知尚有另一种产物二氧化硫。方程式写出,自然可以判断出硝酸钾的用途是为了放出氧气以便氧化更加彻底。
本题难度:一般
3、实验题 “套管实验”具有装置简洁便利等优点,结合下面的图示回答有关问题。

(1)欲利用图A比较碳酸氢钠和碳酸钠的热稳定性,并检验分解产物,最好应在大试管内底部加入 ____(填化学式),石灰水变浑浊的烧杯是 ___(填“甲”或“乙”)。
(2)欲利用图B验证铜与浓硝酸的反应产物,该装置除简洁外,你认为最明显的一个优点是___。
(3)用锌粒和稀硫酸用图C仪器制取并收集一试管氢气,锌粒和稀硫酸应放在____(填“大”或 “小”)试管中组成发生装置,理由是____, 该反应的离子方程式为____。
参考答案:(1) Na2CO3 ;乙
(2)污染物未排入大气,便于控制 反应的进行与停止
(3)小 ;便于收集H2 ;Zn+ 2H+=Zn2++H2↑
本题解析:
本题难度:一般
4、选择题 根据下列实验现象,所得结论不正确的是( )
| 实验 | 装置 | 实验现象 | 结论
A
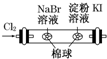
左边棉球变为橙色,右边棉球变为蓝色
氧化性:Cl2>Br2>I2
B
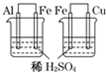
左边烧杯中铁表面有气泡,右边烧杯中铜表面有气泡
活动性:Al>Fe>Cu
C
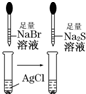
白色固体先变为淡黄色,后变为黑色(Ag2S)
溶解性:AgCl>AgBr>Ag2S
D
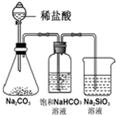
锥形瓶中有气体产生,烧杯中液体变浑浊
酸性:HCl>H2CO3>H2SiO3
|
A.A
B.B
C.C
D.D
参考答案:A、氯气具有氧化性,能将溴离子氧化为溴单质,溴单质为橙色,同时次氯酸的漂白性将橙色漂白,氯气能将碘离子氧化为碘单质,碘单质遇到淀粉显示蓝色,同时次氯酸的漂白性将橙色漂白,所以氧化性是Cl2>Br2,Cl2>I2,现象是:左边棉花先变橙色再变无色,右边棉花先变蓝色后变无色,故A错误;
B、两个烧杯形成原电池的工作原理,左边烧杯中,金属铝是负极,右边烧杯中金属铁是负极,在原电池的正极上会产生氢气,负极活泼性强于正极,故B正确;
C、氯化银的溶解能力大于溴化银,溴化银的溶解能力大于碘化银,根据现象结合沉淀会向着更难溶的方向转化,所以溶解性:AgCl>AgBr>Ag2S,故C正确;
D、锥形瓶中有气体二氧化碳产生,烧杯中液体有浑浊硅酸产生,现说明盐酸酸性强于碳酸,碳酸酸性强于硅酸,故D正确.
故选A.
本题解析:
本题难度:简单
5、实验题 如图所示,以石墨为电极电解A的水溶液,并做下面一系列实验。试根据实验现象完成下列问题(电解质A的水溶液焰色反应呈紫色)。?
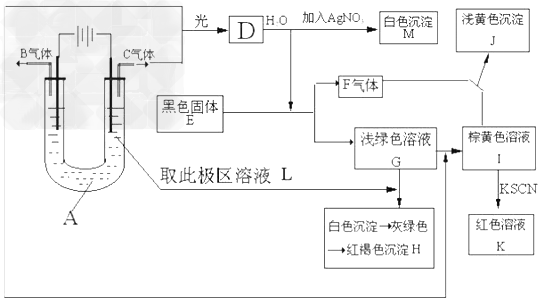
(1)A的化学式为__________,E的名称为____________
(2)I和F反应的离子方程式是____________。
(3)若将电解装置中的阳极换成铁棒,则在U型管底部可观察到的现象是______________,电解的化学方程式为______________。
参考答案:(1)KCl;?硫化亚铁?
(2)2Fe3+?+?H2S==2Fe2+?+?S↓+?2H+
(3)产生了白色絮状沉淀,变成灰绿,后变成红褐色。?Fe+2H2O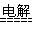 Fe(OH)2↓+H2?↑
Fe(OH)2↓+H2?↑
本题解析:
本题难度:一般