微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 已知:A、B、C、D、E、F六种元素核电荷数依次增大,属周期表中前四周期的元素。其中A原子核外有三个未成对电子;化合物B2E的晶体为离子晶体,E原子核外的M层中只有两对成对电子;C元素是地壳中含量最高的金属元素;D单质的熔点在同周期元素形成的单质中最高;F能形成红色(或砖红色)的F2O和黑色的FO两种氧化物。
回答下列问题:
(1)F的原子的M层电子排布式为?。
(2)B、C、D的第一电离能由小到大的顺序为?。(用元素符号表示)
(3)A的简单氢化物分子极易溶于水,其主要原因是?.
(4)E的最高价氧化物分子的空间构型是?。其中心原子的杂化方式为?。
(5)F的高价离子与A的简单氢化物形成的配离子,配位数为?。
(6)A、F形成某种化合物的晶胞结构如图所示,则其化学式为?;(黑色球表示F原子),已知紧邻的白球与黑球之间的距离为a cm, 该晶胞的密度为??g/cm3。
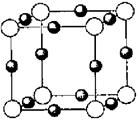
参考答案:(1)3s23p63d10(2分)
(2)Na<Al<Si(2分)
(3)氨分子与水分子之间存在氢键(2分)
(4)平面正三角形(2分)? sp2(1分)?
(5) 4(2分)?
(6)Cu3N?(2分)?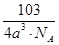 ?(2分)(其它合理答案也给分)
?(2分)(其它合理答案也给分)
本题解析:原子核外有三个未成对电子,其电子排布式为1S22S22P3,为N元素,E原子核外的M层中只有两对成对电子,电子排布式为1s22s22p3,应为S元素,C元素是地壳中含量最高的金属元素,为Al元素,化合物B2E的晶体为离子晶体,B应为第ⅠA族元素,且原子序数在N元素和Al之间,应为Na元素,D单质的熔点在同周期元素形成的单质中是最高的,应为Si元素,单质硅为原子晶体,熔点在第三周期中最高,F能形成红色(或砖红色)的F2O和黑色的FO两种氧化物,应为Cu元素.
(1)Cu的原子的电子排布式为1s22s22P63s23p63d104s1,M层电子排布式为3s23p63d10
(2)在元素周期表中,同一周期元素的第一电离能从左到右逐渐增大,同一主族元素的第一电离能从上到下逐渐减小,据此可判断三种元素的第一电离能的顺序为:Na<Al<Si
(3)A(N)的简单氢化物分子是氨气,氨气极易溶于水,其主要原因N、O的电负性强,分子之间形成氢键;
(4)S03中含有3个δ键,孤电子对数为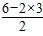 =0,所以分子的空间构型是平面正三角形,sp2杂化?
=0,所以分子的空间构型是平面正三角形,sp2杂化?
(5)铜离子与氨气可以配位键形成配合物,其化学式为,[Cu(NH3)4]2+
(6)根据晶胞中微粒个数的分配方法计算,晶胞中含有原子的数目为8×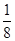 =1,原子的数目为:12×
=1,原子的数目为:12×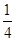 =3,故化学式为Cu3N,白球与黑球之间的距离为a cm,边长为2acm,则
=3,故化学式为Cu3N,白球与黑球之间的距离为a cm,边长为2acm,则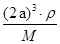 ×NA=1,解得ρ=
×NA=1,解得ρ=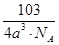 ?。
?。
本题难度:困难
2、填空题 在氢、氮、氯和钠四种元素中:
(1)有2种元素组成的共价化合物的水溶液显酸性,这种化合物的电子式是?;
(2)有2种元素可形成离子化合物,用子电式表示其形成过程:
?;
(3)在它们可能形成的双原子分子的单质中,化学性质最稳定的是:
?。(写化学式)
参考答案:
18、(1)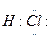 ? H―N―H
? H―N―H
 (2)Na・+
(2)Na・+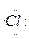 →Na+[
→Na+[ ]-?(3)N2
]-?(3)N2
本题解析:略
本题难度:简单
3、简答题 在①HF、②H2S、③BF3、④CS2、⑤CCl4、⑥N2、⑦SO2分子中:
(1)以非极性键结合的非极性分子是______
(2)以极性键相结合,具有直线型结构的非极性分子是______
(3)以极性键相结合,具有正四面体结构的非极性分子是______
(4)以极性键相结合,而且分子极性最大的是______.
参考答案:(1)以上几种物质中,只有⑥为单质,只有非极性键,则属于非极性分子,故答案为:⑥;
(2)以极性键相结合的物质有①②③④⑤⑦,直线型的分子为①④,但④为非极性分子,故答案为:④;
(3)以极性键相结合的物质有①②③④⑤⑦,具有正四面体结构的非极性分子只有⑤,故答案为:⑤;
(4)以极性键相结合的分子有①②⑦,因F的非金属性最强,则电子对的偏移最大,则①的极性最大,故答案为:①.
本题解析:
本题难度:一般
4、填空题 A、B、C、D四种短周期元素,A元素有三个电子层,其中最外层电子数占总电子数的1/6;B元素原子核外电子数比A元素原子核外电子数多1;C-离子核外电子层数比A元素的离子核外电子层数多1;D元素原子最外层电子数是次外层的2倍.请填写下列空格:
(1)请写出A的元素符号______;(2)C的负一价阴离子的结构示意图______;
(3)C、D两元素形成的化合物的电子式______.
(4)A、B两元素相比较,A元素的金属性较强,可以验证该结论的实验是______
A.将这两种元素的块状单质分别放入冷水中
B.将这两种元素的单质分别和同浓度的盐酸反应
C.将这两种元素的单质粉末分别和热水作用,并滴入酚酞试液
D.比较这两种元素的气态氢化物的热稳定性.
参考答案:A元素有三个电子层,其中最外层电子数占总电子数的16,设最外层电子数为x,则有xx+2+8=16,x=2,故A为Mg元素,B元素原子核外电子数比A元素原子核外电子数多1,应为Al元素,C-离子核外电子层数比A元素的离子核外电子层数多1,则C-离子核外有3层电子,C为Cl元素,D元素原子最外层电子数是次外层的2倍,应为C元素,则
(1)由以上分析可知A为Mg元素,故答案为:Mg;
(2)C原子核内用17个质子,C的负一价阴离子核外各层电子数分别为2、8、8,结构示意图为
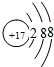
,故答案为:
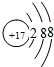
;
(3)C、D两元素形成的化合物为CCl4,分子中各原子核外最外层达到8电子稳定结构,电子式为
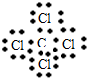
,故答案为:

;
(4)A.将这两种元素的块状单质分别放入冷水中,都不能与冷水反应,故A错误;
B.将这两种元素的单质分别和同浓度的盐酸反应,镁反应较剧烈,可以证明Mg的金属性较强,故B正确;
C.将这两种元素的单质粉末分别和热水作用,并滴入酚酞试液,Mg可以可热水反应,生成Mg(OH)2,溶液呈碱性,而Al难以反应,可证明Mg的金属性较强,故C正确;
D.两种金属元素都不能形成氢化物,故D错误.
故答案为:BC.
本题解析:
本题难度:一般
5、填空题 研究物质的微观结构,有助于人们理解物质变化的本质。请回答下列问题:
(1)C、Si、N元素的电负性由大到小的顺序是__________。 C60和金刚石都是碳的同素异形体,二者比较熔点高的是___________,原因是__________________________。
(2)A、B均为短周期金属元素,依据下表数据,写出B的基态原子的电子排布式__________________。
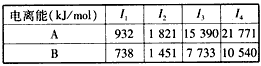
(3)过渡金属离子与水分子形成的配合物是否有颜色,与其d轨道电子排布有关。一般地,为d0或d10排布时,无颜色;为d1-d9排布时,有颜色。如[Co(H2O)6]2+显粉红色。据此判断,[Mn(H2O)6]2+_________(填“无”或 “有”)颜色。
(4)利用CO可以合成化工原料COCl2、配合物Fe(CO)5等。
①COCl2分子的结构式为 每个COCl2分子内含有______个σ键,________个π键。其中心原子采取_________ 杂化轨道方式。
每个COCl2分子内含有______个σ键,________个π键。其中心原子采取_________ 杂化轨道方式。
②Fe(CO)5在一定条件下发生分解反应:Fe(CO)5(s) = Fe(s) +5CO(g),反应过程中,断裂的化学键只有 配位键,则形成的化学键类型是_______________。
参考答案:(1)N>C>Si;金刚石;金刚石为原子晶体,而C60为分子晶体
(2)1s22s22p63s2
(3)有
(4)①3;1;sp2②金属键
本题解析:
本题难度:一般