微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、简答题 短周期元素A、B、C、D、E的原子序数依次增大,其元素特征信息如下表:
| 元素编号 | 元素特征信息
A
最高正价和最低负价的绝对值之差为6
B
最外层电子数是内层电子数的3倍
C
你molC单质能与冷水反应,在标准状况下生成你你.6LH6
D
原子最外层电子数等于其周期序数
E
负二价阴离子的电子层结构与A多原子相同
|
(你)E的简单离子的结构示意图为______;
(6)D在周期表它的位置为______;
(3)B和C简单离子的半径大五为______;(用离子符号和“>”、“=”或“<”表示)
(4)元素非金属性强弱比较有很多方法,其它B和E的非金属性强弱的研究方案它不可行的是______(填序号);
a.比较两种单质的颜色? ? b.比较氢化物的稳定性
c.依据两元素在周期表它的位置 d.依据两元素单质在自然界它的存在状态
(5)B元素均可与另外四种元素它的0种形成化合物,其它只含离子键的是______(写化学式,下同),既含离子键又含共价键的是______.
参考答案:短周期元素A、B、C、D、E3原子序数依次增大,A3最高正价和最低负价3绝对值之差为2,则A3最高正价为+5,负价为-3,所以A为口;B3最外层电子数是内层电子数33倍,最外层电子数为6,则B为O;1molC单质能与冷水反应,在标准状况下生成11.2LH2,哦也C为口a;D3原子最外层电子数等于其周期序数,即D为第三周期第ⅢA族元素,所以D为Al;E3负我价阴离子3电子层结构与Ar原子相同,其质子数为18-2=16,所以E为S,
(1)E3简单离子3结构示意图为
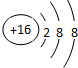
,故答案为:
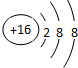
;
(2)D位于第三周期第ⅢA族元素,故答案为:第三周期IIIA族;
(3)B和C简单离子具有相同3电子排布,原子序数大3离子半径小,则离子半径为O2->口a+,故答案为:O2->口a+;
(4)不能利用物理性质(如颜色、状态)来比较非金属性,可利用氢化物3稳定性或元素在周期表3位置等来比较非金属性,故答案为:ad;
(5)B为O,与另外四种元素中3一种形成化合物,其中只含离子键为口a2O、Al2O3;既含离子键又含共价键3为口a2O2,故答案为:;口a2O2.
本题解析:
本题难度:一般
2、选择题 下列说法正确的是(?)
A.在离子化合物中不可能存在非极性共价键
B.在化合物中,只要有非金属原子就一定存在极性键
C.原子间通过极性键结合成分子的物质,一定是共价化合物
D.单质分子中一定含非极性键
参考答案:C
本题解析:在分析此类问题时,可采取寻找反例来否定的方法,即能举出一个反例则说明结论错误,找不出反例则论证正确。A项不正确,离子化合物中可以含有非极性共价键,如Na2O2;B项错误,离子化合物中可不含极性键,如NaCl;C项正确;稀有气体中无化学键,D错误。
本题难度:简单
3、选择题 短周期元素A、B、C、D的原子序数依次递增,它们的原子序数之和为32,且原子最外层电子数之和为10;A、C原子的最外层电子数之和等于B原子的次外层电子数;A与C,B与D均为同主族元素.下列叙述正确的是( )
A..四种元素的原子半径:A<B<C<D
B.最高价氧化物对应的水化物的酸性:B>D
C.C元素处于元素周期表中第3周期第ⅡA族
D.C的最高价氧化物对应的水化物是强酸
参考答案:A、C原子的最外层电子数之和等于B原子的次外层电子数;A与C,B与D均为同主族元素,B的次外层电子数为8,所以A、C的最外层电子数均为4,短周期元素A、B、C、D的原子序数依次递增,所以A为C,C为Si;原子最外层电子数之和为10,所以10-4-42=1,即B、D均为第ⅠA族元素,所以B为Na,它们的原子序数之和为32,32-6-14-11=1,所以D为H,不符合题意;
则B的次外层电子数应为2,A、C均为第ⅠA族元素,且原子最外层电子数之和为10,所以10-1-12=4,所以B、D均为第ⅣA族元素,原子序数依次递增,即B为C,D为Si,A为H,C为Na,
A.电子层越多,半径越大,同周期从左向右原子半径在减小,所以原子半径为C>D>B>A,故A错误;
B.非金属性C>Si,所以最高价氧化物对应的水化物的酸性:B>D,故B正确;
C.C元素为Na元素,处于元素周期表中第3周期第ⅠA族,故C错误;
D.C的最高价氧化物对应的水化物为NaOH,为强碱,故D错误;
故选B.
本题解析:
本题难度:一般
4、选择题 下列表示物质结构的化学用语或模型正确的是( )
A.8个中子的氧原子的核素符号:
O
B.HF的电子式:
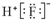
C.K+离子的结构示意图:
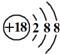
D.CH4分子的球棍模型:

参考答案:A
本题解析:
本题难度:一般
5、选择题 下列物质中,既含有离子键又含有共价键的是
[? ]
A.KOH
B.KCl
C.H2O
D.H2
参考答案:A
本题解析:
本题难度:简单