微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 在温度相同,压强分别为p1、p2条件下,A(g)+2B(g) nC(g)的反应体系中,C的体积分数(C%)随时间(t)变化的曲线如图所示.下列结论正确的是
nC(g)的反应体系中,C的体积分数(C%)随时间(t)变化的曲线如图所示.下列结论正确的是

A.p1 > p2 n < 3
B.p1< p2 n > 3
C.p1< p2n = 3
D.p1 > p2n > 3
参考答案:D
本题解析:分析题给图像知,压强为p1时达到平衡的时间短,反应速率快,结合压强对反应速率的影响规律知,p1 > p2,压强增大,C%的百分含量降低,从压强对平衡移动的影响分析,说明平衡向逆反应方向,则n>3,选D。
本题难度:一般
2、选择题 决定化学反应速率的主要因素是
[? ]
A.反应温度
B.使用催化剂
C.外界压强
D.反应物的性质
参考答案:D
本题解析:
本题难度:简单
3、选择题 下列做法,不能使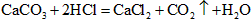 的反应速率增大的是
的反应速率增大的是
[? ]
A.增大盐酸的浓度
B.碾碎碳酸钙
C.适当加热
D.把2mol/L盐酸换成2mol/LH2SO4
参考答案:D
本题解析:
本题难度:一般
4、填空题 (I)在一定条件下,发生反应:aA(g)+bB(g) cC(g)△H="Q" kJ/mol,其化学平衡常数K和温度的关系如下表所示:
cC(g)△H="Q" kJ/mol,其化学平衡常数K和温度的关系如下表所示:

依据图表判断该反应△H?0(填“>”或“<”):若其它条件保持一定,降低温度,该反应物A的转化率?(填“增大”、“减小”或“不变”下同),化学反应速率将?。
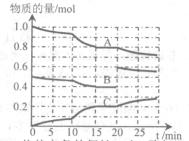
 (II)在恒定温度t℃,2L恒容密闭容器中发生反应aA(g)+bB(g)? cC(g),容器中A、B、C物质的量变化如图所示,回答下列问题:
(II)在恒定温度t℃,2L恒容密闭容器中发生反应aA(g)+bB(g)? cC(g),容器中A、B、C物质的量变化如图所示,回答下列问题:
(1)该化学方程式中a:b:c为?,t℃时该反应的化学平衡常数K的值为____?。(保留2位小数)
(2)0~15 min内,B的平均反应速率为?,反应达平衡时,A的转化率为?。
(3)据图判断,反应进行至20 min时,曲线发生变化的原因是?(用文字表达),反应重新达平衡时,A的体积分数将?(填“增大”、“减小”或“不变”)。
(4)10 min到15 min的曲线变化的原因可能是?。
参考答案:(I)<?增大?减小
(II)(1)2:1:2? 0.31?(每空2分)
(2)0.0033 mol/( L・min) 20%?(每空2分)
(3)增大了B的量(合理答案给分)减小
(4)使用了催化剂?(除标明外其余每空1分)
本题解析:(I)温度升高,化学平衡常数减小,说明升温平衡逆向移动,正向是放热反应,△H<0,降低温度平衡正向移动,反应物A的转化率增大,反应速率减小;
(II)(1)10 min时,A、B、C的物质的量的改变量分别是0.1mol、0.05mol、0.1mol,所以该化学方程式中a:b:c为2:1:2;15 min达平衡时,A、B、C的物质的量浓度分别为0.4mol/L、0.2 mol/L、0.1 mol/L,所以K=0.12/(0.42×0.2)=0.31
(2)0~15 min内,B的浓度变化是0.05mol/L,所以B的平均反应速率为0.05mol/L/15 min=0.0033 mol/( L・min),平衡时A的物质的量变化是0.2mol,所以A的转化率为0.2mol/1.0mol=20%;
(3)反应进行至20 min时,B的物质的量陡然增加,所以曲线发生变化的原因是B的物质的量增加了,平衡正向移动,所以A的体积分数将减小;
(4)10 min时反应未达平衡,A、B、C的反应速率瞬间增大,且反应仍正向进行,所以可能是加入了催化剂
本题难度:一般
5、选择题 反应4A(g)+6B(g) 4C(g)+5D(g)在2L的密闭容器中进行,1min后A气体减少了0.12mol,则平均每秒中浓度变化正确的是
4C(g)+5D(g)在2L的密闭容器中进行,1min后A气体减少了0.12mol,则平均每秒中浓度变化正确的是
A.A气体:0.05mol・L-1・min-1
B. B气体:0.075mol・L-1・min-1
C.C气体:0.04mol・L-1・min-1
D.D气体:0.075mol・L-1・min-1
参考答案:D
本题解析:略
本题难度:简单