微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 将31.2 g过氧化钠和100 g水充分反应后所得溶液的质量分数为(?)
A.25.6%
B.31.2%
C.32.0%
D.34.5%
参考答案:A
本题解析:过氧化钠溶于水生成氢氧化钠溶液,故所求溶液的溶质为NaOH。
2Na2O2+2H2O====4NaOH+O2↑
2×78? 4×40? 32
31.2 g? x? y
x=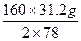 ="32" g(NaOH)
="32" g(NaOH)
y=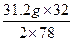 ="6.4" g(O2)
="6.4" g(O2)
w(NaOH)=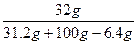 ×100%=25.6%
×100%=25.6%
本题难度:简单
2、选择题 关于Na2CO3和NaHCO3性质的说法正确的是
A.热稳定性:NaHCO3 <Na2CO3
B.与Ca(OH)2溶液反应:Na2CO3溶液中有白色沉淀生成,NaHCO3溶液中没有沉淀生成
C.相同温度时,在水中的溶解性:NaHCO3>Na2CO3
D.相同物质的量浓度时,溶液的导电能力:NaHCO3>Na2CO3
参考答案:A
本题解析:
正确答案:A
A.正确,热稳定性酸式盐通常小于正盐:NaHCO3 <Na2CO3
B.不正确,与Ca(OH)2溶液反应:Na2CO3、NaHCO3溶液中均有白色沉淀生成
C.不正确,相同温度时,在水中的溶解性:NaHCO3<Na2CO3
D.不正确,相同物质的量浓度时,溶液的导电能力:NaHCO3<Na2CO3,因为在水中的溶解性:NaHCO3<Na2CO3,NaHCO3溶液中离子浓度小,导电能力差。
本题难度:一般
3、填空题 (6分)完成下列各小题中的化学反应方程式。
⑴碱金属与O2反应生成氧化物较复杂,有普通氧化物(如Na2O)过氧化物(如Na2O2)还有超氧化物和臭氧化物等。因此要制备碱金属的普通氧化物一般是用碱金属还原对应的过氧化物、硝酸盐或亚硝酸盐。试用化学方程式表示以下反应:
①钠与过氧化钠反应?。②钾还原硝酸钾还产生了一种单质气体?。
⑵将Al(OH)3和Na2CO3的混和物一同 溶于氢氟酸可制得电解法炼铝必需的熔剂冰晶石(Na3AlF6),同时反应中产生一种无色无味的气体,试写出有关化学方程式_________。
溶于氢氟酸可制得电解法炼铝必需的熔剂冰晶石(Na3AlF6),同时反应中产生一种无色无味的气体,试写出有关化学方程式_________。
参考答案:(6分)⑴①Na2O2+2Na=2Na2O?
②2KNO3+10K=6K2O+N2?
⑵2Al(OH)3+12HF+3Na2CO3=2Na3AlF6+3CO2?+9H2O?(2,2,2)
本题解析:略
本题难度:一般
4、填空题 取等物质量浓度的NaOH溶液两份,每份为50ml。向其中通入一定量的CO2,随后分别取溶液10ml,将其稀释成100ml,并分别向稀释后的溶液中逐滴加入0.1mol/L的HCI溶液,产CO2的体积(标准状况)与加入盐酸体积之间的关系如图所示(设分别为A、B两种情况)。
 回答下列问题:
回答下列问题:
 ?(1)在(A)情况下,溶质为(写化学式)?,其物质的量之比为?,在标准状况下,通人CO2气体的体积为? ?。
?(1)在(A)情况下,溶质为(写化学式)?,其物质的量之比为?,在标准状况下,通人CO2气体的体积为? ?。
 ?(2)在(B)情况下,溶质为(写化学式)?,其物质的量之比为?,在标准状况下,通人CO2气体的体积为? ?。
?(2)在(B)情况下,溶质为(写化学式)?,其物质的量之比为?,在标准状况下,通人CO2气体的体积为? ?。
 ?(3)原NaOH溶液的物质的量浓度为? ?。
?(3)原NaOH溶液的物质的量浓度为? ?。
参考答案:①NaOH、Na2CO3







 ?3:1 ?33.6
?3:1 ?33.6
②Na2CO3、NaHCO3?1:1 ?112
③ 0.75mol/L
本题解析:根据题意和图像综合分析,在(A)情况下,溶质为NaOH、Na2CO3在(B)情况下,溶质为Na2CO3、NaHCO3
本题难度:简单
5、选择题 下列各组中两种物质作用时,反应条件或反应物用量改变,对生成物没有影响的是
?[? ]
A.Na与O2
B.Na2O2与CO2
C.NaOH与CO2
D.C与O2
参考答案:B
本题解析:
本题难度:简单