微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
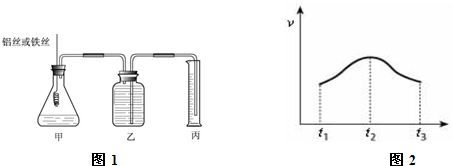
1、简答题 某研究小组为比较Al和Fe的金属性强弱,设计了图1所示的装置,甲中锥形瓶内盛放的是100ml稀盐酸(反应前后溶液体积变化可以忽略不计).
(1)若要比较产生气体的快慢有两种方法,一种是比较产生相同体积气体所需的时间,另一种是比较______.
(2)为了确保“Al和Fe的金属活动性不同是导致产生气体速率不同的唯一原因”,实验时需要控制好反应条件.实验时除需保证甲中液体的体积、物质的量浓度和温度相同外,还需保证______.
(3)实验测得产生气体的速率(v)与时间(t)的关系如图2所示,则t1~t2时间内速率逐渐加快说明该反应是______(填放热或吸热)反应,t2~t3时间内速率逐渐减慢的主要原因是______.
(4)能使甲中的反应停止的操作是______.
参考答案:(1)由v=△V△t知,反应速率与气体的体积和时间有关,所以一种是固定体积比较时间,另一种是固定时间比较体积.
故答案为:相同时间内产生气体体积大小;
(2)影响化学反应速率的因素有反应物的浓度、溶液的温度、固体的表面积等,所以还需保证Al和Fe表面积相同.
故答案为:Al和Fe表面积相同;
(3)该反应是一个放热的反应,随着反应的进行,放出的热量越多,溶液的温度越高,温度越高反应速率越大;随着反应的进行,溶液中盐酸的浓度不断减小,浓度越小反应速率越小.
故答案为:放热;盐酸浓度不断减小;
(4)要想使反应停止,没有反应物即可,所以将铁丝或铝丝从溶液中拔出即可停止反应.
故答案为:铁丝或铝丝从溶液中拔出.
本题解析:
本题难度:一般
2、简答题 在20℃时某化学反应的速率为0.15mol?L-1?s-1,若温度每升高10℃,反应速率提高到原来的3倍,则为使反应速率达到1.35mol?L-1?s-1,应使反应在什么温度下进行( )
A.30℃
B.35℃
C.40℃
D.45℃
参考答案:令温度提高n个10℃,则:
3n×0.15mol?L-1?s-1=1.35mol?L-1?s-1
解得n=2,
所以后来的温度为20℃+2×10℃=40℃
故选C.
本题解析:
本题难度:一般
3、选择题 一定条件下进行反应:A(g) B(g)+C (g),向2.0 L恒容密闭容器中充入1.0 mol A(g),经过一段时间后达到平衡。反应过程中测得的有关数据见下表:
B(g)+C (g),向2.0 L恒容密闭容器中充入1.0 mol A(g),经过一段时间后达到平衡。反应过程中测得的有关数据见下表:
t/s
| 0
| 2
| 4
| 6
| 8
|
n(B)/mol
| 0
| 0.30
| 0.39
| 0.40
| 0.40
|
下列说法正确的是
A.反应前2min的平均速率v(B)="0.15" mol/(L・min)
B.保持其他条件不变,升高温度,平衡时c(B)="0.22" mol・L-1,则反应的ΔH < 0
C.保持其他条件不变,起始向容器中充入2.0 mol A,反应达到平衡时C的体积分数减小
D.保持其他条件不变,起始向容器中充入1.2 mol A、0.60 mol B和0.60 mol C,反应达到平衡前的速率:v(正)<v(逆)
参考答案:CD
本题解析:A、反应前2min的平均速率v(B)="0.30mol/2.0L/2min=0.075" mol/(L・min),错误;B、原平衡时,c(B)="0.40mol/2.0L=0.2" mol・L-1,保持其他条件不变,升高温度,平衡时c(B)="0.22" mol・L-1>0.20mol/L,说明升高温度,平衡正向移动,则该反应是吸热反应,ΔH >0,错误;C、保持其他条件不变,起始向容器中充入2.0 mol A,臂原平衡时物质的浓度增大,相当于缩小容器的体积,增大压强,则平衡逆向移动,反应达到平衡时C的体积分数减小,正确;D、根据表中数据可计算该温度时的平衡常数是0.4/3,保持其他条件不变,起始向容器中充入1.2 mol A、0.60 mol B和0.60 mol C,则Qc=0.32/0.6=0.15>0.4/3,则反应逆向进行,所以反应达到平衡前的速率:v(正)<v(逆),正确,答案选CD。
考点:考查反应速率的计算,平衡移动的判断,化学平衡常数的应用
本题难度:一般
4、选择题 对于某容器中一定条件下进行的反应N2+3 H2 2NH3,能增大化学反应速率的措施是?
2NH3,能增大化学反应速率的措施是?
[? ]
A.保持其他条件不变,恒压下,通入3 mol Ne
B.保持其他条件不变,压缩容器体积使压强增大到原来的2倍
C.保持其他条件不变,恒容下,通入Ar使压强增大到原来的2倍
D.保持其他条件不变,将容器的体积扩大一倍
参考答案:B
本题解析:
本题难度:一般
5、实验题 (12分)影响化学反应速率的因素很多,某课外兴趣小组用实验的方法进行探究。他们利用Cu、Fe、Mg和不同浓度的硫酸(0.5mol/L、2mol/L、18.4mol/L),设计实验方案来研究影响反应速率的因素。
(1)甲同学研究的实验报告如下表:
①分别取等体积的2 mol/L
硫酸于试管中;
②分别投入大小、 形状相同 形状相同
的Cu、Fe、Mg。
| 反应快慢:
Mg>Fe>Cu
| 反应物的性质越活泼,反应速率越快。
|
?
该同学的实验目的是研究?? ??对化学反应速率的影响;根据控制变量法,要得出正确的实验结论,还需控制的实验条件是保持
??对化学反应速率的影响;根据控制变量法,要得出正确的实验结论,还需控制的实验条件是保持 ?条件相同。
?条件相同。
(2)乙同学为了更精确地研究浓度对反应速率的影响,利用右图装置进行定量实验。
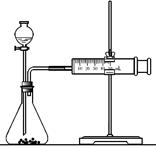
完成该实验应选用的实验药品是?
?;应该测定的实验数据是?。
参考答案:(共12分)
(1)反应物本身的性质;温度;(每空2分)
(2)Mg(或Fe)、0.5mol/L硫酸和2mol/L硫酸;(6分)
测定一定时间产生气体的体积(或者测定一定体积的气体所需时间);(2分)
本题解析:略
本题难度:一般