微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 把镁带投入盛有盐酸的敞口容器里,在下列因素中:①盐酸的浓度②镁带的表面积?③溶液的温度?④氯离子的浓度.对反应速率有影响的是( )
A.①②
B.③④
C.①②③④
D.①②③
参考答案:镁和盐酸反应的实质为:Mg+2H+=Mg2++H2↑,从方程式可知影响因素为镁带的表面积和H+的浓度,另外,温度对反应速率有较大的影响,而氯离子没有参加反应,对反应速率没有影响.
故选D.
本题解析:
本题难度:一般
2、选择题 关于化学反应速率的影响因素的说法中不正确的是
[? ]
A.改变压强,若不能引起浓度的变化,反应速率就不会受影响
B.决定化学反应速率快慢的主要因素是反应物的性质
C.任何一种加快反应速率的因素都是由于增加了活化分子的百分数
D.反应速率加快的原因是有效碰撞次数增多
参考答案:C
本题解析:
本题难度:一般
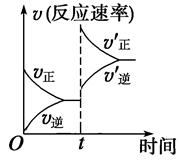
3、选择题 一定条件下,可逆反应C(s)+CO2(g)  ?2CO(g)? ΔH>0,达到平衡状态,现进行如下操作:①升高反应体系的温度;②增加反应物C的用量;③缩小反应体系的体积;④减小体系中CO的量。上述措施中一定能使反应的正反应速率显著加快的是?(?)
?2CO(g)? ΔH>0,达到平衡状态,现进行如下操作:①升高反应体系的温度;②增加反应物C的用量;③缩小反应体系的体积;④减小体系中CO的量。上述措施中一定能使反应的正反应速率显著加快的是?(?)
A.①②③④
B.①③
C.①②
D.①③④
参考答案:B
本题解析:①升高体系温度、③增大体系压强均能加速反应速率;②C为固体,不会影响反应速率;④减少CO的量会减小反应速率。
本题难度:一般
4、实验题 硫代硫酸钠(Na2S2O3)俗称大苏打,照相业中用作定影剂。Na2S2O3易溶于水,在酸性溶液中与酸反应有单质硫和SO2生成。
(1)Na2S2O3溶液与稀硫酸混合反应可用于探究外界条件对反应速率的影响,完成有关的实验设计表(已知各溶液体积均为5 mL):
实验编号
| T/K
| c(Na2S2O3)/ mol・L-1
| c(H2SO4)/ mol・L-1
| 实验目的
|
①
| 298
| 0.1
| 0.1
| 实验①和②探究温度对该反应速率的影响;
实验①和③探究反应物浓度对该反应速率的影响
|
②
| 308
| ?
| ?
|
③
| ?
| 0.2
| ?
|
(2)Na2S2O3还具有很强的还原性,Na2S2O3溶液与足量氯水反应的化学方程式为:
________??(提示:S元素被氧化为SO42-)。
(3)现有一瓶Na2S2O3固体,可能含有Na2SO4固体,请设计实验验证,写出实验步骤、预期现象和结论。限选试剂:1 mol・L-1 H2SO4、1 mol・L-1 HNO3、1 mol・L-1 HCl、1 mol・L-1 NaOH、0.1 mol・L-1 Ba(NO3)2、0.1 mol・L-1 BaCl2、0.01 mol・L-1 KMnO4、蒸馏水。
实验步骤
| 预期现象和结论
|
步骤1:取少量固体于试管A中,加蒸馏水溶解。
| ?
|
步骤2:向试管A加入?
?
| ?
?
|
步骤3:取步骤2的少量上层清液于试管B中,??
?
| ?
?
|
?
参考答案:(1)表格内每空1分,共4分
实验编号
T/K
c(Na2S2O3)/
mol・L-1
c(H2SO4)/
mol・L-1
①
?
?
?
②
?
0.1
0.1
③
298
?
0.1
(2) Na2S2O3+4Cl2+5H2O = Na2SO4+8HCl+H2SO4(2分,未配平给1分)(或Na2S2O3+4Cl2+5H2O = 2NaCl+6HCl+2H2SO4)
(3)
实验步骤
预期现象和结论
步骤1:取少量固体于试管中,加蒸馏水溶解
?
步骤2:向试管中加入过量1 mol・L-1 HCl溶液,充分振荡,静置(2分)
有淡黄色沉淀生成(2分)
步骤3:取上层清液于另一试管中,滴加少量0.1 mol・L-1BaCl2溶液(2分)
有白色沉淀生成,证明固体中混有Na2SO4(2分)
[或无白色沉淀生成,证明固体中无Na2SO4]
?
步骤2:步骤与现象、结论不株连。未写“过量”扣1分;缺少“充分振荡”扣一分。现象和结论中:刺激性气味气体或气泡产生可给分。
步骤3:无“少量”不扣分,将BaCl2写成Ba(NO3)2的不得分,不株连现象和结论
本题解析:(1)探究影响化学反应速率的因素时,每次只能改变一个条件,①和②温度不同,浓度应该相同,①和③改变了Na2S2O3的浓度,其他条件相同;(2)发生氧化还原反应,结合电子守恒配平;(3)
实验步骤
预期现象和结论
步骤1:取少量固体于试管中,加蒸馏水溶解
?
步骤2:向试管中加入过量1 mol・L-1 HCl溶液,充分振荡,静置(2分)
有淡黄色沉淀生成(2分)
步骤3:取上层清液于另一试管中,滴加少量0.1 mol・L-1BaCl2溶液(2分)
有白色沉淀生成,证明固体中混有Na2SO4(2分)
[或无白色沉淀生成,证明固体中无Na2SO4]
本题难度:一般
5、选择题 下列说法错误的是(?)
A.固体颗粒大小也会影响反应速率
B.温度越高反应速率也越大
C.加入催化剂一定能加快反应速率
D.反应速率主要由反应物性质决定
参考答案:C
本题解析:反应物的接触面积越大,反应速率越快,则A正确;升高温度,反应速率一定加快,B正确;催化剂一定能改变反应速率,但不一定是加快,也可能是降低反应速率,C不正确;影响反应速率的主要因素是反应物自身的性质,D正确,答案选C。
点评:该题是基础性试题的考查,随意考查学生对影响反应速率因素的熟悉掌握程度,有利于调动学生的学习兴趣,也有利于培养学生灵活运用基础知识解决实际问题的能力。
本题难度:简单