微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 在一定温度下的定容的容器中,当下列哪些物理量不再发生变化时,表明反应A(g)+2B(g)═C(g)+D(g)已达到平衡状态的是( )
①混合气体的压强?②混合气体的密度?③B的物质的量浓度? ④混合气体总物质的量? ⑤混合气体的平均相对分子质量?
⑥速率关系:v(C)与v(D)的比值? ⑦混合气体总质量? ⑧混合气体总体积.
A.①②③④⑤⑥⑦⑧
B.①③④⑤
C.①②③④⑤⑦
D.①③④⑤⑥
参考答案:①该反应为反应前后气体的物质的量减小的反应,容器体积不变,随反应进行压强降低,当压强不再变化,说明到达平衡,故①正确;
②反应混合物都是气体,总质量不变,容器体积不变,密度自始至终都不变,不能说明到达平衡状态,故②错误;
③随反应进行B的浓度减小,当B的物质的量浓度不再变化,说明到达平衡,故③正确;
④该反应为反应前后气体的物质的量减小的反应,随反应进行混合气体总物质的量减小,混合气体总物质的量不再变化,说明到达平衡,故④正确;
⑤反应混合物都是气体,总质量不变,随反应进行混合气体总物质的量减小,所以随反应进行混合气体的平均相对分子质量增大,当混合气体的平均相对分子质量不再变化,说明到达平衡,故⑤正确;
⑥v(C)与v(D)的速率关系自始至终都是1:1,不能说明到达平衡,故⑥错误;
⑦反应混合物都是气体,混合气体总质量不发生变化,不能说明到达平衡,故⑦错误;
⑧容器的体积不变,混合气体总体积不变,不能说明到达平衡,故⑧错误.
故①③④⑤正确.
故选:B.
本题解析:
本题难度:简单
2、选择题 恒温恒容条件下,下列叙述正确的是( )
A.甲、乙两容器中分别加入1gSO2、1gO2与2gSO2、2gO2,反应2SO2(g)+O2(g)

2SO3(g)达到平衡,SO2的转化率前者大
B.反应2HI(g)

H2(g)+I2(g)达平衡,增大HI的物质的量,平衡不移动
C.反应2HI(g)

H2(g)+I2(g)达平衡,增大HI的物质的量,HI分解率不变,体积分数不变
D.反应2NO2(g)

N2O4(g)达到平衡时,再向容器内通入一定量的NO2(g),重新达到平衡后,与第一次平衡时相比,NO2的体积分数增大
参考答案:C
本题解析:
本题难度:一般
3、选择题 工业上采用乙烯和水蒸气合成乙醇的原理为:CH2=CH2(g) + H2O(g)  CH3CH2OH(g)。下图是乙烯的转化率随温度、压强的变化关系,下列说法正确的是( ?)
CH3CH2OH(g)。下图是乙烯的转化率随温度、压强的变化关系,下列说法正确的是( ?)
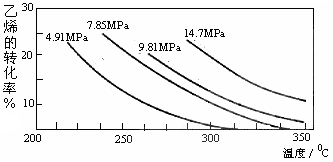
A.该反应为吸热反应
B.工业上采用7MPa左右,250~300℃,是综合考虑反应速率和乙醇的产率等因素的结果
C.相同温度下,压强越大,乙烯的转化率越大,平衡常数越大
D.给予足够的压强和适当的温度,可实现乙烯的转化率为 100%
参考答案:B
本题解析:A、温度升高、转化率降低,平衡逆向移动,逆向吸热,正向放热;B、正确;C、平衡常数只与温度有关,相同温度下,为定值;D、该反应为可逆反应,有一定限度,转化率不可能为100%。
本题难度:一般
4、选择题 对于反应2A(g)+B(g) 2C(g) ΔH<0,下图图象正确的是
2C(g) ΔH<0,下图图象正确的是
参考答案:D
本题解析:略
本题难度:一般
5、填空题 (16分)下图是煤化工产业链的一部分,试运用所学知识,解决下列问题:
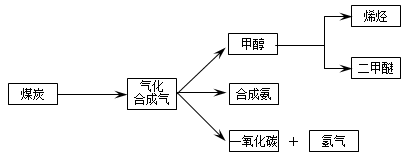
I.已知该产业链中某反应的平衡表达式为:K= ,它所对应反应的化学方程式为 。
,它所对应反应的化学方程式为 。
II.二甲醚(CH3OCH3)在未来可能替代柴油和液化气作为洁净液体燃料使用.工业上以CO和H2为原料生产CH3OCH3。工业制备二甲醚在催化反应室中(压力2.0~10.0Mpa, 温度230~280℃)进行下列反应:
温度230~280℃)进行下列反应:
①CO(g)+2H2(g) CH3OH(g) △H1=-90.7kJ·mol-1
CH3OH(g) △H1=-90.7kJ·mol-1
②2CH3OH(g) CH3OCH3(g) +H2O(g) △H2=-23.5kJ·mol-1
CH3OCH3(g) +H2O(g) △H2=-23.5kJ·mol-1
③CO(g)+H2O(g) CO2(g)+H2(g) △H3=-41.2kJ·mol-1
CO2(g)+H2(g) △H3=-41.2kJ·mol-1
(1)催化反应室中总反应的热化学方程式为 。830℃时反应③的K=1.0,则在催化反应室中反应③的K 1.0(填“>”、“<”或“=”)。
(2)在某温度下,若反应①的起始浓度分别为:c(CO)=1 mol/L,c(H2)=2.4 mol/L,5 min后达到平衡,CO的转化率为50%,则5 min内CO的平均反应速率为 ;若反应物的起始浓度分别为:c(CO)=4 mol/L,c(H2)=a mol/L;达到平衡后,c(CH3OH)=2 mol/L,a= mol/L。
(3)为了寻找合适的反应温度,研究者进行了一系列试验,每次试验保持原料气组成、压强、反应时间等因素不变,试验结果如图.CO转化率随温度变化的规律是 ,其原因是 .

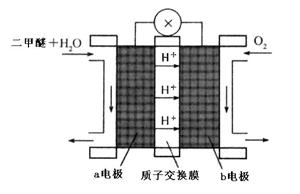
(4)“二甲醚燃料电池”是一种绿色电源,其工作原理如图所示。写出a电极上发生的电极反应式  。
。
参考答案:C(s)+H2O(g)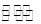 CO(g)+H2(g)(2分)
CO(g)+H2(g)(2分)
(1)3CO(g)+3H2(g) CH3OCH3(g)+CO2(g) ΔH=-246.1 kJ·mol-1(2分);
CH3OCH3(g)+CO2(g) ΔH=-246.1 kJ·mol-1(2分);
>(2分)
(2)0.1mol/(L·min) (2分);5.4 (2分)
(3)温度低于240℃时,CO的转化率随着温度的升高而增大;温度高于240℃时,CO的转化率随着温度的升高而减小。(2分)
在较低温时,各反应体系均未达到平衡,CO的转化率主要受反应速率影响,随着温度的升高反应率增大,CO的转化率也增大;在较高温时,各反应体系均已达到平衡,CO的转化率主要受反应限度影响,随着温度的升高平衡向逆反应方向移动,CO的转化率减小。(2分)
(4)CH3OCH3+3H2O-12e-=2CO2+12H+(2分)
本题解析:略
本题难度:困难