| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高中化学知识点总结《化学反应与能量》在线测试(2017年最新版)(二)
参考答案:C 本题解析:略 本题难度:一般 2、选择题 甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是 |
参考答案:D
本题解析:A、若用甲醇(CH3OH)为原料设计成燃料电池,甲醇发生氧化反应,则通入甲醇的一极是负极,错误;B、反应①是吸热反应,反应物的总能量低于生成物的总能量,错误;C、若以②的方式甲醇转化为氢气,则该过程放热,错误;D、液态甲醇转化为气态甲醇需要吸收热量,所以液态甲醇完全燃烧放出的热量低于气态甲醇放出的热量,ΔH<0,则ΔH>-192.9 kJ・mol-1,正确,答案选D。
考点:考查化学反应的热效应的判断,电化学原理的应用
本题难度:一般
3、选择题 下列元素的原子在形成不同物质时,既能形成离子键,又能形成共价键的是( )
A.K
B.Ca
C.I
D.Ne
参考答案:A、K是活泼金属,所以钾元素在形成不同物质时,只能形成离子键,故A错误;
B、钙是活泼金属,所以钙元素在形成不同物质时,只能形成离子键,故B错误;
C、碘在形成不同物质时,和活泼金属能形成离子键,如NaI;和非金属易形成共价键,如HI,所以碘在形成不同物质时,既能形成离子键,又能形成共价键,故C正确;
D、Ne是稀有气体,性质较稳定,一般不和其它物质发生化学反应,故D错误;
故选C.
本题解析:
本题难度:一般
4、选择题 以下分子或离子的结构为正四面体且键与键之间夹角为109°28′的是( )
①CH4? ? ②NH4+? ③CH3Cl? ④P4 ? ⑤金刚石
A.①②④
B.①②③④⑤
C.①②
D.①②⑤
参考答案:D
本题解析:①CH4分子中C原子是sp3型杂化,杂化轨道全部用于成键,碳原子连接4个相同的原子,为正四面体构型,键角是109°28′;②NH4+离子中N原子形成成4个σ键,N原子是sp3型杂化,杂化轨道全部用于成键,N原子连接4个相同的原子,为正四面体构型,键角是109°28′;③CH3Cl分子中C原子是sp3型杂化,杂化轨道全部用于成键,但C原子连接的4个原子不完全相同,为四面体构型,但不是正四面体;④P4?分子中4个P原子位于正四面体4个的顶点上,P4?分子的空间构型是正四面体构型,但键角是60°;⑤金刚石中C原子是sp3型杂化,形成4个σ键,C原子连接4个相同的原子,为正四面体构型,键角是109°28′,所以正确的答案选D。
点评:该题是高考中的常见题型,属于中等难度的试题,题目难度不。该题的关键是掌握价层电子对互斥理论与杂化轨道理论,注意P4(白磷)分子的键角为60°而不是109°28′。
本题难度:一般
5、选择题 白磷与氧气可发生如下反应:P4 +5O2=P4O10。已知断裂下列化学键需要吸收的能量分别为:P-P
akJ・mol-1、P-O b kJ・mol-1、P=O c kJ・mol-1、 O=O d kJ・mol-1。 根据下图所示的分子结构和有关数据估算该反应的△H,其中正确的是?
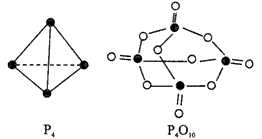
[? ]
参考答案:A
本题解析:
本题难度:一般
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学必考知识点《分子式、结.. | |