��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��10�֣��ȼҵ��ԭ�ϱ���ʳ��ˮ�к���һ������笠����ӣ��ڵ��ʱ���������ʼ����ȶ������Ȼ�������������ը��
��1�����Ȼ�����ˮ�⣬��ˮ��������������ɰ����⣬��һ����Ϊ? ��?��
��2��Ϊ��ȥ����ʳ��ˮ�е�笠����ӣ����ڼ���������ͨ����������Ӧ���ɵ������÷�Ӧ�����ӷ���ʽΪ? ��?���ù���ѡ���������ŵ���? ��?������һ�㼴�ɣ�
��3������������Na2S2O3��ȥ����Ӧ��S2O32-������ΪSO42-��������������Ϊ10-3 mol/L�������������ɵ�SO42-Ϊ? ��?mol/L��
��4��������ʵ���й㷺���ü�ȩ���ⶨ��Ʒ�ĺ���������ȩ��笠����ӵķ�Ӧ���£�
4NH4+ + 6HCHO ����CH2)6N4H+��һԪ�ᣩ+ 3H+ + 6H2O
ʵ�鲽�����£�
�ټ�ȩ�г����������ᣬӦ�ȳ�ȥ����ȡ��ȩb mL����ƿ������1�η�̪����Ũ��ΪC mol/L��NaOH��Һ�кͣ��ζ��ܵij�ʼ����V1 mL������Һ����ɫʱ���ζ��ܵĶ���V2 mL��
�������м��뱥��ʳ��ˮ����a mL������1���ӡ�
���ټ�1~2�η�̪����������NaOH��Һ�ζ�����ɫ���ζ��ܵĶ���V3 mL��
��ʳ��ˮ�еĺ�����Ϊ? ��?mg/L��
�ο��𰸣���1��HClO ��2�֣�
��2��3Cl2 + 2NH4++ 8OH- = N2�� + 6Cl- + 8H2O����2�֣�
�����ȼҵ�IJ�Ʒ����Ϊԭ�ϣ��ͽ�ȡ�ģ������������������ӡ���2�֣�
��3��5��10-4��2�֣�
��4��14000C(V3��V2)/a mg/L ��2�֣�
�����������
�����Ѷȣ�һ��
2��ѡ���� �������з�Ӧ�Ʊ������е����ʣ����������ǣ�������
A����ϩ�������ӳɣ�1��2-�������飩
B����ϩ��ˮ�ӳɣ��Ҵ���
C�������ʵ����������������ڹ��������·�Ӧ�������飩
D�������뱽���Ȼ�����������Ӧ���ȱ���
�ο��𰸣�A����ϩ�����������ӳɷ�Ӧ�������͵�C=C˫���Цм����ѣ�������̼ԭ��������ԭ�ӣ�����1��2-�������飬��A��ȷ��
B����ϩ��ˮ�����ӳɷ�Ӧ�������͵�C=C˫���Цм����ѣ�������̼ԭ������ˮ�ṩ��-H��-OH�������Ҵ�����B��ȷ��
C�������������ڹ����·�����ӦΪ��ʽ��Ӧ�������ʵ��������������鷴Ӧ�������ȴ����鶼������������ֻ���������飬�������������ϩ���Ȼ��ⷢ���ӳɷ�Ӧ�Ʊ�����C����
D�����Ȼ��������������뱽����ȡ����Ӧ�����ȱ�����D��ȷ��
��ѡ��C��
���������
�����Ѷȣ���
3��ʵ���� ��14�֣�ijѧϰС��������ͼװ�òⶨ��þ�Ͻ������������������������ԭ��������
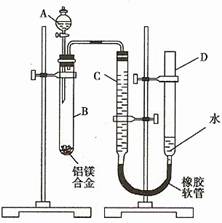
��1��A���Լ�Ϊ_______________________��
��2��ʵ��ǰ���Ƚ���þ�Ͻ���ϡ�����н���Ƭ�̣���Ŀ����_____________________��
��3����������ԣ���ҩƷ��ˮװ��������У����Ӻ�װ�ú�
����еIJ������У��ټ�¼C��Һ��λ�ã��ڽ�B��ʣ�������ˡ�ϴ�ӡ�������أ��۴�B�в���������������ָ������º�¼C��Һ��λ�ã�����A��B�еμ������Լ����ݼ�������ԡ�����������˳����_______________________________������ţ�����¼C��Һ��λ��ʱ��������ƽ���⣬��Ӧ_________________________��
��4��B�з�����Ӧ�Ļ�ѧ����ʽΪ_________________________________________��
��5����ʵ������þ�Ͻ������Ϊa g ������������Ϊb mL ���ѻ���Ϊ��״������B��ʣ���������Ϊc g�����������ԭ������Ϊ____________________��
��6��ʵ������У���δϴ�ӹ������õIJ����������������������___________________���ƫ����ƫС����������Ӱ�족����
�ο��𰸣�

�����������
�����Ѷȣ���
4��ʵ���� ��8�֣����������䡢��ˮ��Ӧ��������ˮ������Ӧ������ͼ��ʾ����װ�õ�Ӳ�ʲ������ڷ��뻹ԭ���ۺ�ʯ���Ļ���ͨ��ˮ���������ȣ��Ϳ�����ɸ����¡�Fe��ˮ������Ӧ��ʵ�顱��
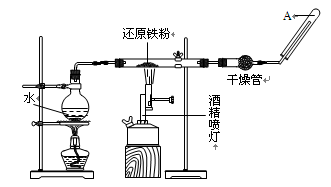
��ش��������⣺
��1��д����Ӧ�Ļ�ѧ����ʽ��?��
��2��ʵ�鿪ʼʱ��Ӧ�ȵ�ȼ?����д���ƾ��ơ��ƾ���ơ�������
��3���������ʢװ�����ʿ�����?����дһ�ּ��ɣ�����������A�ķ�����
?��
�ο��𰸣�1��3Fe+4H2O(g) Fe3O4+4H2��2���ƾ���?
Fe3O4+4H2��2���ƾ���?
��3��CaCl2�����ʯ�ҡ����������ȣ�����ȼ���巢������ɫ���棬�ڻ����Ϸ���һ�������С�ձ����ձ��ڳ���Сˮ�顣
�����������1���ڸ����£�����ˮ������Ӧ������������������������3Fe+4H2O(g)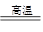 Fe 3O4 +4H2
Fe 3O4 +4H2
��2��װ���к��п���������Ϊ��ֹ������������������Ҫ����ˮ�����ų������������ȵ�ȼ�ƾ��ơ�ͬ��ʵ�����ʱӦ��Ϩ��ƾ���ơ�
��3������������ͨ����ȼ�ķ������е���ɫ������֣����ڻ����Ϸ���һ�������С�ձ����ܹ۲쵽�ձ��ڳ���Сˮ��
�����Ѷȣ���
5������� ���Ȼ��ѣ�TiCl4������ȡ���캽�չ�ҵ����--�ѺϽ����Ҫԭ�ϣ�����������Ҫ�ɷ���FeTiO3���Ʊ�TiCl4�Ȳ�Ʒ��һ�ֹ�������ʾ�����£�
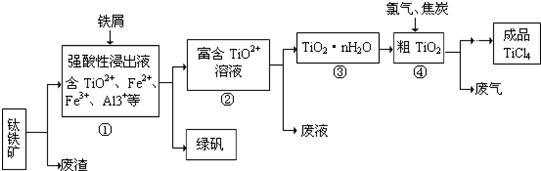
�ش��������⣺
��1�������м�����м������Һ����ɫ����ʱ��Һ�Գ�ǿ���ԣ��ù����������·�Ӧ������
2Fe3++Fe�T3Fe2+
2TiO2+����ɫ��+Fe+4H+�T2Ti3+����ɫ��+Fe2++2H2O
Ti3+����ɫ��+Fe3++H2O�TTiO2+����ɫ��+Fe2++2H+
�������������______��
��2���ڢڡ��۹�������Ҫ�����������γ�TiO2?n?H2O�ܽ����÷�ɢ�ʿ���ֱ����С��______��Χ��
��3���������վ��гɱ��͡����õ�Ʒλ����Ϊԭ�ϵ��ŵ㣮������ɫ��ѧ����ù��������д��ڵIJ���֮����______��ֻҪ��д��һ���
��4�������±���Ϣ��Ҫ���ƺ�����SiCl4���ʵ�TiCl4���ɲ���______������
| TiCl4 | SiCl4
�۵�/��
-25.0
-68.8
�е�/��
136.4
57.6
�ο��𰸣���1�������м�����м������Һ����ɫ��˵������Һ�к���Ti3+���ɷ���ʽ��֪��Fe3+����ΪTi3+��������м����ԭ������Fe3+��ԭΪFe2+����ֹTi3+��Fe3+������TiO2+��
�ʴ�Ϊ����ֹTi3+��Fe3+������TiO2+��
��2�������������γ�TiO2?n?H2O�ܽ���˵���õ����壬���ɢ�ʿ���ֱ����СΪ10-9��10-7m����1nm-100nm����
�ʴ�Ϊ��10-9��10-7m����1nm-100nm����
��3���ɹ������̿�֪�������в�����������Һ�������ȣ���������ɫ��ѧ���
�ʴ�Ϊ�������˷�������Һ�������ȣ�
��4���ɱ������ݿ�֪��SiCl4��TiCl4ΪҺ�壬���߷е����ϴ�Ҫ���ƺ�����SiCl4���ʵ�TiCl4���ɲ��������������
�ʴ�Ϊ���������
���������
�����Ѷȣ�һ��
|