微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列各元素中,一定属于主族元素的是
[? ]
A.X元素能形成+7价的含氧酸及其盐
B.Y元素原子最外层电子数为2
C.Z元素的阴离子与同一周期稀有气体元素的原子电子层结构相同
D.R元素的最高价氧化物是酸性氧化物
参考答案:C
本题解析:
本题难度:简单
2、填空题 按要求填空:
(1)某阴离子核外18电子,带两个单位负电荷,其离子结构示意图__________。
(2)含6个质子、8个中子的原子符号为__________,它与16O形成3原子分子甲,4.6克甲的物质的量是________mol,甲分子中相邻原子间以?_______键结合(填“离子键”或“共价键”)。
(3)铁原子核外有4个电子层,在周期表第8列,它在元素周期表的第____周期____族。
(4)盛放碱液的试剂瓶不能用玻璃塞,是为了防止发生__________反应(以NaOH为例用化学方程式表示),避免瓶塞与瓶口粘在一起。
参考答案:(1)“略”
(2)146C;0.1;共价键?
(3)四;第Ⅷ
(4)SiO2?+?2NaOH?=Na2CO3+H2O
本题解析:
本题难度:一般
3、推断题 A、B、C是中学化学中常见的三种短周期元素。已知:
①A元素原子最外层电子数是次外层电子数的2倍;
②B元素最高正价与最低负价的代数和为2;
③C元素有多种化合价,且常温下C元素的单质与某种一元强碱溶液反应,可得到两种含C元素的化合物;
④B、C两种元素质子数之和是A元素质子数的4倍。
(1)写出A元素在周期表中的位置_______________________。
(2)写出C的单质和强碱溶液反应的离子方程式________________________________。
(3)意大利罗马大学的FuNvio?Cacace等人获得了极具理论研究意义的B4气态分子。C4分子结构与白磷分子结构相似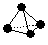 ,已知断裂1?mol?B―B吸收167?kJ的热量,生成1?mol?B≡B放出942?kJ热量。试写出由C4气态分子变成C2气态分子的热化学方程式:____________________________。
,已知断裂1?mol?B―B吸收167?kJ的热量,生成1?mol?B≡B放出942?kJ热量。试写出由C4气态分子变成C2气态分子的热化学方程式:____________________________。
(4)由B、C两种元素组成的化合物X,常温下为易挥发的淡黄色液体,X分子为三角锥形分子,且分子里B、C两种原子最外层均达到8个电子的稳定结构。X遇水蒸气可形成一种常见的漂白性物质。则X的结构式为____________,X与水反应的化学方程式是___________________。
(5)A、B两种元素可形成一种硬度比金刚石还大的化合物Y。在化合物Y中,A、B原子间以单键相结合,且每个原子的最外层均达到8个电子的稳定结构。则Y的化学式为______________,Y晶体的熔点比金刚石熔点______(填“高”或“低”)。
(6)B2H4是一种可燃性液体,其水溶液呈弱碱性,是因为溶液中存在平衡:H2B-BH2+H2O _________________________。
_________________________。
参考答案:
(1)第二周期ⅣA族
(2)Cl2+2OH-=ClO-+H2O
(3)N4(g) ====2N2(g);△H=-882 kJ/mol
(4) ;NCl3+3H2O==== NH3+3HClO?
;NCl3+3H2O==== NH3+3HClO?
(5)C3N4;高
(6)H2B-BH3++OH-(或B2H5++OH-)
本题解析:
本题难度:一般
4、选择题 元素的种类与原子的种类
[? ]
A、前者大
B、相同
C、后者大
D、无法确定
参考答案:C
本题解析:
本题难度:简单
5、填空题 (1)上表中的实线是元素周期表部分边界,请在表中用实线画出金属元素的边界(实线内的元素全是金属元素)
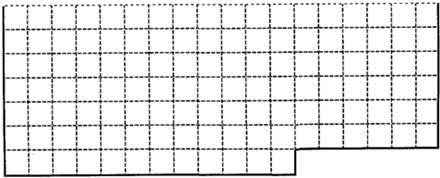
(2)元素甲是第三周期ⅦA族元素,化合物A是由甲元素等非金属元素组成的离子化合物写出其化学式______,
(3)元素乙是第三周期原子半径最小的金属元素,丙是短周期元素中原子半径最大的元素,用电子式表示丙在空气中加热反应生成B的形成过程______.B中含有的化学键是______
(4)化合物C是由甲元素和乙元素形成的化合物,将化合物A与化合物C等物质的量溶于水中,向其中滴加过量的2mol?L-1氢氧化钠溶液,直至形成透明溶液.请根据实验现象出现的先后顺序,依次写出离子方程式:__________________.
(5)实验中丙元素的鉴别方法______(不写过程)与现象______.
参考答案:(1)元素周期表的结构以及元素的分布情况,表示元素周期表的部分边界如下:
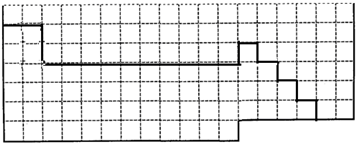
,故答案为:

;
(2)第三周期ⅦA族元素是Cl,由Cl元素等非金属元素组成的离子化合物是氯化铵,故答案为:NH4Cl;
(3)第三周期原子半径最小的金属元素为Al,短周期元素中原子半径最大的元素是Na,钠在空气中加热反应生成过氧化钠,它的形成过程可以表示为:
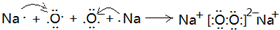
,在过氧化钠中,钠离子和过氧根之间是离子键,过氧根中氧和氧之间是共价键,故答案为:
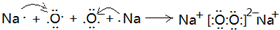
;离子键和非极性键(或离子键和共价键);
(4)化合物C是氯化铝,将化合物氯化铵与化合物氯化铝等物质的量溶于水中,向其中滴加过量的2mol?L-1氢氧化钠溶液,直至形成透明溶液铝离子先和氢氧化钠反应生成氢氧化铝沉淀,然后是铵根离子和氢氧根之间的反应,最后是氢氧化铝溶解的过程,故答案为:Al3++3OH-=Al(OH)3;NH4++OH-=NH3+H2O(NH3?H2O);Al(OH)3+OH-=AlO2-+H2O;
(5)含有钠元素的化合物的检验可以采用颜色反应的方法,颜色反应为黄色,故答案为:焰色反应;火焰呈现黄色.
本题解析:
本题难度:一般