��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� �������ӷ�Ӧ����ʽ��ȷ���ǣ� ? ��
A��̼�������Һ�����ᷴӦ��Ca��HCO3��2+2H+=Ca2++2H2O+2CO2��
B���Ȼ�����Һ�м��������ˮ��Al3++3NH3?H2O=Al��OH��3��+3NH4+
C������������Һ������������Һ��Ӧ��SO42-+Ba2+=BaSO4��
D��Fe3O4����ϡ���Fe3O4+8H+=3Fe3++4H2O
�ο��𰸣�B
���������
�����Ѷȣ���
2������� ��14�֣��Ƽ��仯������й㷺����;��
��1�������£�Ũ�Ⱦ�Ϊ0��1mol��L-1����������������Һ��pH���±���
����
| CH3COONa
| NaHCO3
| Na2CO3
| NaClO
| NaCN
|
pH
| 8��8
| 9��7
| 11��6
| 10��3
| 11��1
|
��������Һ�е������ӣ����H+������ǿ����_______ _�����ݱ������ݣ�Ũ�Ⱦ�Ϊ0��01mol��L��1���������������Һ�ֱ�ϡ��100����pH�仯������________�����ţ���
A��HCN B��HClO C��CH3COOH D��H2CO3
��2���Т�100ml 0��1 mol/L NaHCO3 ��100ml 0��1 mol/L Na2CO3������Һ����Һ��ˮ�������H+������
�� ��(�>������������<������ͬ)����Һ�������ӵ����ʵ���Ũ��֮�ͣ��� ��
��3��NaHCO3��һ�� ���ǿ��������������ʣ�д��HCO3
�ο��𰸣�
���������
�����Ѷȣ�����
3������� (12��)��1�������Ȼ�ͭ���壨CuCl2.2H2O��������FeCl2���ʣ���ȡ������CuCl2��H2O�Ƚ����Ƴ�ˮ��Һ������ͼ��������ᴿ��
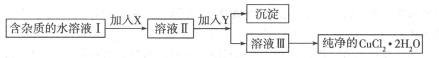
��֪Cu2����Fe3����Fe2�����������↑ʼ�����ͳ�����ȫʱ��pH���±�[��Դ:91exam.org]
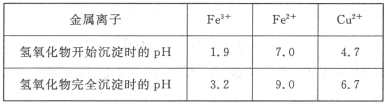
��ش��������⣺
��������� 91ExaM.org������ѡ����һ����������X
a��NaClO b��H2O2
c��KMnO4 d��HNO3
����μ�����Һ���г�Cu2����Ľ��������ӣ�________________________________��
������Һ��õ�CuCl2.2H2O����IJ�����___________________________________��
��2��ij��ѧ��ȤС��ȡһ������˫��ˮ����ȷ�ⶨ����H2O2�ĺ�����
ȡ˫��ˮ25. 00 mL����ƿ�У�����ϡ�����ữ��������ˮϡ�͡���һ��Ũ�ȵĸ�����ر���Һ�ζ����䷴Ӧ�����ӷ���ʽΪ��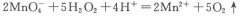
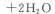
��1���ζ�ʱ����������ر���Һע��________�����ʽ����ʽ�����ζ����У��ζ������յ��������________________________________________________
��2�����ζ�ǰ�ζ��ܼ����������ݣ��ζ���������ʧ����ⶨ���____���ƫ�ߡ���ƫ�͡����䡱����
�ο��𰸣���1����b����ȡ������Һ���Թ��У������������軯����Һ����Һ�Ժ�ɫ��֤�����������ӣ������������Ʒ���������Ũ������ȴ�ᾧ����2����ʽ����Һ����ɫ���Ϻ�ɫ����30���ڲ���ɫ����3��ƫ�ߡ�
�����������1������ΪҪ����ͭ���Ӻ��������ӣ������������↑ʼ����ʱ��pHʱ���������������ӿ�ʼ����ʱ��ͭ�����Ѿ�������ȫ�������ӿ�ʼ��������������ȫ��ͭ����û�п�ʼ������������Ҫ����Ԫ��ת��Ϊ�����ӽ��з��룬���������ӱ����������Ҫ����һ���������������������µ�Ԫ�ػ����ʣ�����ѡ��b�������⡣����Һ���еij���ͭ��������Ľ����������������ӣ����������Ӻ����軯�ط�Ӧ���ɺ�ɫ���м��飬���Բ���Ϊȡ������Һ���Թ��У������������軯����Һ����Һ�Ժ�ɫ��֤�����������ӣ������������Ӻ������������ɺ��ɫ�����ķ�����������Һ���к��е��Ȼ�ͭ��Ҫ�õ����ᾧˮ�ľ��壬��Ҫ����Һ����Ũ����Ȼ����ȴ�ᾧ����2����Ϊ�������һ�㶼�����Ե���Һ���Ҹ��������ǿ�����ԣ���������ʴ�ܣ�����ѡ����ʽ�ζ��ܣ��ζ����յ�Ϊ��Һ����ɫ���Ϻ�ɫ����30���ڲ���ɫ����3�����ζ�ǰ�����ݣ��ζ�����ʧ��˵������ƫ����ⶨ�Ľ��ƫ�ߡ�
���㣺���ʵķ�����ᴿ���к͵ζ�ʵ��IJ�������������
�����Ѷȣ�����
4��ѡ���� ���е��뷽��ʽ�У���ȷ���ǣ� ? ��
A��Na2SO4�T2Na++SO4-2
B��Al2��SO4��3�T2Al3++3SO42-
C��Ba��OH��2�TBa2++��OH-��2
D��CuSO4�TCu2++S6++4O2-
�ο��𰸣�B
���������
�����Ѷȣ���
5��ʵ���� (12��)ijѧ����0.1000mol/LKOH��Һ�ζ�δ֪Ũ�ȵ�������Һ��������ɷֽ�Ϊ��
�¼���:
A ��ȡ20.00mL�����������Һע��ྻ����ƿ��������2-3�η�̪
B �ñ���Һ��ϴ�ζ���2-3��
C ��ʢ�б���Һ�ļ�ʽ�ζ��̶ܹ��ã�����Һ��ʹ�ζ��ܼ��������Һ
D��ȡ��KOH��Һע���ʽ�ζ�����0�̶�����2-3cm
E������Һ����0��0�̶����£����¶���
F������ƿ���ڵζ��ܵ����棬�ñ�KOH��Һ�ζ����յ㣬���µζ���Һ��̶�
��1�� ��ȷ������˳����(�������ĸ��д) B- ��
��2�� �ζ���ʼ���۾�ע�� ���жϵζ��յ�������ǣ�
��3�� ���в����п���ʹ���������Ũ����ֵƫ�ߵ���
A ��ʽ�ζ���δ�ñ���Һ��ϴ��ֱ��ע���Һ
B �ζ�ǰʢ��HCl����ƿ������ˮϴ����������ˮ����
C ��ʽ�ζ����ڵζ�ǰ�����ݣ��ζ���������ʧ
D ��ȡ����������Һʱ����ʼ���Ӷ������ζ�����ʱ���Ӷ���
��4���ζ���ʼ�ͽ���ʱ����ʽ�ζ����е�Һ����ͼC��ʾ�����յ����Ϊ mL������������Һ��Ũ��Ϊ mol/L��
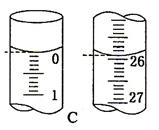
�ο��𰸣�26. (12��) ��1�� DCEAF (2��) ��2�� ��ƿ����Һ��ɫ�ı仯(2��)
��Һ����ɫ��Ϊ��dz����ɫ���Ұ��������Һ��ɫ�������ı�(2�֣�ÿ��1��)
��3�� AC(2�֣�ѡ1����ȷ��1�֣��д�������) ��4��25.90(2��) 0.1295 mol/L(2��)
���������
�������:��1���к͵ζ����ռ�©��ϴ�ӡ���ϴ��װҺ��ȡ����Һ����ָʾ�����ζ���˳�������������ȷ��˳��ΪBDCEAF����2�� �ζ���ʼ������Ӧ��ע����ƿ����Һ����ɫ�仯���ζ�ʱ����ƿ����Һ����ɫ����ɫ��dz���ұ���30���ڲ���ɫ����˵���ﵽ�ζ��յ㣺��3����ʽ�ζ���δ�ñ���Һ��ϴ��ֱ��ע���Һ���ᵼ�±�Һϡ�ͣ�����c�����⣩=C���꣩xV���꣩/V(��)�������ɵ�c�����⣩ƫ�ߣ�Aƫ�ߣ��ζ�ǰʢ��HCl����ƿ������ˮϴ����������ˮ������û��Ӱ��HCl�����ʵ�����B��Ӱ�죻��ʽ�ζ����ڵζ�ǰ�����ݣ��ζ���������ʧ���ᵼ��ĩ�����������ƫ��,Cƫ�ߣ���ȡ����������Һʱ����ʼ���Ӷ������ζ�����ʱ���Ӷ�������ʼ����ƫ��������ƫС�����ƫС��D�������в����п���ʹ���������Ũ����ֵƫ�ߵ���A��C��4���ζ��ܵ�0�̶����ϣ�1cm֮����10������������յ����Ϊ25.90mL������c�����⣩=C���꣩xV���꣩/V(��)����ɵ�����������Һ��Ũ��Ϊ0.1295 mol/L��
���㣺�����к͵ζ���֪ʶ��
�����Ѷȣ�һ��