微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (12分)湄潭中学某化学兴趣小组利用铁锈(Fe2O3)做了系列实验,物质间关系图如下。根据所学知识回答相关问题:
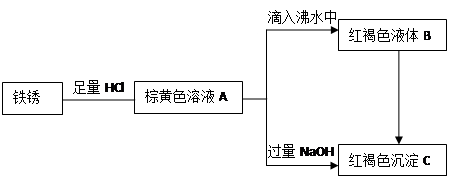
(1)写出A 、B、C三种物质的名称:
A??B??C?
(2)写出由A滴入沸水中制备B的离子方程式:?
(3)兴趣小组讨论了多种使B转换为C的方法,请写出你认为可行的一种方法:?
(4)下列说法正确的有(填序号):?
①B转换为C的过程发生了化学反应
②由A制备B时,加热越久越好
③物质B具有丁达尔效应
④把B、C的混合物过滤,滤液无色透明
⑤整个系列反应,都不涉及氧化还原反应
2、选择题 等质量的下列物质与足量稀硝酸反应,放出NO物质的量最多的是
A.FeO
B.Fe2O3
C.FeSO4
D.Fe3O4
3、实验题 某化学研究性学习小组讨论Fe3+溶液和SO32-溶液之间发生怎样的反应,提出了两种可能,写出预计反应的离子方程式:
一是发生氧化还原反应?①?;二是发生互促水解反应?②?。
为了证明发生怎样的反应,同学们设计并进行如下实验,请填写下列空白:
实验Ⅰ:取5mLFeCl3浓溶液于试管中,逐滴加入某Na2SO3浓溶液至过量,观察到无气泡产生,无沉淀生成,但溶液颜色最终变为红褐色。这种红褐色液体是?③?。
向红褐色液体中逐滴加入稀盐酸至过量,可观察到溶液最终变为黄色。将所得溶液分成两等份:
其中一份加入KSCN溶液,溶液变成血红色,此步实验的目的是?④?;另一份加入BaCl2稀溶液,有少量白色沉淀生成,产生该白色沉淀的离子方程式是?⑤?。
实验Ⅱ:将FeCl3和Na2SO3溶液分别稀释后,重复实验Ⅰ,产生的现象完全相同。
同学们由上述实验得出的结论是?⑥?。
指导老师看过上述实验步骤后认为该设计有缺陷,应在开始实验前对某主要药品进行检验,该主要药品为?⑦?;检验的目的是?⑧?。
4、选择题 向盛有a g镁铝合金的烧杯中加入cl mol/L稀硫酸V1L,合金完全溶解后,再加入c2mol/L的NaOH溶液V2L,生成沉淀的质量恰好达到最大值bg。则下列关系式不正确的是(?)
A.2c1V1=c2V2
B.反应产生氢气的质量m(H2)= 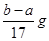
C.b≤a+17c2V2
D.合金中含镁的质量分数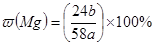
5、填空题 某氯化亚铁和氯化铁的混合物。现要测定其中铁元素的质量分数,按以下步骤
进行实验:

Ⅰ.请根据上面流程,回答以下问题:
(1)操作I所用到的玻璃仪器除烧杯、胶头滴管、玻璃棒外,还必须有?。(填仪器名称)
(2)请写出加入氯水发生的离子反应方程式?。
(3)将沉淀物加热、灼烧,冷却至室温,用天平称量其质量为b1 g,再次加热并冷却至室温称量其质量为b2 g,若b1-b2=0.3g,则接下来还应进行的操作是?
?;蒸发皿质量是W1 g,蒸发皿与加热后固体总质量是W2 g,则样品中铁元素的质量分数是?。?
Ⅱ.有同学提出,还可以采用以下方法来测定:
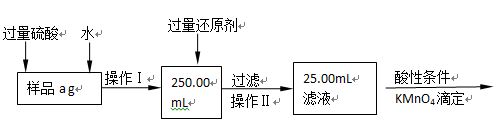
(1)选择的还原剂是否能用铁?(填“是”或“否”),原因是:?;
(2)若滴定用掉c mol?L-1 KMnO4溶液b mL,则样品中铁元素的质量分数是:?。