微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 已知A、B两种气体在一定条件下可发生反应:2A+B=C+3D+4E.现将相对分子质量为M的A气体mg与适量的B充入一个密闭容器内,恰好完全反应,有少量液滴生成,在相同的温度下测得反应前后压强分别为6.06×106和1.01×107Pa,又测得反应共放热Q?kJ,下列说法正确的是( ? )
A.D为气体
B.C为液体
C.E为气体
D.该反应的热化学方程式2A(g)+B(g)=C(g)+3D(l)+4E(g);△H=-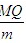 kJ/mol
kJ/mol
参考答案:C
本题解析:
本题难度:一般
2、实验题 20.(10分)某厂以重晶石(有效成分是BaSO4)为主要原料制取Ba(OH)2・8H2O晶体的示意图如下:

已知:i.BaSO4(s)+2C(s)=2CO2(g)+BaS(s) ΔH1=+226.2 kJ/mol
C(s)+CO2(g)=2CO(g) ΔH2=+172.5kJ/mol
ii.某些物质的溶解度(g/100g)简表
| 10℃
| 20℃
| 40℃
| 60℃
| 80℃
|
Ba(OH)2・8H2O
| 2.48
| 3.89
| 8.22
| 20.9
| 101
|
NaOH
| 98.0
| 109
| 129
| 174
| 314
|
NaCl
| 35.8
| 35.9
| 36.4
| 37.1
| 38.0
|
BaCl2
| 33.5
| 35.8
| 40.8
| 46.2
| 52.5
|
回答下列问题:
(1)炭与重晶石直接反应的热化学方程式是:BaSO4(s)+4C(s)=BaS(s)+4CO(g) ΔH=____kJ/mol。
(2)由BaCl2溶液可通过不同途径得到Ba(OH)2・8H2O。
途径1:

①得到固体1的离子方程式是______。
②固体2与水反应的化学方程式是______。
途径2:
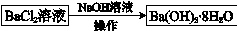
途径2中的“操作”是加热浓缩,冷却结晶,过滤。依据上述溶解度简表分析,过滤时的最佳温度是______;能从混合液中得到Ba(OH)2・8H2O晶体的原因是______。
(3)若向滤液1中加入CuO粉末,可直接得到含Ba(OH)2・8H2O晶体和CuS的浊液,反应化学方程式是______。将该浊液加热到80℃左右浓缩,趁热过滤,冷却滤液至室温,再过滤,即可得到Ba(OH)2・8H2O晶体。上述操作中趁热过滤的原因是______。
参考答案:(1)+571.2
(2)途径1:① CO32-+Ba2+ =BaCO3↓; ② BaO+9H2O=Ba(OH)2・8H2O
途径2:20℃或常温;20℃时4种物质中Ba(OH)2・8H2O溶解度最小
(3)BaS+CuO+9H2O=Ba(OH)2・8H2O+CuS;为减少过滤过程中Ba(OH)2・8H2O的损失
本题解析:(1)由于①BaSO4(s)+2C(s)=2CO2(g)+BaS(s) ΔH1=+226.2 kJ/mol
②C(s)+CO2(g)=2CO(g) ΔH2=+172.5kJ/mol
ΔH=①+2×②=226.2+2×172.5="571.2" kJ/mol
(2)①氯化钡溶液中加入碳酸钠固体,发生复分解反应,BaCl2+Na2CO3="Ba" CO3↓+ 2NaCl,则离子方程式为CO32-+Ba2+ =BaCO3↓;②BaCO3经灼烧后生成BaO,氧化钡溶于水生成氢氧化钡,化学反应方程式为BaO+9H2O=Ba(OH)2・8H2O;途径2中的“操作”是加热浓缩,冷却结晶,过滤。依据上述溶解度简表分析,过滤时的最佳温度是20℃左右,因为当温度升高后,氢氧化钡晶体的溶解度会逐渐增大;能从混合液中得到Ba(OH)2・8H2O晶体的原因是在20℃时4种物质中Ba(OH)2・8H2O溶解度最小,温度在20℃时氢氧化钡晶体以沉淀的形式析出;
(3)若向滤液1中加入CuO粉末,可直接得到含Ba(OH)2・8H2O晶体和CuS的浊液,反应化学方程式是BaS+CuO+9H2O=Ba(OH)2・8H2O+CuS;将该浊液加热到80℃左右浓缩,趁热过滤,冷却滤液至室温,再过滤,即可得到Ba(OH)2・8H2O晶体,操作中趁热过滤是为减少过滤过程中Ba(OH)2・8H2O的损失
考点:热化学方程式的计算、离子方程式的书写、工艺流程
点评:本题考查内容较丰富,注意离子方程式及化学方程式的书写,本题的关键是弄明白反应的流程。
本题难度:困难
3、选择题 下列有关热化学方程式的表示及说法正确的是
[? ]
A.已知c(石墨,s)=c(金刚石,s)?△H>0,则金刚石比石墨稳定
B.已知I2(g)+H2(g)=2HI(g)?△H1;I2(s)+H2(g)=2HI(g)?△H2;则△H1<△H2
C.HCl和NaOH反应的中和热△H=-57.3kJ/mol,则H2SO4和Ba(OH)2反应的中和热△H=2×(-57.3)kJ/mol
D.已知H2(g)+F2(g)=2HF(g)?△H=-270kJ/mol,则2L氟化氢气体分解成1L氢气和1L氟气吸收270kJ热量
参考答案:B
本题解析:
本题难度:一般
4、选择题 已知下列热化学方程式:Zn(s)+1/2O2(g)=ZnO(s);△H=-351.1kJ・mol-1
Hg(l)+1/2O2(g)=HgO(s);△H=-90.7 kJ・mol-1,由此可知反应:
Zn(s)+HgO(s)=ZnO(s)+ Hg(l)的△H为。
A.△H=-1141.8 kJ・mol-1
B.△H=+260.4kJ・mol-1
C.△H=+441.8 kJ・mol-1
D.△H=-260.4 kJ・mol-1