��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��������������Ӧ����1molˮ�����ų�241.8kJ��������1gˮ����ת��ΪҺ̬ˮ�ų�2.45kJ���������������Ȼ�ѧ����ʽ��д��ȷ���ǣ�������
A��H2��g��+ O2��g��=H2O��l������H=-285.9kJ/mol
O2��g��=H2O��l������H=-285.9kJ/mol
B��H2��g��+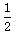 O2��g��=H2O��l������H=-241.8kJ/mol
O2��g��=H2O��l������H=-241.8kJ/mol
C��H2��g��+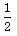 O2��g��=H2O��l������H=+285.9kJ/mol
O2��g��=H2O��l������H=+285.9kJ/mol
D��H2��g��+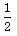 O2��g��=H2O��l������H=+241.8kJ/mol
O2��g��=H2O��l������H=+241.8kJ/mol
�ο��𰸣�A
���������
�����Ѷȣ���
2������� ���³�ѹ�£�����1mol�����룩������ӻ�ѧ�������յ��������γ�1mol�����룩������ӻ�ѧ�����ų���������Ϊ���ܣ���λΪkJ.mol-1���±���һЩ�������ݣ�kJ·mol��1��
��ѧ��
| ����
| ��ѧ��
| ����
| ��ѧ��
| ����
|
C��F
| 427
| C��Cl
| 330
| C��I
| 218
|
H��H
| 436
| S��S
| 255
| H��S
| 339
|
�ش��������⣺
��1���ɱ������ݹ���Ԥ��C��Br���ļ��ܷ�Χ��_________ <C��Br����<__________ ���ش���ֵ�͵�λ��
��2���Ȼ�ѧ����ʽ2H2(g)��S2(g) =2H2S(g)����H= QkJ·mol��1����Q=
��3�� ��֪�����Ȼ�ѧ����ʽ��
O2 (g) = O+2(g) + e��  H1=" +1175.7" kJ·mol-1
H1=" +1175.7" kJ·mol-1
PtF6(g) + e��= PtF6��(g)  H2= ��771.1 kJ·mol-1
H2= ��771.1 kJ·mol-1
O2+PtF6��(s) = O2+(g) + PtF6��(g)  H3=" +482.2" kJ·mol-1
H3=" +482.2" kJ·mol-1
��ӦO2(g) + (g) = O2+PtF6�� (s)  H="_____________" kJ·mol-1��
H="_____________" kJ·mol-1��
�ο��𰸣���1��218 KJ·mol��1 ~330 KJ·mol��1 ��2����229 ��3��PtF6����77.6
�����������1�����ݱ������ݵù��ɣ�±��Ԫ��C��X���ļ������ϵ������μ�С��Ԥ��C��Br���ļ��ܷ�Χ��218 KJ·mol��1<C��Br����<330 KJ·mol��1����2�����ݻ�ѧ��Ӧ���ʱ���ڷ�Ӧ��ļ���֮�ͼ�������ļ���֮�ͼ��㣬ע������ʵĽṹ�ͻ�ѧ������Ŀ��
��H="2��436" KJ·mol��1 +255KJ·mol��1 ��4��339KJ·mol��1=��229 kJ·mol-1;
��3�����ݸ�˹���ɢ�+��-�۵õ�����Ӧ�Ȼ�ѧ����ʽΪ��O2��g��+PtF6��g��
�����Ѷȣ�����
3������� ����ȷ�ϣ�CO��SO2��NOx���ŷ�����ɴ�����Ⱦ����Ҫԭ��
��1����CO2�������ϳ�CH3OH������Ҫ���壬�ȿ��Խ���������⣬���ɽ����ԴΣ������֪CH3OH������Ҫ���壬�ȿ��Խ���������⣬���ɽ����ԴΣ������֪CH3OH��H2��ȼ���ȷֱ�Ϊ-726.5kJ/mol��-285.8kJ/mol��д����ҵ����CO2��H2�ϳ�CH3OH���Ȼ�ѧ����ʽ��______��
��2���ò����缫��һ��ͨ�������һ��ͨ��CH3OH��l������KOH��Һ�����ȼ�ϵ�أ��为����ӦʽΪ______����Һ�е���������______�������ƶ���
��3����ͼ��һ���绯ѧװ��ʾ��ͼ����CH3OH-����ȼ�ϵ������װ�õĵ�Դ��
�����AΪ��ͭ��BΪ��ͭ��CΪCuSO4��Һ����ԭ���Ĺ�ҵ����������______��
�����A�Dz��缫��B��ʯī�缫��C��AgNO3��Һ��ͨ�����B������10.8g����ȼ�ϵ������������______mol�״���������
���������λ��Ч���֣�
��4����������1L��0.2mol/L?NaOH��Һ��ͨ��4.48L����״������SO2�����Ի�Ϻ���Һ����ı仯�����������Һ��pH��7������Һ��c��SO32-��_______c��H2SO3���������������������=�������йظ���Һ������Ũ�ȹ�ϵ���ж���ȷ����______������ĸ��ţ���
A��c��SO32-��ʮc��OH-��+c��HSO3-��=c��Na+��+c��H+��
B��c��H2SO3��+c��HSO3-��+c��SO32-��=0.2mol/L
C��c��H2SO3��+c��H+��=c��SO32-��ʮc��OH-��
D��c��Na+����c��H+����c��HSO3-����c��OH-��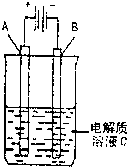
�ο��𰸣���1���״���������ȼ������д���Ȼ�ѧ����ʽ�ֱ�Ϊ��
��2CH3OH��l��+3O2��g��=2CO2��g��+4H2O��l������H1=-1453kJ/mol��
��2H2��g��+O2��g��=2H2O��l������H2=-571.6KJ/mol��
���ݸ�˹���ɣ���ӦCO2��g��+3H2��g���TCH3OH��l��+H2O��l��
���Կ����Ƿ���ʽ32����-�١�12�����ԡ�H=32����-571.6KJ/mol��-��-1453kJ/mol����12=-130.9KJ/mol��
�ʴ�Ϊ��CO2��g��+3H2��g���TCH3OH��l��+H2O��l������H=-130.9KJ/mol��
��2���ڼ״�ȼ�ϵ���У���������ȼ�ϼ״�ʧ���ӵķ�Ӧ�����������KOH��Һʱ��
�缫��ӦΪ��CH3OH-6e-+8OH-=6H2O+CO32-��������е����������ƶ���
�ʴ�Ϊ��CH3OH-6e-+8OH-=6H2O+CO32-������
��3�����������Ϊ��ͭ������Ϊ��ͭ�������ΪCuSO4��Һ�ĵ��ؿ���ʵ�ִ�ͭ�н���ͭ�ľ���������⾫������ͭ���ʴ�Ϊ��������ͭ��
��A�Dz��缫��B��ʯī�缫��C��AgNO3��Һ��ͨ���B���ϵĵ缫��ӦΪ��Ag++e-=Ag������������10.8gʱ��ת�Ƶ���0.1mol�����ݼ״�ȼ�ϵ�ص��ܷ�Ӧʽ��2CH3OH��l��+3O2��g��=2CO2��g��+4H2O��l������֪��ת��12mol����ʱ�����ļ״������ʵ���Ϊ2mol�����Ե�ת��0.1mol����ʱ�����ļ״������ʵ���Ϊ0.212��0.017mol��
�ʴ�Ϊ��0.017��
��4����������1L��0.2mol/L?NaOH��Һ��ͨ��4.48L����״������SO2�����Ի�Ϻ���Һ����ı仯��ʱ�����õ���ҺΪ0.2mol/L�����������ƣ���Һ�����ԣ�˵������������ĵ���̶ȴ���ˮ��̶ȣ�A�����ݵ���غ�ã�2c��SO32-��ʮc��OH-��+c��HSO3-��=c��Na+��+c��H+������A����
B�����������غ�ã�c��H2SO3��+c��HSO3-��+c��SO32-��=0.2mol/L����B��ȷ��
C�����������غ�ã�c��H2SO3��+c��H+��=c��SO32-��ʮc��OH-������C��ȷ��
D����Һ�е�����Ũ�ȴ�С��ϵΪ��c��Na+����c��HSO3-����c��H+����c��OH-������D����
��ѡBC��
���������
�����Ѷȣ�һ��
4��ѡ���� C(s) + H2O(g) == CO(g) + H2(g)�� ��H=+131��3 KJ/mol������ʾ
[? ]
A��̼��ˮ��Ӧ����131��3 KJ������
B��1mol��̬��̿��1molˮ������Ӧ����һ����̼������������131��3 KJ������
C��1mol̼��1molˮ��Ӧ����131��3 KJ������
D����̬̼����̬ˮ��1mol��Ӧ���ų�131��3 KJ������
�ο��𰸣�C
���������
�����Ѷȣ�һ��
5��ѡ���� ͬ��ͬѹ�£���֪���и���ӦΪ���ȷ�Ӧ�����и��Ȼ�ѧ����ʽ�С�H������
[? ]
A��2A ��l��+ B��l ��= 2C��g�� ��H1
B��2A ��g��+ B��g��= 2C��g�� ��H2
C��2A ��g��+ B��g��= 2C��l�� ��H3
D��2A ��l��+ B��l��= 2C��l�� ��H4
�ο��𰸣�A
���������
�����Ѷȣ���