| �߿�ʡ������ | |
|
|
| �߿�ʡ������ | |
|
|
|
���л�ѧ֪ʶ����ɡ�ˮ�ĵ���ƽ�⡷����̣�2017�����°棩(��)
�ο��𰸣�B ����������� �����Ѷȣ��� 3��ѡ���� ��pH������9��NaOH��CH3COONa������Һ�У�����ˮ���������OH������Ũ�ȷֱ�ΪA mol��L��1��B mol��L��1����A��B�Ĺ�ϵΪ [? ] A��A��B B��A��10��4B C��B��10��4A D��A��B �ο��𰸣�B ��������� �����Ѷȣ�һ�� 4��ѡ���� ������Һ���й����ӵ����ʵ���Ũ�ȹ�ϵ��ȷ���� �ο��𰸣�A ������������������A����HCl�TH++Cl-��CH3COOH?H++CH3COO-����pH��Ϊ4ʱc��H+����ͬ��������Һ�����Կɵã�c��Cl-��=c��CH3COO-������A��ȷ�� �����Ѷȣ����� 5��ѡ���� ����������ȷ���� |
�ο��𰸣�AD
��������������ε���ɿ�֪������Ũ����ͬʱ���������Һ�е�笠�����Ũ�ȱ��Ȼ����Һ�еĴ������������Һ�е�笠�����Ũ�ȱ��������С����Ϊ�������ӵ�ˮ�ⷴӦ������笠����ӵ�ˮ�⣬��c(NH4+)��(NH4)2Fe(SO4)2>(NH4)2SO4>NH4Cl����֮�������������Һ��c(NH4+)��ȣ����������Ũ�ȱ��ֲ���ʱ�����Ȼ��Ũ������ij̶���������Ũ������ij̶���Σ���������Ũ�ȴ�С��ϵΪc[(NH4)2Fe(SO4)2]��c[(NH4)2SO4]��c(NH4Cl)����Aѡ����ȷ������n=c?V����HY��NaOH�����ʵ�����ȣ�����ǡ����ȫ�кͣ�����NaY��Һ��������ҺpH=9������Һ�Լ��ԣ�˵��NaY��ǿ�������Ρ�HY�����ᣬ��ͬ������c(H+)=10��pHmol/L=10��9mol/L��Kw=c(H+)?c(OH��)=10��14����ü�����Һ�е���Һ��c(OH��)=Kw/c(H+)=10��5mol/L������NaY��Һ�������غ��ϵʽΪc(OH��)=c(H+)+c(HY)= 10��5mol/L����Bѡ�����ǿ����ǿ����ʱǿ����������Ϻ���Һ��c(H+)=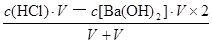 =
=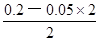 mol/L=0.05mol/L������pH="��lg" c(H+)�������ҺpH����1��2֮�䣬��Cѡ�����̼�����Ƶĵ���̶�Զ����ˮ����NaHCO3=Na++HCO3����H2O
mol/L=0.05mol/L������pH="��lg" c(H+)�������ҺpH����1��2֮�䣬��Cѡ�����̼�����Ƶĵ���̶�Զ����ˮ����NaHCO3=Na++HCO3����H2O H++OH����ˮ�������������Ũ�ȵ���ˮ����������������ӣ�̼��������Ӳ�����ˮ�⣬�����ܵ��룬��HCO3��+ H2O
H++OH����ˮ�������������Ũ�ȵ���ˮ����������������ӣ�̼��������Ӳ�����ˮ�⣬�����ܵ��룬��HCO3��+ H2O H2CO3+OH����HCO3��
H2CO3+OH����HCO3�� H++ CO32����ǰ������ˮ�������������Ũ�������ɵ�̼��Ũ����ȣ���������ˮ�����������������Ũ�������ɵ�̼�������Ũ����ȣ����������غ�ԭ���ɵã�c(H+)+c(H2CO3)=c(CO32��)+c(OH��)����Dѡ����ȷ��
H++ CO32����ǰ������ˮ�������������Ũ�������ɵ�̼��Ũ����ȣ���������ˮ�����������������Ũ�������ɵ�̼�������Ũ����ȣ����������غ�ԭ���ɵã�c(H+)+c(H2CO3)=c(CO32��)+c(OH��)����Dѡ����ȷ��
���㣺����ˮ��Һ������Ũ�ȴ�С��ϵ���漰����ˮ��̶ȴ�С��ϵ������Һ�������غ��ϵʽ����Һ��pH��ˮ�����ӻ��ȡ�
�����Ѷȣ�һ��
| ���� �� С������ӡ�� �������� ���ر��� �����ض����� | |
| ��һƪ���߿���ѧ���⡶���ۺ����ƶϡ�.. | |
| �����Ŀ |