��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ���������У��������ᷴӦ�������ܲ�����������
A.Pb(NO3)2��Һ
B.Na2S��Һ
C.CuSO4��Һ
D.ϡH2SO4
�ο��𰸣�B
������������������A������PbS������B������NaHS��C������CuS������D�в���Ӧ����ѡB��
���㣺����H2S������
������������ʶ����֪ʶ�Ŀ��飬�ص㿼��ѧ����H2S���ʵ���Ϥ�˽�̶ȣ�ּ�ڿ���ѧ��������û���֪ʶ���ʵ��������������ѶȲ���������ס����������ü��ɡ�
�����Ѷȣ�����
2��ѡ���� ��CO��H2��O2��ɵĻ�����壬��һ��������ǡ����ȫ��Ӧ�������������101?kPa��120���¶Կ���������ܶ�Ϊ1.293����ԭ���������CO��ռ�������Ϊ
A.1/3
B.2/3
C.1/2
D.1/6
�ο��𰸣�C
���������
�����Ѷȣ�һ��
3��ѡ���� 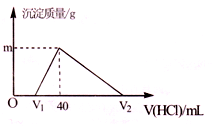 �����£���ag�����Ͻ��ĩ����һ����ˮ�У������ȫ���ܽ⣬�ռ���b?mL���壨��״������Ȼ������Һ�м���1mol/L�����ᣬ���ɳ�������������������������ϵ��ͼ��ʾ����V1=20mL�������й�ϵ��ȷ����
�����£���ag�����Ͻ��ĩ����һ����ˮ�У������ȫ���ܽ⣬�ռ���b?mL���壨��״������Ȼ������Һ�м���1mol/L�����ᣬ���ɳ�������������������������ϵ��ͼ��ʾ����V1=20mL�������й�ϵ��ȷ����
A.a=0.92
B.b=896
C.m=1.56
D.V2=100
�ο��𰸣�CD
��������������������Ͻ�����ˮ�У��Ͻ�ȫ���ܽ⣬����2Na+2H2O�T2NaOH+H2����2Al+2H2O+2NaOH�T2NaAlO2+3H2����
��ͼ���֪����������û���������������������ȷ�����ӦNaOH+HCl�TNaCl+H2O���ý���������20mL��
Ȼ������ӦNaAlO2+HCl+H2O�TNaCl+Al��OH��3����������������������40mLʱ���������ֵ����ʱ��Һ������ΪNaCl������Ԫ���غ��֪n��Na��=n��NaCl�����ý������������Ϊ40mL-20mL=20mL�����ݷ���ʽ����n[Al��OH��3]��������Ԫ���غ�n��Al��=n[Al��OH��3]��
�������ӦAl��OH��3��+3HCl�TAlCl3+3H2O�������������������ʵ�������ý���������������
A������m=nM����Na��Al�Ͻ��������
B������Na��Al�����ʵ�������������������������ٸ���V=nVm�������ɵ������������
C�������������������ʵ���������m=nM��������������������
D���ܽ������������ĵ����������40mL֮��ΪV2��ֵ��
��������Ͻ�����ˮ�У��Ͻ�ȫ���ܽ⣬����2Na+2H2O�T2NaOH+H2����2Al+2H2O+2NaOH�T2NaAlO2+3H2����
��ͼ���֪����������û���������������������ȷ�����ӦNaOH+HCl�TNaCl+H2O���ý���������20mL��
Ȼ������ӦNaAlO2+HCl+H2O�TNaCl+Al��OH��3����������������������40mLʱ���������ֵ����ʱ��Һ������ΪNaCl������Ԫ���غ��֪n��Na��=n��NaCl��=0.04L��1mol/L=0.04mol���ý������������Ϊ40mL-20mL=20mL�����ݷ���ʽ����n[Al��OH��3]=n��HCl��=0.02L��1mol/L=0.02mol��������Ԫ���غ�n��Al��=n[Al��OH��3]=0.02mol��
�������ӦAl��OH��3��+3HCl�TAlCl3+3H2O��������������ʵ���Ϊ0.02mol��3=0.06mol���ʸý����ĵ��������Ϊ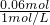 =0.06L=60mL��
=0.06L=60mL��
A��������������֪��Na��Al�Ͻ������Ϊ0.04mol��23g/mol+0.02mol��27g/mol=1.46g����A����
B���ɷ���ʽ��֪��0.04molNa��������Ϊ0.04mol�� =0.02mol��0.02molAl��������Ϊ0.02mol��
=0.02mol��0.02molAl��������Ϊ0.02mol�� =0.03mol�����������������ʵ���Ϊ0.02mol+0.03mol=0.05mol�������µ����Ϊ0.05mol��22.4L/mol=1.12L����B����
=0.03mol�����������������ʵ���Ϊ0.02mol+0.03mol=0.05mol�������µ����Ϊ0.05mol��22.4L/mol=1.12L����B����
C�������������֪�����ɳ���Ϊ0.02mol��������Ϊ0.02mol��78g/mol=1.56g����C��ȷ��
D�������������֪���ܽ���������������������Ϊ60mL����V2Ϊ40mL+60mL=100mL����D��ȷ��
��ѡCD��
���������⿼��������йؼ��㼰�ơ����Ļ�ѧ���ʵȣ���ȷ�����Ļ�ѧ��Ӧ����Ӧ��ͼ��Ķ�Ӧ��ϵ�ǽ����Ĺؼ���ע������Ԫ���غ�ķ���������ѶȽϴ�
�����Ѷȣ���
4��ѡ���� ��CO2ͨ��NaOH��Һ�У�������Na2CO3��NaHCO3�����ʵ���֮��Ϊ2��1ʱ��CO2��NaOH�����ʵ���֮��Ϊ
A.3��2
B.3��4
C.3��5
D.1��2
�ο��𰸣�C
��������������ֱ���á������Ӻ�̼ԭ���غ㡱��������Na2CO3��NaHCO3�����ʵ����ֱ�Ϊ2mol��1mol���������ӵ����ʵ���Ϊ2mol��2��1mol��5mol��̼ԭ�ӵ����ʵ���Ϊ2mol��1mol��3mol����Ȼ��CO2��NaOH�����ʵ���֮��Ϊ3��5��
�����Ѷȣ�����
5��ѡ���� �����Ȼ�������ֱ���ý��������ᷴӦ�õ�����
A.CuCl2
B.FeCl2
C.FeCl3
D.AgCl
�ο��𰸣�B
���������Cu�������ᷴӦ��Ag�������ᷴӦ��Fe�����ᷴӦ����FeCl2��
�����Ѷȣ���