微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列粒子中,核外电子总数相同的是( )
①F-?②Na+?③Ne?④K+?⑤
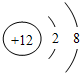
A.①②③⑤
B.①②④⑤
C.①②③④
D.②③④⑤
2、选择题 某电子层当它作为最外层时,最多只能容纳8个电子,当它作为次外层时,最多只能容纳18个电子,该电子层可能是( )
A.M层
B.K层
C.L层
D.P层
3、简答题
元素
Mn
Fe
|
电离能(?kJ?mol-1)
I1
717
759
I2
1509
1561
I3
3248
2957
|
Mn、Fe均为第四周期过渡元素,两元素的部分电离能数据列于下表:
回答下列问题:
(1)Mn元素价电子的电子排布式为______,比较两元素的I2、I3可知,气态Mn2+再失去一个电子比气态Fe2+再失去一个电子难.对此,你的解释是:______
(2)Fe原子或离子外围有较多能量相近的空轨道能与一些分子或离子形成配合物.
①与Fe原子或离子形成配合物的分子或离子应具备的结构特征是______.
②六氯和亚铁离子〔Fe(CN)64-〕中的配体CN-中C原子的杂化轨道类型是______,写出一种与CN-互为等电子体的单质分子的路易斯结构式______.
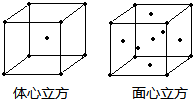
(3)三氯化铁常温下为固体,熔点:282℃,沸点315℃,在300℃以上升华.易溶于水,也易溶于乙醚、丙酮等有机溶剂.据此判断三氯化铁的晶体类型为:______
(4)金属铁的晶体在不同的温度下有两种堆积方式,晶体分别如图所示.面心立方晶胞和体心立方晶胞中实际含有的Fe原子个数之比为:______.
4、选择题 最近因大地震导致的日本核泄漏使核电站周边大气中人工放射性核素53131I含量偏高,当空气中53131I超过某种数值时就会对人体产生危害,下面有关说法中正确的是( )
A.53131I的中子数是131
B.53131I的中子数与质子数的差是25
C.53131I的电子数是78
D.53131I有放射性而53126I没有,故它们核外电子排布不同
5、简答题 氮、磷、砷是同族元素,该族元素单质及其化合物在农药、化肥等方面有重要应用.请回答下列问题.
(1)砷原子核外电子排布式为______.
(2)K3[Fe(CN)6]晶体中Fe3-与CN-之间的键型为______,该化学键能够形成的原因是______.
(3)NH4+中氮原子的杂化类型为______,NH4+的空间构型为______.
(4)已知:
| CH4 | SiH4 | NH3 | PH3
沸点(K)
101.7
161.2
239.7
185.4
分解温度(K)
873
773
1073
713.2
|
分析上表中四种物质的相关数据,请回答:
①CH4和SiH4比较,NH3和PH3比较,沸点高低的原因是______;
②CH4和SiH4比较,NH3和PH3比较,分解温度高低的原因是______;
结合上述数据和规律判断,一定压强下HF和HC1的混合气体降温时______先液化.
(5)电负性(用X表示)也是元素的一种重要性质,下表给出8种元素的电负性数值:
| 元素 | Na | Mg | Al | Si | P | S | Cl | K
电负性
0.9
1.2
1.5
1.8
2.1
2.5
3.0
0.8
|
请回答下列有关问题:
①估计钙元素的电负性的取值范围:______<X<______.
②经验规律告诉我们:当形成化学键的两原子相应元素的电负性差值大于1.7时,所形成的一般为离子键;当小于1.7时,一般为共价键.试推断AIC13中形成的化学键的类型及其理由是______.