微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (10分)(1)肼(N2H4)又称联氨,是一种可燃性液体,可用作火箭燃料。已知在101kPa,320g N2H4在氧气中完全燃烧生成氮气,放出热量624kJ(25℃时),N2H4完全燃烧的热化学方程式是:
(2)肼―空气燃料电池是一种碱性燃料电池,电解质溶液是20~30%的KOH溶液。肼―空气燃料电池放电时,正极的电极反应式是 ;负极的电极反应式是 。
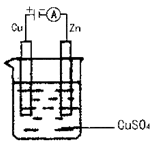
(3)如图是一个电化学过程示意图。假设使用肼―空气燃料电池作为本过程的电源,铜片质量变化128g,则肼―空气燃料电池理论上消耗标准状况下的空气 L(假设空气中氧气的体积含量为20%)。
(4)传统制备肼的方法是以NaClO氧化NH3制得肼的稀溶液,该反应的离子方程式是 。
参考答案:(1)N2H4(l)+O2(g)=N2(g)+2H2O(l);△H=-62.4KJ・mol-1
(2)正:O2+2H2O+4e―=4OH― 负:N2H4+4OH―-4e―=N2+4H2O
(3)112 L (4)ClO―+2NH3=Cl―+N2H4+H2O
本题解析:(1)320g肼恰好是10mol,所以热化学方程式为N2H4(l)+O2(g)=N2(g)+2H2O(l);△H=-62.4kJ/mol。
(2)原电池中正极得电子发生还原反应,所以空气是正极,在碱性电解质溶液中电极反应为:O2+2H2O+4e―=4OH―;负极失电子发生氧化反应,所以肼是负极,在碱性电解质溶液中电极反应为: N2H4+4OH--4e-=4H2O+N2↑。
(3)根据装置可知,铜和电源的正极相连,作阳极。因此反应中转移电子是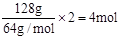 所以根据电子得失守恒可知,消耗氧气是1mol,则空气是5mol,标准状况下的体积是5mol×22.4L/mol=112L。
所以根据电子得失守恒可知,消耗氧气是1mol,则空气是5mol,标准状况下的体积是5mol×22.4L/mol=112L。
(4)NaClO氧化NH3的离子方程式是ClO―+2NH3=Cl―+N2H4+H2O。
考点:化学反应中的热量变化、原电池和氧化还原反应
点评:本题综合性比较强,知识点比较基础,难度小。
本题难度:一般
2、填空题 Li-SOCl2电池可用于心脏起搏器。该电池的电极材料分别为锂和碳,电解液是LiAlCl4-SOCl2。电池的总反应可表示为:4Li+2SOCl2 =4LiCl+S+SO2。
请回答下列问题:
(1)电池的负极材料为____________,发生的电极反应为____________;
(2)电池正极发生的电极反应为________________________;
(3)SOCl2易挥发,实验室中常用NaOH溶液吸收SOCl2,有Na2SO3和NaCl生成。如果把少量水滴到
SOCl2中,实验现象是____________________,反应的化学方程式为_____________________;
(4)组装该电池必须在无水、无氧的条件下进行,原因是_________________________。
参考答案:(1)锂;Li-2e-==Li+
(2)2SOCl2+4e-==4Cl-+S+SO2
(3)出现白雾,有刺激性气体生成;SOCl2+H2O==SO2↑+2HCl↑
(4)锂是活泼金属,易与H2O、O2反应,SOCl2也可与水反应
本题解析:
本题难度:一般
3、选择题 为将来源:91考试网 91eXAm.org反应2Al+6H+=2Al3++3H2↑的化学能转化为电能,下列装置能达到目的的是(铝条均已除去了氧化膜)
[? ]
A.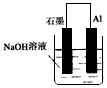
B.
C.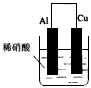
D.
参考答案:B
本题解析:
本题难度:简单
4、选择题 某原电池装置如图所示,电池总反应为2Ag+Cl2===2AgCl。下列说法正确的是
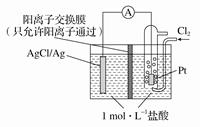
A.当电路中转移0.1 mol e-时,交换膜左侧溶液中约减少0.2 mol离子
B.放电时,交换膜两侧溶液中均有大量白色沉淀生成
C.若用NaCl溶液代替盐酸,则电池总反应随之改变
D.正极反应为AgCl+e-===Ag+Cl-