微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
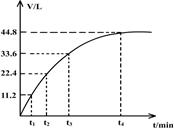
1、选择题 向一洁净干燥的烧杯中加入44.4gAl粉与Fe粉混合物,然后加入过量的盐酸,产生标况下气体26.88L。若将该混合物加入500mL14 mol・L-1的HNO3中(不考虑发生钝化),产生的气体(标准状况下测定)如图所示,假设HNO3的还原产物为NO与NO2,那么理论上从哪一时刻开始产生NO气体?(假设浓度小于9mol/L为稀HNO3)
A.t1
B.t2
C.t3
D.t4
参考答案:C
本题解析:由Al粉与Fe粉的混合物共44.4g,与过量盐酸反应产生标况下?气体26.88L,根据得失电子守恒可以计算出Al与Fe分别是0.4mol、0.6mol,将该混合物加入500mL14 ?mol・L-1的HNO3中,若金属全部生成+3价硝酸盐,则未被还原的硝酸的物质的量为3mol,被还原的硝酸的物质的量由图中的气体体积可知是2mol,所以共消耗硝酸3+2=5mol<0.5ml×14 mol・L-1=7mol,硝酸过量,固体全部溶解。设气体产物中NO与NO2的物质的量分别为x、ymol,根据得失电子守恒可得,3x+y=(0.4+0.6)×3,x+y=2,解得x=0.5,y=1.5,1.5mol×22.4L/mol=33.6L,所以理论上在t3时刻开始产生NO气体,答案选C。
 考点:
考点:
本题难度:一般
2、选择题 取一定质量的均匀固体混合物Cu、Cu2O和 CuO,将其分成两等份,取其中一份用足量的氢气还原,测得反应后固体质量减少6.40g,另一份中加入500mL稀硝酸,固体恰好完全溶解,且同时收集到标准状况下NO气体4.48L,则所用硝酸的物质的量浓度为 (?)?
A.3.2mol/L
B.2.8mol/L
C.1.8mol/L
D.缺数据无法计算
参考答案:A
本题解析:用足量的氢气还原时发生反应:Cu2O+H2 2Cu +H2O;CuO+H2
2Cu +H2O;CuO+H2 Cu +H2O。固体减少的质量为氧元素的质量。n(O)=6.4g÷16g/mol=0.4mol.所以①n(Cu2O)+ (CuO)= n(O)=0.4mol.稀硝酸恰好完全溶解固体发生反应:3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O;CuO+2HNO3=Cu(NO3)2+H2O; 3Cu2O+14HNO3=6Cu(NO3)2+2NO↑+7H2O.根据这两个反应方程式可看出:3Cu---2NO;3Cu2O―2NO。n(NO)=4.48L÷22.4L/mol=0.2mol,所以②n(Cu)+n(Cu2O)="0.3mol." ①+②可得:n(Cu)+n(CuO)+2n(Cu2O)=0.7mol.n(HNO3)=2n(Cu(NO3)2)+n(NO).而n(铜元素)=n(Cu)+n(CuO)+2n(Cu2O).所以n(HNO3)=2×0.7+0.2=1.6mol.故C(HNO3)= n(HNO3)÷V=1.6mol÷0.5L=3.2mol/L.选项为:A。2O、CuO与H2、HNO3发生化学反应的知识。
Cu +H2O。固体减少的质量为氧元素的质量。n(O)=6.4g÷16g/mol=0.4mol.所以①n(Cu2O)+ (CuO)= n(O)=0.4mol.稀硝酸恰好完全溶解固体发生反应:3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O;CuO+2HNO3=Cu(NO3)2+H2O; 3Cu2O+14HNO3=6Cu(NO3)2+2NO↑+7H2O.根据这两个反应方程式可看出:3Cu---2NO;3Cu2O―2NO。n(NO)=4.48L÷22.4L/mol=0.2mol,所以②n(Cu)+n(Cu2O)="0.3mol." ①+②可得:n(Cu)+n(CuO)+2n(Cu2O)=0.7mol.n(HNO3)=2n(Cu(NO3)2)+n(NO).而n(铜元素)=n(Cu)+n(CuO)+2n(Cu2O).所以n(HNO3)=2×0.7+0.2=1.6mol.故C(HNO3)= n(HNO3)÷V=1.6mol÷0.5L=3.2mol/L.选项为:A。2O、CuO与H2、HNO3发生化学反应的知识。
本题难度:一般
3、选择题 已知某金属硝酸盐,在受热分解时生成了金属氧化物、二氧化氮与氧气。得到的二氧化氮与氧气通入水中,恰好被水完全吸收,试分析该硝酸盐分解时金属化合价的变化情况是(? )?
A.升高
B.降低
C.不变
D.不能确定
参考答案:C
本题解析:根据题意可知,NO2是还原产物,氧气是氧化产物。得到的二氧化氮与氧气通入水中,恰好被水完全吸收,这说明二者恰好反应又生成硝酸,所以根据电子的得失守恒可知,原硝酸盐中金属的化合价是不变的,答案选C。
点评:该题是高考中的常见题型,属于中等难度的试题。试题综合性强,侧重对学生灵活运用氧化还原反应的知识解决实际问题的能力,有利于培养学生的逻辑推理能力和逆向思维能力,提高学生分析问题、解决问题的能力。
本题难度:简单
4、填空题 【化学―选修2:化学与技术】(15分)
近年来,为提高能源利用率,西方提出共生理念――为提高经济效益,人类生产活动尽可能多功能化。共生工程将会大大促进化学工业的发展。
(1)由于共生工程的应用,利用发电厂产生的SO2制成自发电池,其电池反应方程式为:2SO2+O2+2H2O=2H2SO4,该电池电动势为1.06V。实际过程中,将SO2通入电池的 极(填“正”或“负”),负极反应式为 ;用这种方法处理SO2废气的优点是 。
(2)以硫酸工业的SO2尾气、氨水、石灰石、焦炭、碳酸氢铵和氯化钾等为原料,可以合成有重要应用价值的硫化钙、硫酸钾、亚硫酸铵等物质。合成路线如下:
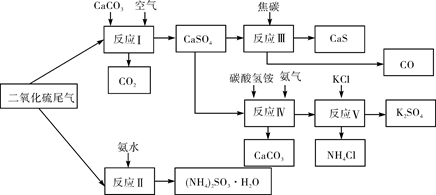
①生产中,向反应II中的溶液中加入适量还原性很强的对苯二酚等物质,其目的是 。
②下列有关说法正确的是 (填序号)。
A.反应Ⅰ中需鼓入足量空气,以保证二氧化硫充分氧化生成硫酸钙
B.反应III中发生反应的化学方程式为CaSO4+4C CaS+4CO↑
CaS+4CO↑
C.反应IV需控制在60~70℃,目的之一是减少碳酸氢铵的分解
D.反应V中的副产物氯化铵可用作氮肥