微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 (12分)Ⅰ试写出中学阶段常见的两种制取氧气的化学方程式:
?;?。
Ⅱ.实验室中通常用MnO2作催化剂分解过氧化氢,已知CuSO4溶液对过氧化氢的分解也具有催化作用,某实验兴趣小组同学猜想其他盐溶液也可能在这个反应中起同样的作用,于是他们做了以下探究。请你帮助他们完成实验报告:
(1)实验过程:在一支试管中加入5 mL 5%的H2O2溶液,然后滴入适量的FeCl3溶液,把带火星的木条伸入试管。
实验现象:?。
实验结论:FeCl3溶液可以催化分解H2O2。
(2)已知FeCl3在水中可解离出Fe3+和Cl-,同学们提出以下猜想:
甲同学的猜想:真正催化分解H2O2的是FeCl3溶液中的H2O;
乙同学的猜想:真正催化分解H2O2的是FeCl3溶液中的Fe3+;
丙同学的猜想:真正催化分解H2O2的是FeCl3溶液中的Cl-。
你认为最不可能的是?同学的猜想,理由是?。
(3)同学们对余下的两个猜想,用实验进行了探究,并记录如下,请你仔细分析后填表:
实验过程?实验现象?结论
实验过程
| 实验现象
| 结论
|
向盛有5 mL 5%的H2O2溶液的试管中滴入少量的 HCl,把带火星的木条伸入试管.
| 无明显现象
| ?
?
|
向盛有5 mL 5%的H2O2溶液的试管中滴入少量的Fe2(SO4)3,把带火星的木条伸入试管.
| 试管中有大量气泡产生,带火星的木条复燃?
| ?
?
2、选择题 实验室可利用反应“Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O”制取SO2,下列措施能降低该化学反应速率的是( )
A.适当降低反应温度
B.用铜粉代替铜片
C.加入MnO2作催化剂
D.将浓硫酸改为稀硫酸
3、填空题 (6分)(1)反应I2+2S2O32―=2I―+S4O62―常用于精盐中碘含量测定。某同学利用该反应探究浓度对反应速率的影响。实验时均加入1mL淀粉溶液做指示剂,若不经计算,直接通过褪色时间的长短判断浓度与反应速率的关系,下列试剂中应选择 (填序号)。
①1mL 0.01 mol・L―1的碘水 ②1mL 0.001 mol・L―1的碘水
③4mL 0.01 mol・L―1的Na2S2O3溶液 ④4mL 0.001 mol・L―1的Na2S2O3溶液
(2)若某同学选取①③进行实验,测得褪色时间为4s,计算υ(S2O32―)=
4、填空题 (15分)在100℃时,将0.40mol的二氧化氮气体充入2L抽空的密闭容器中,发生反应:
2NO2 N2O4。每隔一定时间就对该容器内的物质进行分析,得到如下表数据: N2O4。每隔一定时间就对该容器内的物质进行分析,得到如下表数据:
时间/s
| 0
| 20
| 40
| 60
| 80
| n(NO2)/mol
| 0.40
| n1
| 0.26
| n3
| n4
| n(N2O4)/mol
| 0.00
| 0.05
| n2
| 0.08
| 0.08
|
?
(1)在上述条件下,从反应开始直至20 s时,二氧化氮的平均反应速率为__________
mol/(L・s)。
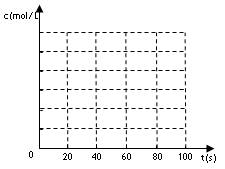
(2)若在相同情况下最初向该容器充入的是四氧化二氮气体,要达到上述同样的平衡状态,四氧化二氮的起始浓度是_________mol/L。假设在80s时达到平衡,请在如图中画出该条
件下N2O4和NO2的浓度随时间变化的曲线。
(3)上述(2)达到平衡后四氧化二氮的转化率为_________,混合气体的平均摩尔质量
为___________。
(4)达到平衡后,如向该密闭容器中再充入0.32molHe气,并把容器体积扩大为4L,则平衡将?(填“向左移动”、“向右移动”或“不移动”)。
5、填空题 在下列事实中,什么因素影响了化学反应的速率?
(1)集气瓶中有H2和Cl2的混合气体,在瓶外点燃镁条时发生爆炸__________;
(2)黄铁矿煅烧时要粉碎成细小的矿粒__________;
(3)KI晶体和HgCl2晶体混合后无明显现象,若一起投入水中,很快生成红色HgI2________;
(4)熔化的KClO3放出气泡很慢,撒入少量MnO2很快产生气体________________;
(5)同浓度、同体积的盐酸中放入同样大小的锌粒和镁块,产生气体有快有慢______;
(6)同样大小的石灰石分别在0.1 mol/L的盐酸和1 mol/L的盐酸中反应速率不同__________;
(7)夏天的食品易变霉,冬天就不易发生该现象______。
|