��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��������Ũ�Ⱦ�Ϊ0.5 mol��L-1��������Һ����̼������Һ��̼��������Һ������ܰ�ˮ���������ĿҪ��ش��������⣺
(1)������Һ�У��ɷ���ˮ�ⷴӦ����___________(����ţ���ͬ)���ڷ���ˮ�ⷴӦ����Һ��pH������____________________��
(2)������Һ�У�����������������Һ��Ӧ��������������Һ��Ӧ����____________________��
(3)ȡ������Һ�ܣ����������Ȼ�粒��壬��ʱ��Һ��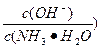 ��ֵ_________(�������С�����䡱)��
��ֵ_________(�������С�����䡱)��
(4)��������Ģۺܵ͢���Һ��Ϻ�������Һ������Ũ���ɴ�С��˳����___________��
(5)ȡ10 mL��Һ�ۣ���ˮϡ�͵�500 mL�������Һ����ˮ�������c(H+)=______________��
2��ѡ���� ���л�ѧ����ʽ�У�����ˮ�ⷴӦ����ȷ����(?)
A��HCO3-+H2O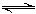 H3O++CO32-
H3O++CO32-
B��CO32-+2H2O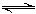 H2CO3+2OH-
H2CO3+2OH-
C��CO32-+H2O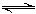 HCO3-+OH-
HCO3-+OH-
D��Cl2+H2O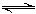 H++ Cl- + HClO
H++ Cl- + HClO
3��ѡ���� �����ʵ���Ũ�ȶ���0.1mol/L��ij����HX��Һ��NaX��Һ�������ϣ�����˵��������ǣ�?��
A������Ϻ���Һ��c(Na+)��c(X-),˵��HX�ĵ���̶�����X-��ˮ��̶�
B���������Һ�����ԣ���c(X-)��c(HX)��c(Na+)��c(H+)��c(OH-)
C�������Һ��c(HX)+ c(X-)=0.1mol/L
D�������Һ��c(HX) + c(H+)= c(Na+)+ c(OH-)
4������� (8��)��֪��A�����ҺpH��a��B�����ҺpH��b��
(1)��AΪ���ᣬBΪ������������a��b��14�����ߵ������ϣ���Һ��pH��________���������Ϊ1 ��10��Ϻ���Һ�����ԣ���a��b��________��
(2)��AΪ���ᣬBΪ�������ƣ���a��4��b��12����ôA��Һ��ˮ�������������Ũ��Ϊ________mol��L��1��B��Һ��ˮ�������������Ũ��Ϊ________mol��L��1��
(3)��AΪ���ᣬBΪ�������ƣ���a��b��14�������ΪVA�Ĵ�������ΪVB������������Һ��Ϻ���Һ�����ԣ����������ϵΪVA________VB(�>������<����������ͬ)����Ϻ���Һ�е�����Ũ�ȹ�ϵΪc(Na��)________
c(CH3COO��)��
(4)��A�Ļ�ѧʽΪHR��B�Ļ�ѧʽΪMOH����a��b��14�����ߵ������Ϻ���Һ�Լ��ԡ�������Һ�бض���һ�������ܷ���ˮ�⣬��ˮ�ⷴӦ�����ӷ���ʽΪ________________________________________________________________________
________________________________________________________________________��
5������� (6��)�����£���0.1mol/L�������0.1mol/L�Ĵ�����Һ���ش��������⣺
�ٱȽ�����Һ��pH ������__���<�� ����="��" �� ��>��������,д���������ķ���ʽ__________��
��������������������Ʒ�Ӧ�����Σ����д������������Ʒ�Ӧ�����ɴ����ƣ�ʵ�������в��ִ����ƹ��壬ȡ��������ˮ����Һ��____������ԡ� �� �����ԡ� �� �����ԡ�������ԭ���ǣ������ӷ���ʽ��ʾ��__________��
�����ԡ� �� �����ԡ�������ԭ���ǣ������ӷ���ʽ��ʾ��__________��
���������Һ�м���һ������NaOH��Һ���������Һ��pH=7ʱ����Һ�����ӵ�Ũ�ȴ�СΪ
?������ĸ����ͬ�����������Һ��pH<7ʱ����Һ�����ӵ�Ũ�ȴ�СΪ?
a��c(Na+)��c(CH3COO��)��c(OH��)��c(H+)
b��c(Na+) = c(CH3COO��)��c(OH��) =c(H+)?
c��c(CH3COO��)��c(Na+)��c(H+)��c(OH��)
d��c(Na+)��c(CH3COO��)��c(H+)��c(OH��)