微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 将0.1mol?L-1的CH3COOH溶液稀释10倍,下列微粒浓度减小得最多的是( )
A.CH3COO-
B.OH-
C.H+
D.CH3COOH
参考答案:CH3COOH溶液中存在:CH3COOH

CH3COO-+H+,加水稀释,促进电解质电离,n(CH3COOH)减小,n(CH3COO-)、
n(H+)增大,由于体积增大程度大于电离程度,则c(CH3COOH)、c(CH3COO-)、c(H+)都减小,
但溶液中还存在水的电离,则c(H+)>c(CH3COO-)>c(CH3COOH),根据Kw=c(H+)?c(OH-),可知c(OH-)浓度增大,
所以微粒浓度减小得最多的是CH3COOH.
故选D.
本题解析:
本题难度:简单
2、选择题 类似于水的离子积,难溶盐AmBn也有离子积Ksp,且Ksp=[C(An+)]m・[C(Bm-)]n。已知常温下BASO4的溶解度为2.33×10-4g,则其Ksp为 (? )
A.2.33×10-4
B.1×10-5
C.1×10-10
D.1×10-12
参考答案:C
本题解析:由于BaSO4溶解度较小,其溶液的密度近似于1 g・cm-3,所以,BaSO4溶液中,c(Ba2+)=c(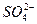 )=1×10-5 mol・L-1,则Ksp=1×10-10。
)=1×10-5 mol・L-1,则Ksp=1×10-10。
本题难度:一般
3、选择题 在100ml下列溶液中,分别加入0.05molNaOH固体,溶液的导电性变化不大的是
A.蒸馏水
B.0.5mol/L的CH3COOH
C.0.5mol/L的HCl
D.0.5mol/L的氨水
参考答案:C
本题解析:溶液的导电性强弱主要和溶液中离子浓度大小以及离子的电荷数有关系。离子浓度越大,电荷数越多,溶液导电性越强。A中离子浓度增加,导电性增强;B中有强电解质醋酸钠生成,导电性增强;C中生成氯化钠,导电性变化不大;D中离子浓度增大,导电性增强,答案选C。
点评:该题的关键是理解溶液的导电性和离子的种类、个数多少无关系。主要是看溶液中离子浓度的大小和离子电荷数,据此可以判断。同时还需要熟练记住常见的强电解质。
本题难度:一般
4、选择题 某探究小组在某温度下测定溶液的pH时发现:0.01mol・L-1的NaOH溶液中,由水电离出的
c(H+)・c(OH-)=10-22,则该小组在该温度下测得0.1mol・L-1NaOH溶液的pH应为
A.13
B.12
C.11
D.10
参考答案:B
本题解析:略
本题难度:简单
5、填空题 今有①CH3COOH;②HCl;③H2SO4三种溶液,选择填空:(在空白处填上相应的字母)
A.①>②>③B.①<②<③C.①=②=③D.①=③>②
E.①>②=③F.①<②=③G.①=②<③H.①=②>③
(1)当它们的c(H+)相同时,其物质的量浓度关系是______.
(2)当它们的物质的量浓度相同时,其溶液中c(H+)的关系是______.
(3)中和等体积、等物质的量浓度的烧碱溶液,需等物质的量浓度的三种酸溶液的体积关系为______.
(4)当它们溶液中c(H+)相同、体积相同时,分别加入足量锌,相同状况下产生气体体积关系为______.
(5)当它们溶液中c(H+)相同、体积相同时,同时加入锌,则开始时反应速率______,若产生相同体积的气体(相同状况),所需时间______.
(6)将溶液中c(H+)相同的三种酸均稀释10倍后,溶液中c(H+)关系为______.
参考答案:(1)当溶液中氢离子浓度相同,假设提供1mol/L的氢离子,需要醋酸浓度应大于1mol/L,需要盐酸溶液浓度为1mol/L,H2SO4 溶液浓度为0.5mol/L,所以其物质的量浓度由大到小排列的是:①>②>③,
故选A;
(2)当它们的物质的量浓度相同时,假设浓度都是1mol/L,CH3COOH溶液电离出氢离子浓度小于1mol/L,HCl电离出氢离子浓度为1mol/L,H2SO4电离出的氢离子浓度为2mol/L,所以氢离子浓度大小顺序是:①<②<③,故选B;
(3)中和等量的烧碱溶液,假设氢氧化钠物质的量为1mol,需要①醋酸1mol,需要②HCl1mol,需要③H2SO40.5mol,所以需同浓度的三种酸溶液的体积大小关系为①=②>③,故选H;
(4)当它们溶液中c(H+)相同、体积相同时,分别加入足量锌,氢元素的物质的量越多,生成氢气则越多,所以醋酸生成氢气最多,盐酸和硫酸生成氢气相同,所以气体体积大小顺序是:①>②=③,故选E;
(5)当它们溶液中c(H+)相同、体积相同时,同时加入锌,反应速率与氢离子浓度成正比,开始时氢离子浓度相同,反应速率相同,故选C;
反应过程中,硫酸和盐酸中氢离子浓度逐渐减小,反应速率逐渐减小,随着反应的进行,醋酸电离出氢离子补充反应的氢离子,所以反应过程中醋酸中氢离子浓度大于硫酸和盐酸,醋酸反应速率快,生成相同体积的氢气所需时间最短,硫酸和盐酸生成相同体积所需氢气时间相同,故选F;
(6)将溶液中c(H+)相同的三种酸均稀释10倍后,醋酸中存在电离平衡,所以加水稀释促进醋酸电离,硫酸和氯化氢都是强电解质,加水稀释改变氢离子个数,所以氢离子浓度相等,醋酸中氢离子浓度最大,则氢离子浓度大小顺序是①>②=③,故选E.
本题解析:
本题难度:一般