微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 X和Y属短周期元素,X原子的最外层电子数是次外层电子数的一半,Y位于X的前一周期,且最外层只有一个电子,下列的说法正确的是:(? )
A.X可能是第二周期非金属元素
B.X可能是第三周期金属元素
C.Y可能与X同主族
D.Y一定是金属元素
参考答案:C
本题解析:在短周期元素中符合最外层电子数是次外层电子数的一半只有锂和硅。Y位于X的前一周期,且最外层只有一个电子,所以Y可以是氢或锂。因此只有选项C正确。答案C。
本题难度:一般
2、选择题 同一主族的两种元素的原子序数之差不可能是(? )
A.16
B.26
C.36
D.46
参考答案:D
本题解析:解法一:元素周期表一~六周期的元素种数分别为2,8,8,18,18,32,因此同一主族的两种元素原子序数之差可能为8+8=16,8+18=26,18+18=36,18+32=50,8+8+18=34,8+18+18=44,18+18+32=68等,不可能为46。
解法二:0族定位法。以惰性元素的原子序数为特例,惰性元素的原子序数分别为2、10、18、36、54、86,则16=18-2,26=36-10,36=54-18,即可得答案选D
本题难度:一般
3、填空题 元素X、Y、Z、M、N均为短周期主族元素,且原子序数依次增大。已知Y原子最外层电子数与核外电子总数之比为3∶4,M原子的最外层电子数与次外层电子数之比为3∶4,且M原子的质子数是Y原子的2倍;N-、Z+、X+ 离子半径逐渐减小;化合物XN常温下为气体,据此回答:

(1)写出Z与N形成化合物的电子式?。
(2)X与Y可分别形成10电子和18电子的分子,写出该18电子分子转化成10电子分子的化学方程式:??。
(3)下图表示由上述两种元素组成的气体分子在一定条件下的密闭容器中充分反应前后的转化关系,请写出该转化过程的化学方程式:
?。
参考答案:(1) ?略?(2分)
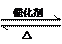 (2)2H2O2
(2)2H2O2 2H2O+O2↑?(其它合理答案亦可)(2分)
2H2O+O2↑?(其它合理答案亦可)(2分)
(3)2SO2+O2? 2SO3(2分,不用可逆符号扣1分)
本题解析:略
本题难度:一般
4、选择题 砷为第4周期第ⅤA族元素,根据它在元素周期表中的位置推测,砷不可能具有的性质
A.AsH3比NH3稳定
B.可以存在-3、+5等多种化合价
C.As2O5对应水化物的酸性比H3PO4弱
D.磷的非金属性比砷强
参考答案:A
本题解析:根据元素周期律可知,同主族自上而下非金属性逐渐减弱,所以A是不正确的,其余都是正确的,答案选A。
本题难度:一般
5、选择题 下列叙述正确的是
①热稳定性:H2O>HF>H2S? ②熔点:Al>Na>K
③IA、IIA族元素的阳离子与同周期稀有气体元素的原子具有相同的核外电子排布
④元素周期表中从ⅢB族到ⅡB族10个纵行的元素都是金属元素
⑤元素的非金属性越强,其氧化物的水化物酸性就越强
⑥已知2H2(g)+O2(g)=2H2O(l);△H=-571KJ・mol-1,则氢气的燃烧热为285.5KJ・mol-1
⑦因为常温下白磷可自燃,而氮气须在放电时才与氧气反应,所以非金属性:P > N
A.只有②④⑥?B.只有①⑥⑦?C.只有②③④ ?D.只有③⑤⑦
参考答案:A
本题解析:略
本题难度:简单