��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��������ͳ�������;�ܹ�����������Իش��������⣺
��1������������һ����ɫ��������д��������������H2O2�����Ȼ����������ӷ�Ӧ����ʽ�� ������ ��������������������
��2��Na2O2��K2O2�� �Լ�BaO2���������������ɹ������⣬Ŀǰʵ������ȡ���������ͨ������ij�ֹ�������������ϡ�������ã����˼����Ƶá����ʺϵĹ���������____________��д����ʽ����
������O3������ʹʪ��ĵ��ۣ��⻯����ֽ��������Ӧ�Ļ�ѧ����ʽΪ��
KI��O3��H2O��KOH��I2��O2��δ��ƽ �� �ش����⣺
�� ��ԭ����Ļ�ѧʽΪ ����
�� ��ƽ��Ļ�ѧ����ʽ��
��4��O3 ���ɳ�����������ԭ������ͼ��ʾ�����ϡ�����Ƶá�
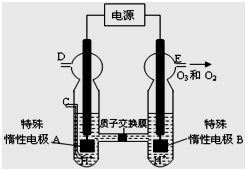
��ͼ������Ϊ ���A����B������
�� ��C����ͨ��O 2 ��D��E���ֱ��ռ���11��2L����4��48L
���壨��״���£��� ��E���ռ���������O3��ռ���������
Ϊ ������ O 3 �ķֽ⣩��
�� ��C��ͨ��O 2����A���ĵ缫��ӦʽΪ�� ��
��5������O3����������ȼú�����е�NOx��SO2�ѳ�Ч����������¯�����е�NOx 95����������NO��ʽ���ڵģ��ɷ�����ӦNO��g��+ O3��g�� NO2��g��+ O2 ��g������һ�������£���NO��O3ͨ����Ⱥ����ܱ������з���������Ӧ ������Ӧ������ʱ��仯��ʾ��ͼ������ͼ����ʾ����ͼ�ɵó�����ȷ˵����
NO2��g��+ O2 ��g������һ�������£���NO��O3ͨ����Ⱥ����ܱ������з���������Ӧ ������Ӧ������ʱ��仯��ʾ��ͼ������ͼ����ʾ����ͼ�ɵó�����ȷ˵����
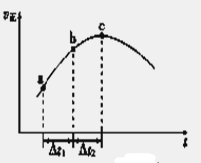
a����Ӧ��c��ﵽƽ��״̬
b����Ӧ��Ũ�ȣ�b��С��c��
c����Ӧ��������������������������
d����t1����t2ʱ��NO��ת���ʣ�a��b��С��b��c��
2��ѡ���� ��֪��ӦmX��g��+nY��g��?qZ��g������H��0��m+n��q���ں����ܱ������з�Ӧ�ﵽƽ��ʱ�������й�˵����ȷ���ǣ�������
A���������ͨ��һ����ij����ʹ��ϵѹǿ����ƽ�⽫�����ƶ�
B����ʱ��X������Ӧ������Y���淴Ӧ���ʵ�
��
C����������¶ȣ��ұ�������״̬�������ı䣬��������ƽ����Է���������С
D���������X�����ʵ�����ƽ�������ƶ���X��ת��������
3��ѡ���� ij�¶��£��ڹ̶��ݻ��������У����淴ӦA��g��+3B��g���T2C��g���ﵽƽ�⣬��ʱ���n��A����n��B����n��C��=2��2��1���������¶Ȳ��䣬��n��A����n��B����n��C��=2��2��1�ı�������������ٳ���A��B��C��������
A��ƽ��������Ӧ�����ƶ�
B��ƽ�����淴�����ƶ�
C��ƽ�ⲻ�����ƶ�
D��n��C����С
4������� ��������ЧӦ����Դ��ȱ�����⣬��ν��ʹ����е�CO2���������Կ������ã������˸������ձ����ӡ�Ŀǰ��ҵ����һ�ַ�������CO2����ȼ�ϼ״���һ�������·�����Ӧ��
CO2(g)+3H2(g) CH3OH(g)+H2O(g)��ͼ1��ʾ�÷�Ӧ����������(��λΪkJ��mol��1)�ı仯��
CH3OH(g)+H2O(g)��ͼ1��ʾ�÷�Ӧ����������(��λΪkJ��mol��1)�ı仯��
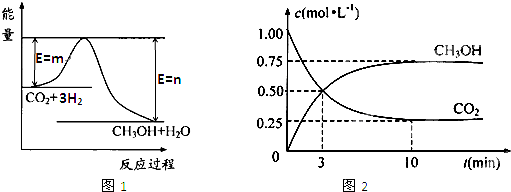
��1��д���÷�Ӧ���Ȼ�ѧ����ʽ ��
��2�����ڸ÷�Ӧ������˵���У���ȷ���� ��
A����H��0����S��0 B����H��0����S��0 C����H��0����S��0 D����H��0����S��0
��3���÷�Ӧ��ƽ�ⳣ��K�ı���ʽΪ�� ��
��4���¶Ƚ��ͣ�ƽ�ⳣ��K ������� �����䡱��С������
��5��Ϊ̽����Ӧԭ�����ֽ�������ʵ�飺�����Ϊ1 L���ܱ������У�����1 molCO2��3 molH2�����CO2��CH3OH(g)��Ũ����ʱ��仯��ͼ2��ʾ���ӷ�Ӧ��ʼ��ƽ�⣬������Ũ�ȱ仯��ʾ��ƽ����Ӧ����v (H2)�� ��
��6�����д�ʩ����ʹ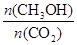 ������� ��
������� ��
A�������¶�
B���������
C����H2O(g)����ϵ�з���
D��������䣬����He(g)ʹ��ϵ��ѹǿ����
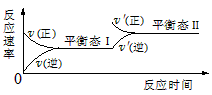
5��ѡ���� ��ͼ�Ǻ�����ij��ѧ��Ӧ�ķ�Ӧ�����淴Ӧʱ��仯��ʾ��ͼ������������ʾ��ͼ������ϵ���
[? ]
A����Ӧ��ƽ��ʱ������Ӧ���ʺ��淴Ӧ�������
B���÷�Ӧ�ﵽƽ��̬I������Ӧ��Ũ�ȣ�ƽ�ⷢ���ƶ����ﵽƽ��̬II
C���÷�Ӧ�ﵽƽ��̬I��С��Ӧ��Ũ�ȣ�ƽ�ⷢ���ƶ����ﵽƽ��̬II
D��ͬһ�ַ�Ӧ����ƽ��̬I��ƽ��̬IIʱŨ�Ȳ����