微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 粗CuO是将工业废铜、废铜合金等高温焙烧而成的,杂质主要是铁的氧化物及泥沙。以粗CuO为原料制备胆矾的主要流程如下:
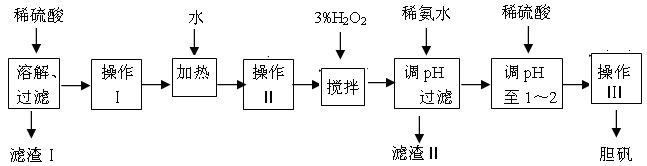
已知Fe3+、Fe2+ 、Cu2+转化为相应氢氧化物时,开始沉淀和沉淀完全时的pH如下表:
?
| Fe3+
| Fe2+
| Cu2+
|
开始沉淀时的pH
| 2.7
| 7.6
| 5.2
|
完全沉淀时的pH
| 3.7
| 9.6
| 6.4
|
?
(1)加入3% H2O2之前必须进行操作Ⅱ,操作Ⅱ的名称是?;
H2O2参加反应的离子方程式为?。
(2)加稀氨水调节pH的目的是?,pH应调至?范围。下列物质可用来替代稀氨水的是?。
①NaOH?②Fe2O3?③CuO?④Na2CO3
(3)经操作Ⅰ得到粗胆矾,操作Ⅲ得到精致胆矾。两步操作相同,具体包括?、?、
过滤、?、干燥等步骤。
2、选择题 在一定温度下,一定量的水中,石灰乳悬浊液存在下列平衡:Ca(OH)2(s) Ca(OH)2(aq)
Ca(OH)2(aq) Ca2+(aq)+2OH-(aq),当向此悬浊液中加入少量生石灰时,下列说法正确的是(? )
Ca2+(aq)+2OH-(aq),当向此悬浊液中加入少量生石灰时,下列说法正确的是(? )
A.n(Ca2+)增大
B.c(Ca2+)不变
C.n(OH-)增大
D.c(OH-)减小
3、计算题 难溶电解质在水溶液里存在着电离平衡。在常温下,溶液里各离子浓度以它们的系数为方次的乘积是一个常数,该常数叫溶度积(Ksp)。例如FeS(s)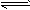 Fe2+(aq)+S2-(aq) ,Ksp = c(Fe2+)・c(S2-)=6.25×10-18 。溶液里各离子浓度幂的乘积,大于溶度积时则出现沉淀;反之沉淀溶解。试根据上述原理,计算:
Fe2+(aq)+S2-(aq) ,Ksp = c(Fe2+)・c(S2-)=6.25×10-18 。溶液里各离子浓度幂的乘积,大于溶度积时则出现沉淀;反之沉淀溶解。试根据上述原理,计算:
(1)求常温下FeS的溶解度________g/100g水)。(设饱和溶液的密度为1g・cm-3)
(2)求常温下H2S的饱和溶液中,c(H+)与c(S2-)间存在关系有[c(H+)]2・[c(S2-)]=1.0×10-22,在该温度下,将适量FeS投入H2S饱和溶液中,欲使溶液中c(Fe2+)达到1mol/L,应调节溶液的pH为多少?(已知:lg2≈0.3)
4、选择题 已知如下物质的溶度积常数:FeS,Ksp=6.3×10-18;CuS,Ksp=1.3×10-36;ZnS,Ksp=1.6×10-24。下列说法正确的是? ( )
A.同温度下,CuS的溶解度大于ZnS的溶解度
B.将足量CuSO4溶解在0.1 mol・L-1的H2S溶液中,Cu2+能达到的最大浓度为1.3×10-35mol・L-1
C.因为H2SO4是强酸,所以Cu2++H2S=CuS↓+2H+不能发生
D.除去工业废水中的Cu2+,可以选用FeS作沉淀剂
5、选择题 一定温度下,难溶强电解质的饱和溶液中存在着沉淀溶解平衡,其平衡常数为
物质
| Fe(OH)2
| Cu(OH)2
| Fe(OH)3
|
Ksp(25℃)
| 8.0×10
|