��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ����˵���У���ȷ����
A������ԭ��������缫�IJ���һ�������ֲ�ͬ�Ľ���
B����ͭ��п���缫������ͭ��Һ��ɵ�ԭ�����ͭ������
C������ͨ�������п����ͭ��ͨ��������Һ�������ӵõ�������
D��ͭ��пԭ��ع���ʱ������13gп�ܽ⣬��·����0.2mol����ͨ��
�ο��𰸣�B
���������A����ȷ��Ҳ�����ǽ����ͷǽ�����ԭ����нϻ��õĽ����Ǹ�����ʧȥ���ӣ�����������Ӧ�����Ӿ����ߴ��ݵ�������������Һ�е��������������ƶ��������õ����ӣ�������ԭ��Ӧ������ѡ��B��ȷ��C����ȷ��13gп��ʧȥ����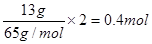 ��D����ȷ����ѡB��
��D����ȷ����ѡB��
�����Ѷȣ�һ��
2��ѡ���� ij��ص��ܷ�Ӧ�����ӷ���ʽΪ2Fe3���� Fe �� 3Fe2��������ʵ�ָ÷�Ӧ��ԭ����ǣ�?��
����?����?�������Һ?
A��Cu Fe FeCl3
B��C Fe Fe��NO3��3
C��Fe Zn Fe2��SO4��3
D��Ag Fe CuSO4
�ο��𰸣�CD
�����������ʵ�ָ÷�Ӧ��ԭ��ر������㣺�ٵ������Һ����Fe3�����ڸ�������ΪFe�����������ϱ�Fe�Ļ����������ܵ�������ʡ���C��D��������������������
�����Ѷȣ���
3������� ��10�֣�ij�о���ѧϰС�飬Ϊ��̽���缫��ԭ��صĵ����֮���ϵ�����������ʵ�鷽��������Ƭ��ͭƬ��þƬ���缫���ֱ���������Һ����ԭ��أ����ӵ�������
��1�����������ҺΪ0.5mol/L���ᣬ�缫ΪͭƬ����Ƭ���������ָ��ƫ��??���������ͭ������
��2������Ũ�������������Һ���缫ΪͭƬ����Ƭ���������ָ��ƫ��?���������ͭ����������?��������������������ϵ缫��ӦʽΪ��?
��3�����������ҺΪ0.5mol/L����������Һ���缫ΪþƬ����Ƭ�������������ĵ缫��ӦΪ?��
ͨ������ʵ��̽�������ܵ�����ʾ�� ?
?
�ο��𰸣���10�֣���1������ ��2��ͭ������ 2NO3-+2e-+4H+=2NO2��+2H2O
��3��2H2O+2e-=2OH-+H2�� ��ʾ1���缫������������Һ�����йأ���ʾ2���������������ij��Һ���ԣ���ͬ���������ͬһ�ֽ��������ܻ����Է����仯����ʾ3�����ݵ缫���ͱȽϽ��������Բ�һ����ȷ����ʾ4������ͨ����������ȷ����������Ի����ԡ�
�����������1���缫ΪͭƬ����Ƭ�������Ϊ������Һʱ������Ϊ�������ӵ���������Ϊ�����������������ķ���Ϊ�������������ʵ�����ָ��ƫ����������2��Ũ�������������Һʱ�����ۻ�����ͭ����������ط�ӦΪͭ��Ũ���ᷴӦ������������������ӵõ������ɶ����������缫��ӦʽΪ��2NO3-+2e-+4H+=2NO2��+2H2O����3���������ҺΪ0.5mol/L����������Һ���缫ΪþƬ����Ƭʱ����Ϊþ���������Ʋ���Ӧ���ʸ���Ϊ������ط�ӦΪ�����������Ʒ�Ӧ����������ӦΪ��2H2O+2e-=2OH-+H2�����������ʾ��Ҫ�Ǹ������ϲ����������ڽ����Ļ�ԣ���Ҫ���ǵ������Һ�����ǵ�ط�Ӧ��
�����Ѷȣ�һ��
4������� (14��)ij��������ˮ������ͼ��ʾװ�ô�������װ�ÿɽ���ˮ�е�Cr2O72-��ԭΪCr3+��
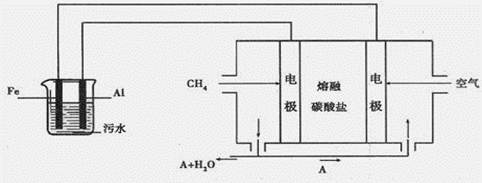
��1��ͼ����������װ���У�?������ҡ���װ��Ϊ���ء���Դ�и����Ļ�������Ϊ??(�ѧʽ)����Դ�����缫�䣬������ɵ������˶��ķ���Ϊ?����������ҡ����ҵ�����������Ϊ?(�ѧʽ)��
��2����д�������ϵĵ缫��Ӧʽ��Cr2O72-����ԭΪCr3+�����ӷ���ʽ�ֱ��ǣ�
?��?��
��3��Ϊ��֤����������ͼ��A���ʱ���ѭ��ʹ�ã��仯ѧʽΪ��?��
��4����ϵԪ�ؾ�Ϊϡ��Ԫ�أ��������缫��λ��Ԫ�����ڱ��������ڣ�������Ԫ���γɵ����������м�����ǿ��Ϊ?����д��ѧʽ�����棨Ce����������������Ce(OH)3��Ce(OH)4��ǰ�߶Կ����Ƚ����У����û�ѧ����ʽ��ʾ��ԭ��?��
�ο��𰸣���14�֣�
����(2��)��CH4(1��)�����ҵ���(2��)��CO32-(1��)
��Fe-2e-=Fe2+(2��)��6Fe2++Cr2O72-+11H2O=6Fe(OH)3��+2Cr3++4H+(2��)
��CO2(1��)
��CsOH(1��)��4Ce(OH)3+O2+2H2O=4Ce(OH)4(2��)
�����������1������ӵ�ԴʱΪ���أ���װ������ӵ�Դ���ڵ��أ�û��ӵ�ԴΪԭ��أ���װ��û����ӵ�ԴΪCH4ȼ�ϵ�أ�����ȼ�ϵ���У�ͨ�����һ��Ϊ��������������������Ӧ������ʧȥ���ӣ��ڼ�������������̼������ӣ�������ӦΪ��CH4+10OH--8e-=CO32-+7H2O����Դ�����缫�䣬������ɵ�CO32-������ԭ��صĸ����ƶ��������˶��ķ���Ϊ���ҵ���
��2���������Ե缫������ʧȥ���ӣ��缫����ʽΪ��Fe-2e-=Fe2+�������������л�ԭ�ԣ�Cr2O72-��ǿ�����ԣ������ܷ���������ԭ��Ӧ�����������ӱ����������������ӣ�Cr2O72-����ԭΪCr3+����Ӧ����ʽΪ��Cr2O72-+6Fe2++14H+�T2Cr3++6Fe3++7H2O��
��3���Ʊ������õ�ԭ�ϣ���ת�������������ɵĿ���ѭ�����ã���ת����ϵͼ֪��ͨ��������һ��Ϊԭ��ص���������缫��ӦʽΪO2+4e-+2CO2=2CO32-��ͬʱ��������������Ӧ������ʧȥ���ӣ��ڼ�������������̼������ӣ�������ӦΪ��CH4+10OH--8e-=CO32-+7H2O����AΪCO2��ͬʱ�����ж�CO2����ѭ�����á�
��4��ͬ����Ԫ�ش�����Ԫ�صĽ�����������CS��Ԫ�����ڱ��������ڵڢ�A��Ԫ�أ�����Ԫ�صĽ�������ǿ����CS�����������м�����ǿ��ΪCsOH��Ce��OH��3��Ce��OH��4��Ce�Ļ��ϼ۷ֱ�Ϊ+3��+4��Ce��OH��3�ױ�����������Ce��OH��4����ӦΪ��4Ce��OH��3+O2+2H2O=4Ce��OH��4�������к���ˮ����������������Ce��OH��3�Կ����Ƚ����С�
�����Ѷȣ�һ��
5��ѡ���� ������ͼ���ж��������ӷ���ʽ�д�����ǣ�?��
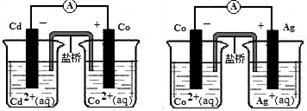
A��2Ag(s)+Cd2+(aq)=2Ag+(aq)+Cd(s)
B��Co2+(aq)+Cd(s)=Co(s)+Cd2+(aq)
C��2Ag+(aq)+Cd(s)=2Ag(s)+Cd2+(aq)
D��2Ag+(aq)+Co(s)=2Ag(s)+Co2+(aq)
�ο��𰸣�A
�������������ԭ�������������֪��������ǿ��˳����Ag����CO2����Cd2��������Cd2��������������������A�Dz����ܵģ��������ȷ�ģ���ѡA��
�����Ѷȣ�һ��