��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��һ�������£�Na2CO3��Һ����ˮ��ƽ�⣺CO32-+H2O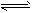 HCO3-+OH-������˵����ȷ����
HCO3-+OH-������˵����ȷ����
[? ]
A��ϡ����Һ��ˮ��ƽ�ⳣ������
B��ͨ��CO2��ƽ�⳯����Ӧ�����ƶ�
C�������¶ȣ�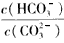 ��С
��С
D������NaOH���壬��ҺpH��С
�ο��𰸣�B
���������
�����Ѷȣ�һ��
2��ѡ���� �ܹ���������Һ��ˮ�⣬������Է���������ͬ���������ʵ���
A������
B������
C����֬
D����ѿ��
�ο��𰸣�A
�����������
�����Ѷȣ���
3��ѡ���� ����˵���У���ȷ���ǣ�?��
A����ͭ����ʱ����������0.5molCu2+��������NA��Cuԭ������
B����Ϊ����H2SO3��H2CO3������S�õ�����������C
C����ͨ���Ƚ�Mg��OH��2��MgCO3��Ksp�Ĵ�С �Ƚ����ǵ��ܽ���
D����0.1molNaClO����Һ���ɿɵ�5.85gNaCl����
�ο��𰸣�D
���������A�����ڴ�ͭ�к������ʣ���ʼʱ��������ͭʧȥ���ӣ�������ʼ����ͭ���ӷŵ硣��˴�ͭ����ʱ����������0.5molCu2+��������һ����NA��Cuԭ��������A����ȷ���ǽ�����Խǿ������������ˮ���������Խǿ���������ǿ�ᣬB����ȷ��C��������þ��̼��þ����ɽṹ��ͬ�����Բ���ͨ���Ƚ�Mg��OH��2��MgCO3��Ksp�Ĵ�С �Ƚ����ǵ��ܽ��ԣ�C����ȷ��D��������������ˮ��ˮ�����ɴ�������������ƣ����ڴ�����ȶ����ֽ������Ȼ�����������������յõ������Ȼ��ơ�����ԭ���غ��֪���Ȼ��Ƶ����ʵ�����0.1mol��D��ȷ����ѡD��
�����Ѷȣ�һ��
4��ѡ���� ����ʱ��V1mL c1 mol/L�Ĵ���μӵ�V2 mL c2 mol/L���ռ���Һ�У����н�����ȷ����
A����V1=V2�һ����ҺpH��7������c1��c2
B����c1V1= c2V2��������Һ��c��Na����= c��CH3COO����
C���������Һ��pH=7������c1V1��c2V2
D���������Һ��pH=7��������Һ��c��Na������c��CH3COO����
�ο��𰸣�AC
�����������V1=V2��c1= c2����c1V1= c2V2�����������ռ�ǡ����ȫ�кͣ��õ������ƺ�ˮ����������ǿ�������Σ���������ˮ����ɿ�֪�����ҺpH>7����ʹ�����ҺpH<7�������һ����������c1>c2����A��ȷ����c1V1= c2V2�����������ռ�ǡ����ȫ�кͣ���Ϻ�õ�CH3COONa��Һ��CH3COONa��ǿ�������Σ������Ӳ�ˮ�⣬��������Ӳ���ˮ�⣬���ͺ���Һ��c(Na+)>c(CH3COO��)����B�������������ռ�ǡ����ȫ�кͣ������ҺpH>7����ʹ�����ҺpH=7�����������ʵ���������c1V1>c2V2����C��ȷ�������Һ�к��е�������CH3COO����Na+��H+��OH�����ɵ���غ�ԭ���ɵã�c(H+)+c(Na+)=c(CH3COO��)+ c(OH��)�������ҺpH=7����c(H+)=c(OH��)�����c(Na+)=c(CH3COO��)����D����
�����Ѷȣ���
5��ѡ���� �й�0.1 mol/L��NH4Cl��Һ������˵���������
A��[H+]+[NH4+]=[Cl-]+[OH-]
B��[Cl-]>[NH4+]>[H+]>[OH-]
C��[H+]=[OH-]+[NH3�qH2O]
D����ˮϡ�ͣ�NH4+��ˮ��̶�����������ǿ
�ο��𰸣�D
��������������������ˮ�⼰��Ũ�ȵĴ�С�Ƚϡ�NH4Cl��Һ�д��ڵ���غ㣺[H+]+[NH4+]=[Cl-]+[OH-]�������غ㣺[NH3�qH2O]+[NH4+]=[Cl-]������ʽ����ǰʽ�ɵã�[H+]=[OH-]+[NH3�qH2O]
��ϡ�����У���Ȼ�ٽ��ε�ˮ�⣬������������Һ�����Լ������ʴ�ΪD
�����Ѷȣ�һ��