微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
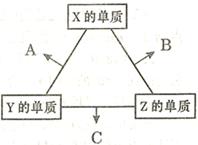
1、填空题 (16分)X、Y、Z三种短周期元素,其单质在常温下均为无色气体,它们的原子序数之和为16。在适当条件下三种单质两两化合,可发生如右图所示变化。己知l个B分子中含有Z元素的原子个数比C分子中含有Z元素的原子个数少1个。请回答下列问题:
 ?
?
(1)由 X、Y、Z三种元素共同组成的三种不同种类的常见化合物的化学式为?,相同浓度上述水溶液中由水电离出的c(H+)最小的是?(填写化学式)。
(2)Allis-Chalmers制造公司发现可以用C作为燃料电池的燃料,以氢氧化钾溶液为介质,反应生成对环境无污染的常见物质,试写出该电池负极的电极反应式?,溶液中OH-向?极移动(填“正”或“负”)。
(3)Z分别与X、Y两元素可以构成18个电子分子甲和乙,其分子中只存在共价单键,常温下甲、乙均为无色液体,甲随着温度升高分解速率加快。
①乙能够将CuO还原为Cu2O,已知每lmol乙参加反应有4mole- 转移,该反应的化学方程式为?。
②将铜粉末用10%甲和3.0mol?L-1H2SO4混合溶液处埋,测得不同温度下铜的平均溶解速率如下表:
温度(℃)
| 20
| 30
| 40
| 50
| 60
| 70
| 80
|
铜的平均溶解速率
(×10-3mol?L-1・min-1)
| 7.34
| 8.01
| 9.25
| 7.98
| 7.24
| 6.73
| 5.76
|
由表中数据可知,当温度高于40℃时,铜的平均溶解速率随着温度的升高而下降,其主要原因是?
_____________________________________________________。
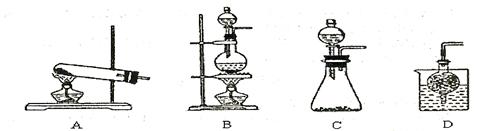
③实验室可用甲作试剂取X的单质,发生装置可选用下图中的?(填装置代号)。
参考答案:(1)HNO3、NH4NO3、NH3・H2O (3分)? HNO3?(1分)
(2)4NH3 + 12OH - 12e- =2N2 + 12H2O?(3分)?负(2分)
(3)①N2H4 + 4CuO = N2↑ + 2Cu2O + 2H2O(3分)
②高于40℃后,H2O2的分解速率加快,c(H2O2)降低,使铜的溶解速率减慢 (2分) ③C (2分)
本题解析:X、Y、Z三种短周期元素,其单质在常温下均为无色气体,短周期中形成无色气体单质的只有H2、N2、O2(稀有气体除外),H、N、O原子序数之和为16,故三种元素为H、N、O,三种气体单质相互反应生成H2O、NH3、NO,一个B分子中含有的Z元素的原子个数比一个C分子中少一个,则B为H2O,C为NH3,Z为氢元素.由关系图可知:Z单质与X单质反应生成B(H2O),故X为氧元素;Z单质与Y单质反应生成C(NH3),故Y为氮元素;所以A为NO,则:
(1)由 X、Y、Z三种元素共同组成的三种不同种类的常见化合物一般是酸碱盐,因此化学式分别为HNO3、NH4NO3、NH3・H2O。硝酸和氨水抑制水的电离,硝酸铵水解促进水的电离。硝酸是一元强酸,氨水是一元弱碱,因此相同浓度上述水溶液中由水电离出的c(H+)最小的是HNO3。
(2)原电池中负极失去电子,正极得到电子,因此在该燃料电池中氨气在负极通入,若以氢氧化钾溶液为介质,反应生成对环境无污染的常见物质,该物质应该是氮气和水,因此该电池负极的电极反应式4NH3 + 12OH - 12e- =2N2 + 12H2O。原电池中阳离子向正极移动,阴离子向负极移动,所以溶液中OH-向负极移动。
(3)Z分别与X、Y两元素可以构成18个电子分子甲和乙,其分子中只存在共价单键,常温下甲、乙均为无色液体,甲随着温度升高分解速率加快,所以甲是双氧水,乙是N2H4。
①乙能够将CuO还原为Cu2O,已知每lmol乙参加反应有4mole- 转移,由于N2H4中氮元素的化合价是-2价,这说明在反应中氮元素化合价升高2个单位,因此其氧化产物是氮气,所以该反应的化学方程式为N2H4 + 4CuO = N2↑ + 2Cu2O + 2H2O。
②由于双氧水不稳定,受热易分解,因此高于40℃后,H2O2的分解速率加快,c(H2O2)降低,使铜的溶解速率减慢。
③在催化剂的作用下双氧水分解生成氧气和水,反应不需要加热,因此选择装置是C。
本题难度:一般
2、选择题 下列俗称表示同一物质的是
A.苏打、小苏打
B.明矾、绿矾
C.消石灰、熟石灰
D.纯碱、烧碱
参考答案:C
本题解析:消石灰和熟石灰都是指氢氧化钙.
本题难度:简单
3、选择题 如果n为第ⅡA族中某元素的原子序数,则原子序数为(n+1)的元素可能位于( )。
A.ⅢA或ⅢB
B.ⅣA
C.ⅠB
D.ⅠA
参考答案:A
本题解析:在元素周期表中,第2、3周期中第ⅡA族与第ⅢA族元素原子序数相差1,在第4、5、6、7周期中,第ⅡA族与第ⅢB族相邻,故原子序数为(n+1)的元素位于第ⅢA或ⅢB族,A正确。
本题难度:一般
4、选择题 有a、b、c、d四种金属,将a与b用导线连结起来浸入稀硫酸溶液中,b不被腐蚀。将a、d分别投入等浓度的盐酸中,d比a反应剧烈;将Cu浸入b的盐溶液里,无明显变化。如果把Cu浸入c的盐溶液里,有c的单质析出。据此判断它们的活动性由强到弱的顺序是(? )
A.d>c>a>b
B.d>b>a>c
C.b>a>d>c
D.d>a>b>c
参考答案:D
本题解析:将a与b用导线连结起来浸入稀硫酸溶液中,b不被腐蚀。则活动性a>b;将a、d分别投入等浓度的盐酸中,d比a反应剧烈;则金属活动性d>a;将Cu浸入b的盐溶液里,无明显变化。则活动性b>Cu;如果把Cu浸入c的盐溶液里,有c的单质析出。则活动性Cu >c;所以金属活动性:d>a>b>c 。故选项是D。
本题难度:一般
5、填空题 下表是元素周期表的一部分,表中所列字母分别代表某一化学元素。用化学用语回答下列问题。
a
| ?
| ?
|
?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| b
| c
| d
| ?
| ?
|
e
| ?
| f
| g
| ?
| h
| i
| ?
|
?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
|
?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
|
?
(1)d、e、f的离子半径由大到小的顺序为?
b、c、g的最高价含氧酸的酸性由强到弱的顺序为?
a与g、h、i形成的简单化合物的稳定性由强到弱的顺序为?
(2)i元素的最高价氧化物对应的水化物为?,它与e的最高价氧化物对应水化物反应的离子方程式为?。
实验室制取i单质的化学方程式为?
(3)呈两性的氢氧化物溶于强碱的离子方程式为??
(4)e与d能形成一种淡黄色的化合物它的化学键类型为?它与h的低价态氧化物反应的化学方程式为??。
参考答案:(1)O2->Na+>Al3+? HNO3>H2CO3>H2SiO3? HCl>H2S>SiH4?(3分)
(2)HClO4 (1分)? OH-+H+ = H2O? (1分)MnO2 +? 4HCl(浓) MnCl2 + Cl2 ↑+ 2H2O? (2分)
MnCl2 + Cl2 ↑+ 2H2O? (2分)
(3)Al(OH)3+OH- = AlO2-+2H2O? (2分)
(4)离子键和非极性共价键 (2分)? Na2O2+SO2=Na2SO4(2分)
本题解析:根据各元素在元素周期表中的位置可推知:a为H,b为C,c为N,d为O,e为Na,f为Al,g为Si,h为S,i为Cl。
(1)d、e、f的离子为O2?、Na+、Al3+,电子排布相同,原子序数越大,离子半径越小,所以O2->Na+>Al3+;b、c、g的最高价含氧酸分别为H2CO3、HNO3、H2SiO3,根据元素周期律酸性:HNO3>H2CO3>H2SiO3;a与g、h、i形成的简单化合物分别为SiH4、H2S、HCl,稳定性由强到弱的顺序为:HCl>H2S>SiH4。
(2)i元素的最高价氧化物对应的水化物为HClO4;e的最高价氧化物对应水化物为NaOH,反应的离子方程式为:OH-+H+ = H2O;实验室由MnO2与浓盐酸反应制取Cl2,化学方程式为:MnO2 +? 4HCl(浓)? ?MnCl2 + Cl2 ↑+ 2H2O。
?MnCl2 + Cl2 ↑+ 2H2O。
(3)呈两性的氢氧化物是Al(OH)3,溶于强碱的离子方程式为:Al(OH)3+OH- = AlO2-+2H2O。
(4)e与d能形成一种淡黄色的化合物为Na2O2,含有离子键和非极性共价键;h的低价态氧化物为SO2,Na2O2能把SO2氧化为Na2SO4,化学方程式为:Na2O2+SO2=Na2SO4。
本题难度:一般